名校
1 . 在容积不变的密闭容器中进行如下反应:H2O(g)+C(s)  H2(g)+CO(g) △H>0,达到平衡后,改变下列反应条件,相关叙述正确的是
H2(g)+CO(g) △H>0,达到平衡后,改变下列反应条件,相关叙述正确的是
 H2(g)+CO(g) △H>0,达到平衡后,改变下列反应条件,相关叙述正确的是
H2(g)+CO(g) △H>0,达到平衡后,改变下列反应条件,相关叙述正确的是| A.加入H2O(g),平衡向正反应方向移动,体系压强减小 |
| B.加入少量C,正反应速率增大,平衡向正反应方向移动 |
| C.降低温度,平衡向正反应方向移动 |
| D.升高温度,混合气体的密度增大 |
您最近一年使用:0次
2021-10-13更新
|
375次组卷
|
3卷引用:宁夏回族自治区石嘴山市第三中学2023-2024学年高二9月月考化学试题
名校
2 . 可逆反应:2X(g)+Y(g)  2Z(g)的平衡状态下,保持恒温恒容向容器中加入一定量的Y,下列说法正确的是(K为平衡常数,Q为浓度熵)
2Z(g)的平衡状态下,保持恒温恒容向容器中加入一定量的Y,下列说法正确的是(K为平衡常数,Q为浓度熵)
 2Z(g)的平衡状态下,保持恒温恒容向容器中加入一定量的Y,下列说法正确的是(K为平衡常数,Q为浓度熵)
2Z(g)的平衡状态下,保持恒温恒容向容器中加入一定量的Y,下列说法正确的是(K为平衡常数,Q为浓度熵)| A.Q不变, K变大, Y的转化率增大 | B.Q不变, K变大, X的转化率减小 |
| C.Q变小, K不变, Y的转化率减小 | D.Q增大, K不变, X的转化率增大 |
您最近一年使用:0次
2021-10-13更新
|
245次组卷
|
4卷引用:宁夏回族自治区石嘴山市第三中学2023-2024学年高二9月月考化学试题
名校
3 . 下列关于化学平衡的叙述,正确的是
A.2NO2(g)  N2O4(g) ΔH < 0,反应达平衡后,压缩体系体积,平衡正向移动,体系颜色变浅 N2O4(g) ΔH < 0,反应达平衡后,压缩体系体积,平衡正向移动,体系颜色变浅 |
B.H2(g)+I2(g)  2HI(g) ΔH < 0,反应达平衡后,增大体系体积,平衡不移动,体系颜色不变 2HI(g) ΔH < 0,反应达平衡后,增大体系体积,平衡不移动,体系颜色不变 |
C.FeCl3(aq)+3KSCN(aq)  Fe(SCN)3(aq)+3KCl(aq),反应达平衡后,向体系中加入少量 KCl 固体,平衡逆向移动,体系颜色变浅 Fe(SCN)3(aq)+3KCl(aq),反应达平衡后,向体系中加入少量 KCl 固体,平衡逆向移动,体系颜色变浅 |
D.N2(g)+3H2(g)  2NH3(g),反应达平衡后,保持体系压强不变,充入He,平衡逆向移动,体系中NH3的体积分数减小 2NH3(g),反应达平衡后,保持体系压强不变,充入He,平衡逆向移动,体系中NH3的体积分数减小 |
您最近一年使用:0次
2021-10-13更新
|
745次组卷
|
10卷引用:宁夏石嘴山市第三中学2020-2021学年高二上学期期中考试化学试题
宁夏石嘴山市第三中学2020-2021学年高二上学期期中考试化学试题宁夏石嘴山市第三中学2021-2022学年高二下学期第一次月考化学试题四川省成都市第七中学2020-2021学年高二上学期十月阶段性考试化学试题安徽省池州市第一中学2020-2021学年高二上学期期中考试化学试题江西省南昌市八一中学2020-2021学年高二上学期期中考试化学试题重庆市第七中学校2021-2022学年高二上学期第一次月考化学试题四川省成都外国语学校2021-2022学年高二上学期10月月考化学试题2021年辽宁高考化学试题变式题11-19江西省吉安市遂川中学2021-2022学年高二上学期第三次月考(B)化学试题黑龙江省牡丹江穆棱市第二中学2021-2022学年高二上学期期末考试化学试题
名校
4 . 一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g) 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是
 2SO3(g)(正反应放热),测得反应的相关数据如下:
2SO3(g)(正反应放热),测得反应的相关数据如下:| 容器1 | 容器2 | 容器3 | |
| 反应温度T/K | 700 | 700 | 800 |
| 反应物投入量 | 2molSO2、1molO2 | 4molSO3 | 2molSO2、1molO2 |
| 平衡v正(SO2)/mol/(L·s) | v1 | v2 | v3 |
| 平衡c(SO3)mol/L | c1 | c2 | c3 |
| 平衡体系总压强p/Pa | p1 | p2 | p3 |
| 物质的平衡转化率/α | α1(SO2) | α2(SO3) | α3(SO2) |
| 平衡常数K | K1 | K2 | K3 |
| A.v1<v2,c2<2c1 | B.K1>K3,p2>2p3 |
| C.v1>v3,α1(SO2)>α3(SO2) | D.c2>2c3,α2(SO3)+α3(SO2)<1 |
您最近一年使用:0次
2021-08-14更新
|
1546次组卷
|
25卷引用:宁夏银川一中2020-2021学年高二上学期期末考试化学试题
宁夏银川一中2020-2021学年高二上学期期末考试化学试题天津市静海区第一中学2020届高三下学期第六周周末训练化学试题人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第二节 化学平衡 高考帮人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 过高考 3年真题强化闯关浙江省诸暨市2019-2020学年高二上学期期末考试化学试题浙江省宁波市九校2020-2021学年高二上学期期末联考化学试题(已下线)【绍兴新东方】绍兴高中化学00008(已下线)【浙江新东方】高中化学20210304-010(已下线)专题06 化学反应速率和化学平衡——备战2021年高考化学纠错笔记(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)四川省蓬安中学校2019-2020学年高二上学期开学考试化学试题(已下线)课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)福建省龙岩市武平县第一中学2021-2022学年高二上学期9月月考化学试题广西浦北中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.3.3 温度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)2.3.2 压强变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)吉林省长春市第二中学2021-2022学年高二上学期第一次月考化学试题江西省吉安一中2021-2022学年高二上学期第一次段考化学试题江西省九江市第一中学2021-2022学年高二上学期期中考试化学试题江西省宜春市八校2022-2023学年高二上学期12月联考化学试题河北省部分学校2023-2024学年高二上学期10月联考化学试题安徽省当涂第一中学2023-2024学年高二上学期10月月考化学试题
名校
5 . 已知反应X(g)+3Y(g) ⇌2Z(g) △H的能量变化如下图所示。下列说法正确的是


| A.△H= E2- E1 | B.更换高效催化剂,E3不变 |
| C.恒压下充入一定量的氦气n(Z)减少 | D.压缩容器,c(X)减小 |
您最近一年使用:0次
2021-08-11更新
|
1495次组卷
|
23卷引用:宁夏回族自治区中宁县第一中学2022-2023学年高二上学期10月月考化学试题
宁夏回族自治区中宁县第一中学2022-2023学年高二上学期10月月考化学试题河北省沧州市普通高中高三上学期教学质量监测(联考)化学试题(已下线)黄金30题系列 高二化学(选修4) 小题好拿分【提升版】辽宁省丹东市凤城市第一中学2019-2020学年高二上学期12月月考化学试题2020届高三化学二轮冲刺新题专练——能量变化的图像分析(已下线)考点06 化学能与热能-2020年高考化学命题预测与模拟试题分类精编辽宁省实验中学2019-2020学年高一下学期期中考试化学试题河南省漯河市漯河实验高中2020-2021学年高二上学期期中考试化学试题广东省湛江市2020-2021学年高二下学期期末调研考试化学试题(已下线)课时28 焓变与热化学方程式-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)2.3.2 压强变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)综合复习与测试(2)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)广东省揭阳华侨高级中学2021-2022学年高二上学期期中考试化学试题陕西省榆林市子洲中学2021-2022学年高二上学期期中考试化学试题山东省潍坊实验中学2022-2023学年高二上学期第一次单元过关检测化学试题江苏省连云港市赣榆智贤中学2022-2023学年高二上学期第一次学情检测化学试题云南省昆明市寻甸县2022-2023学年高二上学期期中考试化学试题四川省自贡市田家柄中学教育集团2021-2022学年高二下学期入学考试化学试题河南省兰考县第二高级中学2021-2022学年高二上学期期中考试化学试题四川省合江县马街中学校2023-2024学年高二上学期1月期末化学试题
名校
6 . 将等物质的量的X、Y气体充入某密闭容器中,一定条件下,发生如下反应并达到平衡: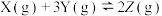
 ,改变某个条件并维持新条件直至达到新的平衡,表中关于新平衡与原平衡的比较正确的是
,改变某个条件并维持新条件直至达到新的平衡,表中关于新平衡与原平衡的比较正确的是
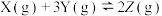
 ,改变某个条件并维持新条件直至达到新的平衡,表中关于新平衡与原平衡的比较正确的是
,改变某个条件并维持新条件直至达到新的平衡,表中关于新平衡与原平衡的比较正确的是| 选项 | 改变的条件 | 新平衡与原平衡比较 |
| A | 升高温度 | X的转化率变小 |
| B | 增大压强(压缩体积) | X的浓度变小 |
| C | 充入一定量Y | Y的转化率增大 |
| D | 使用适当催化剂 | X的体积分数变小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-08-01更新
|
882次组卷
|
23卷引用:宁夏海原第一中学2020-2021学年高二上学期第二次月考化学试题
宁夏海原第一中学2020-2021学年高二上学期第二次月考化学试题(已下线)2010年6月浙江金华四校高二期末测试化学试题(已下线)2014届黑龙江省牡丹江一中高二上学期期末考试化学试卷2014-2015黑龙江省桦南培黎学校高二上学期期末考试化学试卷2014-2015江西省奉新县第一中学高二上学期期末化学试卷2017届江西省九江一中高三上学期月考二化学试卷湖南省长沙市第一中学2017-2018学年高二上学期期中考试化学试题广东省惠州市2017-2018学年高二上学期期末教学质量检测(理)化学试题(已下线)2018年9月25日《每日一题》一轮复习-化学平衡的移动河南省洛阳市2018-2019学年高二第一学期期中考试化学试题广东省惠州市2018-2019学年高二上学期期末考试化学(理科)试题人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第二节 化学平衡 课时3 影响化学平衡的因素(已下线)专题10 化学平衡(速率、影响因素、图像、标志、平衡压强及常数)-2021年高考化学必做热点专题选择性必修1(SJ)专题2第三单元 化学平衡的移动(已下线)考向22 化学平衡状态 化学平衡的移动-备战2022年高考化学一轮复习考点微专题安徽省六安市第一中学2021-2022学年高二下学期开学考试化学试题湖南省长沙市宁乡市2020-2021学年高二下学期期末调研考试化学试题陕西省西安市雁塔区第二中学2021-2022学年高二上学期第一次月考化学试题福建省泉州市第六中学2021-2022学年高二上学期期中模块测试化学试题(已下线)第七章 化学反应速率与化学平衡 第43练 化学平衡移动原理及应用2.3.2温度 催化剂对化学平衡的影响 课中第3课时 温度、催化剂对化学平衡的影响广东省惠州市2023-2024学年高三上学期第三次调研化学试题
名校
7 . 以下是关于“外界因素对化学平衡影响的实验研究”的课题,请回答下列问题。
(1)研究的思路与方法。
①研究对象的选择,现有以下可逆反应:A. 2NO2(g) N2O4(g) ΔH<0 B. FeCl3+3KSCN
N2O4(g) ΔH<0 B. FeCl3+3KSCN Fe(SCN)3+3KCl
Fe(SCN)3+3KCl
其中,A适合于研究___ 对平衡的影响,B适合于研究___ 对平衡的影响。(填字母)
a. 浓度 b. 温度 c. 压强
②研究方法:采用控制其他因素不变,改变其中一个因素的方法,进行对比实验。
(2)单一因素对化学平衡影响的实验研究。
①浓度:将FeCl3与KSCN反应后所得的混合液分为四等份,分别加入FeCl3浓溶液、KSCN浓溶液和NaOH固体、KCl固体观察现象。
现象:加入FeCl3浓溶液后的混合溶液红色___ ;加入KSCN浓溶液后的混合溶液红色___ ;加入NaOH固体后,混合溶液红色___ ;加入KCl固体混合溶液红色___ 。
②温度:将密封并相互连通的盛有NO2的两个玻璃球,一个放入热水中,另一个放入冷水中。现象:放入热水中的球内红棕色___ ;放入冷水中的球内红棕色___ 。
(3)综合(2)中研究结果,请总结外界因素对化学平衡的影响规律__ 。
(1)研究的思路与方法。
①研究对象的选择,现有以下可逆反应:A. 2NO2(g)
 N2O4(g) ΔH<0 B. FeCl3+3KSCN
N2O4(g) ΔH<0 B. FeCl3+3KSCN Fe(SCN)3+3KCl
Fe(SCN)3+3KCl其中,A适合于研究
a. 浓度 b. 温度 c. 压强
②研究方法:采用控制其他因素不变,改变其中一个因素的方法,进行对比实验。
(2)单一因素对化学平衡影响的实验研究。
①浓度:将FeCl3与KSCN反应后所得的混合液分为四等份,分别加入FeCl3浓溶液、KSCN浓溶液和NaOH固体、KCl固体观察现象。
现象:加入FeCl3浓溶液后的混合溶液红色
②温度:将密封并相互连通的盛有NO2的两个玻璃球,一个放入热水中,另一个放入冷水中。现象:放入热水中的球内红棕色
(3)综合(2)中研究结果,请总结外界因素对化学平衡的影响规律
您最近一年使用:0次
名校
解题方法
8 . 恒温密闭容器中加入一定量的A,发生反应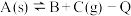 (
(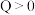 ),达到平衡。以下分析正确的是
),达到平衡。以下分析正确的是
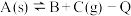 (
(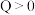 ),达到平衡。以下分析正确的是
),达到平衡。以下分析正确的是| A.加入少量B,平衡就会逆向移动 |
B.达到平衡的标志之一: |
C.若开始时向容器中加入1 A,达到平衡时吸收热量Q A,达到平衡时吸收热量Q |
D.缩小容器体积,重新达到平衡时, 的浓度与原平衡浓度相等 的浓度与原平衡浓度相等 |
您最近一年使用:0次
2021-03-23更新
|
373次组卷
|
4卷引用:宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题
宁夏回族自治区银川一中2022-2023学年高二上学期期中考试化学试题上海市普陀区2021届高三二模化学试题(已下线)第七章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测云南省腾冲市第八中学2022-2023学年高二下学期第三次月考化学试题
名校
9 . 将E(s)和F(g)加入密闭容器中,在一定条件下发生反应E(s)+4F(g) G(g),已知该反应的平衡常数如表所示。下列说法正确的是
G(g),已知该反应的平衡常数如表所示。下列说法正确的是
 G(g),已知该反应的平衡常数如表所示。下列说法正确的是
G(g),已知该反应的平衡常数如表所示。下列说法正确的是| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A.上述反应是熵增反应 |
B.25℃时,反应G(g) E(s)+4F(g)的平衡常数是0.5 E(s)+4F(g)的平衡常数是0.5 |
| C.在80℃时,测得某时刻F、G的浓度均为0.5mol·L-1,则此时v正>v逆 |
| D.恒温恒容下,向容器中再充入少量G(g),达到新平衡时,G的体积百分含量将增大 |
您最近一年使用:0次
2021-03-06更新
|
645次组卷
|
8卷引用:宁夏石嘴山市第三中学2020届高三上学期期中考试化学试题
名校
解题方法
10 . 下列选项中的原因或结论与现象不对应的是
| 选项 | 现象 | 原因或结论 |
| A | 在H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反应所需的活化能 |
| B | 向5mL0.005mol•L-1FeCl3溶液中加入5mL0.010mol•L-1KSCN溶液,溶液呈红色,再滴加几滴1mol•L-1KCl溶液,溶液颜色变浅 | 增大生成物浓度,平衡向逆反应方向移动 |
| C | 将盛有NO2气体的密闭容器浸泡在热水中,容器内气体颜色变深 | 2NO2(g) N2O4(g),△H<0,平衡向生成NO2方向移动 N2O4(g),△H<0,平衡向生成NO2方向移动 |
| D | 在密闭容器中有反应:A(?)+xB(g) 2C(g)。达到平衡时测得c(A)为0.5mol/L,将容器容积扩大到原来的三倍,测得c(A)为0.2mol/L 2C(g)。达到平衡时测得c(A)为0.5mol/L,将容器容积扩大到原来的三倍,测得c(A)为0.2mol/L | A气体,x>1 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-25更新
|
529次组卷
|
4卷引用:宁夏银川一中2020-2021学年高二上学期期末考试化学试题



