名校
解题方法
1 . 从某冶锌工厂的工业废料[除ZnO外,还含有铋(Bi)、锗(Ge)等的氧化物]中回收几种金属的单质或化合物的工业流程如图:
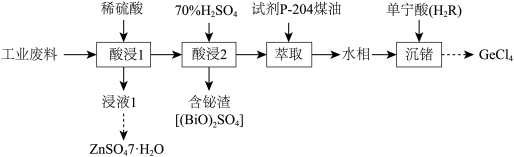
(已知:Ge4+易水解)
(1)下列措施更有利于完成“酸浸1”目的,提高“酸浸1”浸取率的是______ (填字母)。
(2)“酸浸2”时Bi2O3发生反应的离子方程式为______ 。
(3)“沉锗”的反应原理为Ge4++2H2R GeR2↓+4H+,该操作中需调节pH约为2.5,不能过高或过低,其原因是
GeR2↓+4H+,该操作中需调节pH约为2.5,不能过高或过低,其原因是______ 。
(4)①ZnO的一种晶胞结构如图1所示,每个Zn原子周围紧邻的O原子个数为______ 。
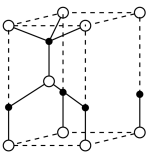
图1
②ZnO也可用作半导体材料,晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分百分数小于Zn-O键,从元素电负性的角度分析其原因为______ 。
③加热ZnSO4•7H2O固体,固体质量保留百分数与温度的关系如图2所示。1050℃时所得固体的化学式为______ 。(写出计算过程)
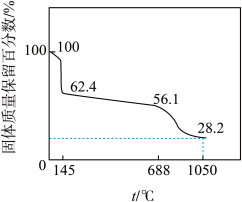
图2

(已知:Ge4+易水解)
(1)下列措施更有利于完成“酸浸1”目的,提高“酸浸1”浸取率的是
| A.延长酸浸时间 | B.浓硫酸代替稀硫酸 |
| C.酸浸过程中不断搅拌 | D.增多工业废料的用量 |
(2)“酸浸2”时Bi2O3发生反应的离子方程式为
(3)“沉锗”的反应原理为Ge4++2H2R
 GeR2↓+4H+,该操作中需调节pH约为2.5,不能过高或过低,其原因是
GeR2↓+4H+,该操作中需调节pH约为2.5,不能过高或过低,其原因是(4)①ZnO的一种晶胞结构如图1所示,每个Zn原子周围紧邻的O原子个数为

图1
②ZnO也可用作半导体材料,晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分百分数小于Zn-O键,从元素电负性的角度分析其原因为
③加热ZnSO4•7H2O固体,固体质量保留百分数与温度的关系如图2所示。1050℃时所得固体的化学式为

图2
您最近一年使用:0次
2 . 资料显示, 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。已知:
氧化的产物及铜元素的价态。已知: 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色); 和
和 氧化性几乎相同。
氧化性几乎相同。
将等体积的 溶液加入到n
溶液加入到n 铜粉和m
铜粉和m
 (
( )的固体混合物中,振荡。
)的固体混合物中,振荡。
实验记录如下:
(1)基态 的电子排布式
的电子排布式___________ 。
(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有 (蓝色)或
(蓝色)或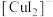 (无色),进行以下实验探究:
(无色),进行以下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入 ,多次萃取、分液。
,多次萃取、分液。
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
i.步骤a除去 的原理是
的原理是___________ 。
ii.查阅资料, (无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:
(无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:___________ ,___________ 。
(3)上述实验推测实验Ⅰ和Ⅱ中的白色沉淀可能是 ,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入
,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入 溶液,
溶液,___________ (填实验现象)。实验Ⅲ中铜被氧化的化学方程式是___________ 。
(4)上述实验结果, 仅将
仅将 氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了
氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了 能将
能将 氧化为
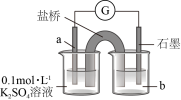
氧化为 。装置如图所示,a物质为
。装置如图所示,a物质为___________ ,b试剂为___________ 。
 可以将
可以将 氧化为
氧化为 。某小组同学设计实验探究
。某小组同学设计实验探究 被
被 氧化的产物及铜元素的价态。已知:
氧化的产物及铜元素的价态。已知: 易溶于
易溶于 溶液,发生反应
溶液,发生反应 (红棕色);
(红棕色); 和
和 氧化性几乎相同。
氧化性几乎相同。将等体积的
 溶液加入到n
溶液加入到n 铜粉和m
铜粉和m
 (
( )的固体混合物中,振荡。
)的固体混合物中,振荡。实验记录如下:
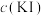 | 实验现象 | |
| 实验Ⅰ | 0.01 | 极少量 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为淡红色 |
| 实验Ⅱ | 0.1 | 部分 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液仍为红棕色 |
| 实验Ⅲ | 4 |  完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色 完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深红棕色 |
 的电子排布式
的电子排布式(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有
 (蓝色)或
(蓝色)或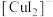 (无色),进行以下实验探究:
(无色),进行以下实验探究:步骤a.取实验Ⅲ的深红棕色溶液,加入
 ,多次萃取、分液。
,多次萃取、分液。步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
i.步骤a除去
 的原理是
的原理是ii.查阅资料,
 (无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:
(无色)容易被空气氧化,用两个离子方程式解释步骤b的溶液中发生的变化:(3)上述实验推测实验Ⅰ和Ⅱ中的白色沉淀可能是
 ,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入
,分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入 溶液,
溶液,(4)上述实验结果,
 仅将
仅将 氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了
氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了 能将
能将 氧化为
氧化为 。装置如图所示,a物质为
。装置如图所示,a物质为
您最近一年使用:0次
2023-11-03更新
|
273次组卷
|
2卷引用:湖北省鄂东南省级示范高中教育教学改革联盟学校2023-2024学年高三上学期期中联考化学试题
名校
解题方法
3 . 实验小组探究酸对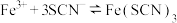 平衡的影响。将0.005 mol/L
平衡的影响。将0.005 mol/L  溶液和0.01 mol/L KSCN溶液等体积混合,得到红色溶液。取两等份红色溶液,进行如下操作并记录现象。
溶液和0.01 mol/L KSCN溶液等体积混合,得到红色溶液。取两等份红色溶液,进行如下操作并记录现象。
(1) 水解显酸性的原因是
水解显酸性的原因是___________ (用方程式表示)。
(2)甲同学认为加入酸后,会使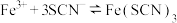 体系中
体系中___________ 浓度改变,导致该平衡正向移动,溶液颜色加深。
【设计并实施实验】
【查阅资料】
 和
和 、
、 均能发生络合反应:
均能发生络合反应:
 (黄色);
(黄色); (无色)。
(无色)。
实验I.探究现象a中溶液颜色变化的原因
(3)实验①的目的是___________ 。
(4)根据实验①和实验②的结果,从平衡移动角度解释现象a:___________ 。
实验Ⅱ.探究现象b中溶液呈浅黄色的原因
(5)结合实验③可推测现象b中使溶液呈浅黄色的微粒可能有三种,分别是 、
、___________ 。
(6)乙同学进一步补充了实验④,确证了现象b中使溶液呈浅黄色的微粒只是(5)中的一种,请将实验④的操作补充完整:___________ 。
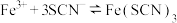 平衡的影响。将0.005 mol/L
平衡的影响。将0.005 mol/L  溶液和0.01 mol/L KSCN溶液等体积混合,得到红色溶液。取两等份红色溶液,进行如下操作并记录现象。
溶液和0.01 mol/L KSCN溶液等体积混合,得到红色溶液。取两等份红色溶液,进行如下操作并记录现象。(1)
 水解显酸性的原因是
水解显酸性的原因是(2)甲同学认为加入酸后,会使
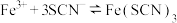 体系中
体系中【设计并实施实验】
 |  |
 和
和 、
、 均能发生络合反应:
均能发生络合反应: (黄色);
(黄色); (无色)。
(无色)。实验I.探究现象a中溶液颜色变化的原因
| 编号 | 操作 | 现象 |
| ① | 向2 mL红色溶液中滴加5滴水 | 溶液颜色无明显变化 |
| ② | 向2 mL红色溶液中滴加5滴3 mol/L KCl溶液 | 溶液颜色变浅,呈橙色 |
(4)根据实验①和实验②的结果,从平衡移动角度解释现象a:
实验Ⅱ.探究现象b中溶液呈浅黄色的原因
| 编号 | 操作 | 现象 |
| ③ | 取1 mL 0.0025 mol/L 溶液(无色),加入1 mL 0.01 mol/L KSCN溶液,再加入5滴1.5 mol/L 溶液(无色),加入1 mL 0.01 mol/L KSCN溶液,再加入5滴1.5 mol/L  溶液 溶液 | 溶液先变红,加硫酸后变为浅黄色 |
| ④ | 取1 mL 0.005mol/L  溶液, 溶液, | 溶液为无色 |
 、
、(6)乙同学进一步补充了实验④,确证了现象b中使溶液呈浅黄色的微粒只是(5)中的一种,请将实验④的操作补充完整:
您最近一年使用:0次
名校
4 . 25℃时,下列有关电解质溶液的说法正确的是
| A.氯水存在Cl2(g)+H2O(l)⇌HClO(aq)+H+(aq)+Cl-(aq),向平衡体系加水,c(Cl-)/c(HClO)不变 |
B.室温下向10mL0.1mo1•L-1的氨水中加水稀释后,溶液中 的值增大 的值增大 |
| C.等体积等浓度的盐酸、硫酸、醋酸三种溶液中,c(H+)相等 |
| D.向醋酸溶液中加入少量冰醋酸,醋酸电离平衡向右移动,电离程度增大 |
您最近一年使用:0次
2023-10-26更新
|
862次组卷
|
3卷引用:广东省广州市铁一中学2023-2024学年高二上学期10月月考化学试题
23-24高三上·上海浦东新·阶段练习
名校
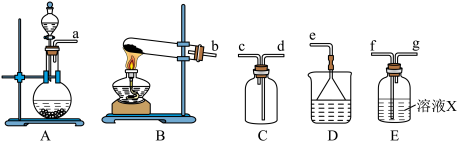
5 . 某研究性学习小组通过亚硫酸钠固体和浓硫酸反应制备SO2并进行性质探究。
Ⅰ.制备干燥的SO2
(1)制备SO2反应的方程式为___________ 。
(2)根据上述原理制备收集干燥SO2的实验装置连接顺序为___________ (填序号)。
(3)溶液X中盛放的试剂为___________ ,装置D的作用为___________ 。
Ⅱ.SO2性质的探究
研究性学校小组将纯净的SO2通100 mL溶液Y中,进行SO2性质的探究。
探究活动1:SO2的氧化性
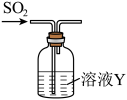
(4)Y是Na2S溶液,可观察到的现象___________ 。Na2S溶液的浓度为0.1 mol/L溶液最多可以吸收标况下的SO2体积为___________ mL(不考虑SO2的溶解)。
探究活动2:SO2的溶解性和酸性
(5)若Y为石蕊溶液,可观察到的现象为___________ ,用方程式表示产生该现象的原因___________ 。
(6)若Y为1 mol/L的NaOH溶液,通入2.24 L SO2(标准状况下),得到的溶液中: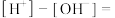
___________ (用溶液中的含硫微粒浓度表示)。
探究活动3:SO2与FeCl3溶液的反应
实验1中出现红棕色的原因,研究小组成员查阅资料得: 与
与 作用可以生成红棕色的配离子:
作用可以生成红棕色的配离子: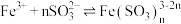 (红棕色)。
(红棕色)。
(7)实验2中,溶液由黄色变为浅绿色的离子方程式为___________ 。
(8)结合速率与平衡的知识,解释实验1颜色变化的原因___________ 。
(9)解释实验2的现象与实验1的现象不同的原因___________ 。

Ⅰ.制备干燥的SO2
(1)制备SO2反应的方程式为
(2)根据上述原理制备收集干燥SO2的实验装置连接顺序为
(3)溶液X中盛放的试剂为
Ⅱ.SO2性质的探究
研究性学校小组将纯净的SO2通100 mL溶液Y中,进行SO2性质的探究。
探究活动1:SO2的氧化性

(4)Y是Na2S溶液,可观察到的现象
探究活动2:SO2的溶解性和酸性
(5)若Y为石蕊溶液,可观察到的现象为
(6)若Y为1 mol/L的NaOH溶液,通入2.24 L SO2(标准状况下),得到的溶液中:
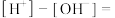
探究活动3:SO2与FeCl3溶液的反应
| 实验 | 溶液Y | 现象 |
| 1 | 1 mol/L FeCl3溶液 | 溶液由黄色变为红棕色,静置,溶液红棕色逐渐消失,1 h后变为浅绿色 |
| 2 | 1 mol/L FeCl3溶液和HCl混合溶液 | 溶液由黄色变为浅绿色 |
 与
与 作用可以生成红棕色的配离子:
作用可以生成红棕色的配离子: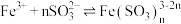 (红棕色)。
(红棕色)。(7)实验2中,溶液由黄色变为浅绿色的离子方程式为
(8)结合速率与平衡的知识,解释实验1颜色变化的原因
(9)解释实验2的现象与实验1的现象不同的原因
您最近一年使用:0次
名校
解题方法
6 . 钼系催化剂广泛用于石油炼制和化学工业生产中,通常利用加碱焙烧——水浸取法从废催化剂(主要成分为MoS、NiS、V2O5、Al2O3)中提取V2O3和 ,其工艺流程如图甲所示。
,其工艺流程如图甲所示。

已知:①MoO3、V2O5、Al2O3均可与纯碱反应生成对应的钠盐,而NiO不行。
②高温下,NH4VO3易分解。
③溶液的酸性较强时,+5价钒主要以 的形式存在。
的形式存在。
请回答下列问题:
(1)研磨的目的是_______ (答出一点即可)。
(2)X中生成的气体主要有_______ (填化学式)。
(3)沉钼过程中,发生的主要化学方程式为_______ 。
(4)沉钒过程中,一般要加入过量NH4Cl,其原因是_______ 。
(5)沉钒过程中,沉钒率随溶液pH的变化如图乙所示。沉钒率随溶液pH的增加先升高后降低的原因可能是_______ 。

(6)金属钼的晶胞如图丙所示,已知钼的密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 。则钼原子的配位数是
。则钼原子的配位数是_______ ,钼原子的半径_______ pm。

 ,其工艺流程如图甲所示。
,其工艺流程如图甲所示。
已知:①MoO3、V2O5、Al2O3均可与纯碱反应生成对应的钠盐,而NiO不行。
②高温下,NH4VO3易分解。
③溶液的酸性较强时,+5价钒主要以
 的形式存在。
的形式存在。请回答下列问题:
(1)研磨的目的是
(2)X中生成的气体主要有
(3)沉钼过程中,发生的主要化学方程式为
(4)沉钒过程中,一般要加入过量NH4Cl,其原因是
(5)沉钒过程中,沉钒率随溶液pH的变化如图乙所示。沉钒率随溶液pH的增加先升高后降低的原因可能是

(6)金属钼的晶胞如图丙所示,已知钼的密度为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 。则钼原子的配位数是
。则钼原子的配位数是
您最近一年使用:0次
名校
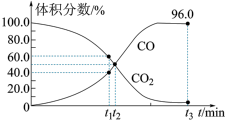
7 . 某固定容积的密闭容器中发生反应: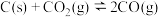 。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
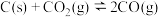 。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
。现向该容器内充入1.0 mol·L-1的CO2,此时压强为P0KPa,反应过程中气体体积分数随时间的变化情况如图所示。下列说法正确的是
A. 时,CO2的转化率为20.0% 时,CO2的转化率为20.0% |
B. 时,该反应体系处于平衡状态 时,该反应体系处于平衡状态 |
C. 时,向该容器中再充入CO2和CO各1.0 mol·L-1,平衡逆向移动 时,向该容器中再充入CO2和CO各1.0 mol·L-1,平衡逆向移动 |
D. 时,该反应的 时,该反应的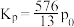 [气体分压(p分)=气体总压(p总)×体积分数] [气体分压(p分)=气体总压(p总)×体积分数] |
您最近一年使用:0次
解题方法
8 . 某小组同学探究盐对Fe3+ +3SCN- Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。
实验I:探究KCl对Fe3+和SCN-平衡体系的影响
将已用稀盐酸酸化的0.005 mol·L-1 FeCl3溶液和0.01 mol·L-1 KSCN溶液等体积混合,静置至体系平衡,得红色溶液X,分别取3 mL溶液X放入比色皿中,分别滴加0.1 mL的试剂①~④,并测定各溶液的透光率随时间的变化,结果如图所示。
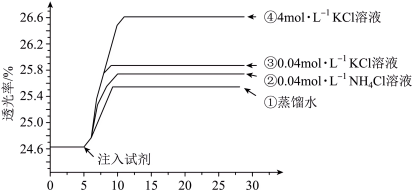
已知:i.Cl-与Fe3+能发生络合反应:Fe3+ +4C1- [FeCl4]-(黄色);
[FeCl4]-(黄色);
ii.Fe3+与NO 不能形成配位化合物;
不能形成配位化合物;
iii.溶液的透光率与溶液颜色深浅有关,颜色越深,透光率越低,忽略[FeCl4]-对透光率的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量筒、玻璃棒、容量瓶外,还需要___________ ,用稀盐酸酸化FeCl3溶液的目的是___________ 。
(2)注入试剂①后溶液透光率升高,甲同学认为是溶液稀释导致颜色变浅,乙同学认为还可能是稀释的过程中,Fe3+ +3SCN- Fe(SCN)3平衡向
Fe(SCN)3平衡向___________ (填“正”或“逆”)反应方向移动。
(3)注入试剂④后的溶液透光率比注入试剂①后高,结合平衡移动原理分析其原因___________ 。
(4)注入试剂③后的溶液透光率比注入试剂②后高,可能是___________ 导致的(答出一种影响因素即可,不需详细说明理由)。
实验II:探究不同盐对Fe3+和SCN-平衡体系的影响
取2 mL溶液X,分别加入下列试剂进行实验,一段时间后测得各溶液的透光率如下表。
(5)丙同学发现A3>A2>A1,查阅资料认为可能的原因:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。推断盐效应较强的金属阳离子为___________ (填离子符号),试分析该离子盐效应对Fe3+和SCN-平衡体系有影响的原因___________ 。
(6)拓展应用:盐效应对多种平衡体系有影响。
分析c(Na2SO4)在0~0.20 mol·L-1范围内,PbSO4溶解度发生变化的原因:___________ 。
(7)FeCl3用途十分广泛,请写出一种其在生活中的用途___________ 。
 Fe(SCN)3平衡体系的影响。
Fe(SCN)3平衡体系的影响。实验I:探究KCl对Fe3+和SCN-平衡体系的影响
将已用稀盐酸酸化的0.005 mol·L-1 FeCl3溶液和0.01 mol·L-1 KSCN溶液等体积混合,静置至体系平衡,得红色溶液X,分别取3 mL溶液X放入比色皿中,分别滴加0.1 mL的试剂①~④,并测定各溶液的透光率随时间的变化,结果如图所示。

已知:i.Cl-与Fe3+能发生络合反应:Fe3+ +4C1-
 [FeCl4]-(黄色);
[FeCl4]-(黄色);ii.Fe3+与NO
 不能形成配位化合物;
不能形成配位化合物;iii.溶液的透光率与溶液颜色深浅有关,颜色越深,透光率越低,忽略[FeCl4]-对透光率的影响。
(1)本实验配制溶液时用到的玻璃仪器除烧杯、量筒、玻璃棒、容量瓶外,还需要
(2)注入试剂①后溶液透光率升高,甲同学认为是溶液稀释导致颜色变浅,乙同学认为还可能是稀释的过程中,Fe3+ +3SCN-
 Fe(SCN)3平衡向
Fe(SCN)3平衡向(3)注入试剂④后的溶液透光率比注入试剂①后高,结合平衡移动原理分析其原因
(4)注入试剂③后的溶液透光率比注入试剂②后高,可能是
实验II:探究不同盐对Fe3+和SCN-平衡体系的影响
取2 mL溶液X,分别加入下列试剂进行实验,一段时间后测得各溶液的透光率如下表。
| 序号 | 加入试剂 | 溶液透光率 |
| 1 | 1 mL蒸馏水 | A1 |
| 2 | 1 mL 3 mol·L-1 KNO3 | A2 |
| 3 | 1 mL 3 mol·L-1 NaNO3 | A3 |
(5)丙同学发现A3>A2>A1,查阅资料认为可能的原因:溶液中的离子会受到周围带有异性电荷离子的屏蔽,使该离子的有效浓度降低,这种影响称为盐效应。推断盐效应较强的金属阳离子为
(6)拓展应用:盐效应对多种平衡体系有影响。
| c(Na2SO4)/(mol·L-1) | 0 | 0.01 | 0.02 | 0.04 | 0.10 | 0.20 |
| PbSO4溶解度/mg | 4.5 | 0.48 | 0.42 | 0.39 | 0.48 | 0.69 |
(7)FeCl3用途十分广泛,请写出一种其在生活中的用途
您最近一年使用:0次
名校
9 . 合成氨反应:N2+3H2 2NH3在密闭容器中进行。下列有关说法正确的是
2NH3在密闭容器中进行。下列有关说法正确的是
 2NH3在密闭容器中进行。下列有关说法正确的是
2NH3在密闭容器中进行。下列有关说法正确的是| A.其他条件相同时在不同容器中发生反应,使用催化剂可能使相同时间内H2的转化率更高 |
| B.若在恒温恒容条件下达到平衡后增大氨气浓度,平衡将逆向移动,氨气产率下降 |
| C.其他条件不变,升高温度,平衡逆向移动,正反应速率下降 |
| D.其他条件不变,降低NH3的浓度,平衡正向移动,正反应速率增大 |
您最近一年使用:0次
名校
10 . 已知: 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色, 为无色。现将
为无色。现将 溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: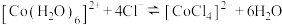 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:

以下结论和解释正确的是
 呈粉红色,
呈粉红色, 呈蓝色,
呈蓝色, 为无色。现将
为无色。现将 溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:
溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: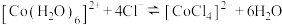 ,用该溶液做实验,溶液的颜色变化如下:
,用该溶液做实验,溶液的颜色变化如下:
以下结论和解释正确的是
| A.由实验①可推知正反应为放热反应 |
B.等物质的量的 和 和 中 中 键数目之比为3∶2 键数目之比为3∶2 |
C.实验②是由于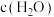 增大,导致平衡逆向移动 增大,导致平衡逆向移动 |
D.由实验③可知配离子的稳定性: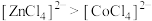 |
您最近一年使用:0次



