名校
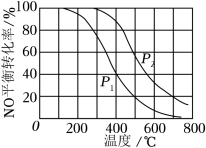
1 . 一定条件下,将NO(g)和O2(g)按物质的量之比2:1充入反应容器,发生反应:2NO(g)+O2(g) 2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如图所示。下列说法正确的是
2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如图所示。下列说法正确的是
 2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如图所示。下列说法正确的是
2NO2(g)。其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线如图所示。下列说法正确的是
| A.p1>p2 |
| B.其他条件不变,温度升高,该反应的反应限度减小 |
| C.400℃、p1条件下,O2的平衡转化率为20% |
D.400℃时,该反应的化学平衡常数的数值为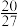 |
您最近半年使用:0次
2024-03-13更新
|
50次组卷
|
2卷引用:湖南省岳阳市岳阳县第一中学2023-2024学年高二下学期开学化学试题
名校
2 .  催化氧化
催化氧化 制取
制取 的新路径,其反应为:
的新路径,其反应为:
反应Ⅰ: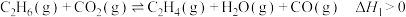
反应Ⅱ:
一定条件下,向容积为 的容器中通入
的容器中通入 和
和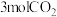 ,若仅考虑上述反应,
,若仅考虑上述反应, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度、压强变化的关系如图所示,
的选择性随温度、压强变化的关系如图所示, 、
、 代表不同压强下乙烷的平衡转化率。
代表不同压强下乙烷的平衡转化率。
已知: 的选择性
的选择性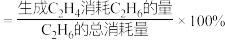
 催化氧化
催化氧化 制取
制取 的新路径,其反应为:
的新路径,其反应为:反应Ⅰ:
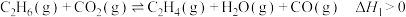
反应Ⅱ:

一定条件下,向容积为
 的容器中通入
的容器中通入 和
和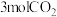 ,若仅考虑上述反应,
,若仅考虑上述反应, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度、压强变化的关系如图所示,
的选择性随温度、压强变化的关系如图所示, 、
、 代表不同压强下乙烷的平衡转化率。
代表不同压强下乙烷的平衡转化率。已知:
 的选择性
的选择性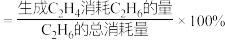

A.压强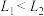 |
B.一定温度下,增大 会降低 会降低 的平衡转化率 的平衡转化率 |
C.压强为 、温度为T时,反应达平衡时,混合气体中 、温度为T时,反应达平衡时,混合气体中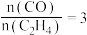 |
D.反应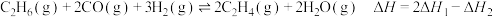 |
您最近半年使用:0次
名校
3 . 当今世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。其中用 、
、 为原料合成甲醇(
为原料合成甲醇( )过程主要涉及以下反应:
)过程主要涉及以下反应:
反应Ⅰ:

反应Ⅱ:

反应Ⅲ:
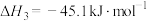
(1)根据盖斯定律,反应Ⅰ的
_______ 。
(2)我国学者结合实验与计算机模拟结果,研究了 与
与 在
在 /Cu催化剂表面生成
/Cu催化剂表面生成 和
和 的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。
的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。
_______ eV。并写出该历程的化学方程式_______ 。
(3)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______(填字母)。
(4)加压,甲醇产率将_______ (填“升高”“不变”“降低”或“无法确定”);若原料二氧化碳中掺混一氧化碳,随一氧化碳含量的增加,甲醇产率将_______ (填“升高”“不变”“降低”或“无法确定”)。
(5)加入新催化剂使1mol 和3mol
和3mol  在1L密闭容器中只发生反应Ⅰ、Ⅱ,
在1L密闭容器中只发生反应Ⅰ、Ⅱ, 平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的
平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的 物质的量分数)与温度的变化趋势如图所示。
物质的量分数)与温度的变化趋势如图所示。_______ (填“473K”“513K”或“553K”)。
②553K时,若反应后体系的总压为p,反应Ⅰ的
_______ (列出计算式)。( 为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
 、
、 为原料合成甲醇(
为原料合成甲醇( )过程主要涉及以下反应:
)过程主要涉及以下反应:反应Ⅰ:


反应Ⅱ:


反应Ⅲ:

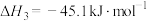
(1)根据盖斯定律,反应Ⅰ的

(2)我国学者结合实验与计算机模拟结果,研究了
 与
与 在
在 /Cu催化剂表面生成
/Cu催化剂表面生成 和
和 的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。
的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。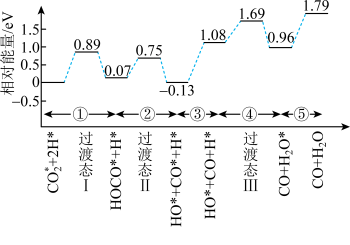

(3)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______(填字母)。
| A.升高温度,反应Ⅱ正向移动,反应Ⅲ逆向移动 |
| B.加入反应Ⅰ的催化剂,可以降低反应的活化能及反应热 |
C.增大 的浓度,有利于提高 的浓度,有利于提高 的平衡转化率 的平衡转化率 |
D.及时分离出 ,可以使得反应Ⅰ的正反应速率增大 ,可以使得反应Ⅰ的正反应速率增大 |
(4)加压,甲醇产率将
(5)加入新催化剂使1mol
 和3mol
和3mol  在1L密闭容器中只发生反应Ⅰ、Ⅱ,
在1L密闭容器中只发生反应Ⅰ、Ⅱ, 平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的
平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的 物质的量分数)与温度的变化趋势如图所示。
物质的量分数)与温度的变化趋势如图所示。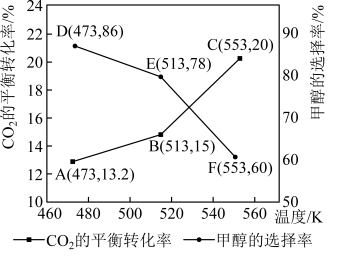
②553K时,若反应后体系的总压为p,反应Ⅰ的

 为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
您最近半年使用:0次
2023-09-30更新
|
254次组卷
|
5卷引用:湖南省平江县颐华高级中学2023-2024学年高三下学期入学考试化学试题
名校
解题方法
4 . 在催化剂作用下, 氧化
氧化 可获得
可获得 。其主要化学反应如下:
。其主要化学反应如下:
反应Ⅰ.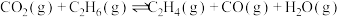

反应Ⅱ.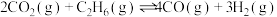

压强分别为 、
、 时,将
时,将
 和
和
 的混合气体置于密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性[
的混合气体置于密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性[ ]如图所示。下列说法正确的是
]如图所示。下列说法正确的是
 氧化
氧化 可获得
可获得 。其主要化学反应如下:
。其主要化学反应如下:反应Ⅰ.
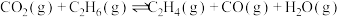

反应Ⅱ.
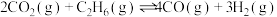

压强分别为
 、
、 时,将
时,将
 和
和
 的混合气体置于密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性[
的混合气体置于密闭容器中反应,不同温度下体系中乙烷的平衡转化率、乙烯的选择性[ ]如图所示。下列说法正确的是
]如图所示。下列说法正确的是
A. |
B.压强为 、温度为210℃时,反应达平衡时, 、温度为210℃时,反应达平衡时, |
C. 的选择性下降的原因可能是随着温度的升高,反应Ⅱ中生成的 的选择性下降的原因可能是随着温度的升高,反应Ⅱ中生成的 抑制了反应Ⅰ的进行 抑制了反应Ⅰ的进行 |
D.研发低温下 转化率高和 转化率高和 选择性高的催化剂,可以提高平衡时 选择性高的催化剂,可以提高平衡时 产率 产率 |
您最近半年使用:0次
2023-09-22更新
|
198次组卷
|
11卷引用:湖南省平江县颐华高级中学2023-2024学年高三下学期入学考试化学试题
湖南省平江县颐华高级中学2023-2024学年高三下学期入学考试化学试题江苏省无锡市2022-2023学年高三上学期期末调研测试化学试题(已下线)素养卷04 化学反应速率与平衡图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)选择题11-13江苏省常州市联盟学校2022-2023学年高二下学期期中学情调研化学试题湖南省长沙市雅礼中学2024届高三上学期月考试卷(一)化学试题湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题湖南省常德市第一中学2023-2024学年高三上学期第六次月考化学试题江苏省南京市第九中学2023-2024学年高二上学期期末化学试卷江苏省南京市六校联合体2023-2024学年高二下学期四月联考化学试卷江苏省盐城市三校联考2023-2024学年高二下学期4月期中考试化学试题
名校
解题方法
5 . 已知:反应反应2NH3(g) N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是
N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是

 N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是
N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是
A.若保持容器体积不变,0~t1min内,N2的平均反应速率为 mol•L﹣1•min﹣1 mol•L﹣1•min﹣1 |
| B.若保持容器体积不变,该温度下,当N2和H2的分压比保持不变时,表明反应已达平衡 |
| C.若保持容器体积不变,t1min时,反应放出0.2akJ的热量 |
| D.t2min时,将容器体积迅速缩小一半并保持不变,N2的分压变化如图中曲线b所示 |
您最近半年使用:0次
名校
6 . 利用CO生产甲醇的反应为2H2(g)+CO(g)=CH3OH(g),在密闭容器中按物质的量之比为2:1充入H2和CO,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图所示。下列相关说法错误的是
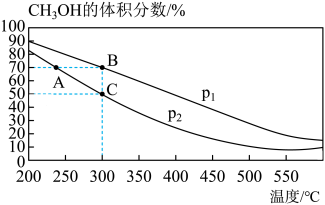

| A.该反应的△H<0,且P1>P2 |
| B.B点与C点的平衡常数关系为KB=KC |
C.C点对应的平衡常数Kp= |
| D.在恒温恒压条件下,平衡后再向容器中加入1molCH3OH(g),再达平衡时CH3OH(g)的转化率降低 |
您最近半年使用:0次
2022-12-08更新
|
433次组卷
|
5卷引用:湖南省岳阳县第一中学2022-2023学年高二下学期开学考试化学试题
名校
7 .  经催化加氢可合成乙烯:
经催化加氢可合成乙烯: 。0.1MPa时,按
。0.1MPa时,按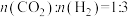 投料,测得不同温度下平衡时体系中各物质浓度的关系如图所示,下列叙述不正确的是
投料,测得不同温度下平衡时体系中各物质浓度的关系如图所示,下列叙述不正确的是

 经催化加氢可合成乙烯:
经催化加氢可合成乙烯: 。0.1MPa时,按
。0.1MPa时,按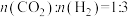 投料,测得不同温度下平衡时体系中各物质浓度的关系如图所示,下列叙述不正确的是
投料,测得不同温度下平衡时体系中各物质浓度的关系如图所示,下列叙述不正确的是
A.该反应的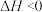 |
B.曲线b代表 的浓度变化 的浓度变化 |
C.N点和M点所处状态下的 一样 一样 |
D.其他条件不变, 、0.2MPa下反应达平衡时 、0.2MPa下反应达平衡时 比M点的小 比M点的小 |
您最近半年使用:0次
2022-10-29更新
|
136次组卷
|
18卷引用:湖南省岳阳市岳阳县第一中学2021-2022学年高二下学期期末考试试题
湖南省岳阳市岳阳县第一中学2021-2022学年高二下学期期末考试试题湖南省岳阳市岳阳县第一中学2021-2022学年高二下学期期末考试试题江西省师范大学附属中学2017届高三第三次模拟考试理综化学试题北京市一零一中学2018届高三10月月考化学试题2020届高三化学选修4二轮专题练——化学平衡移动的图像分析 【精编25题】辽宁省锦州市联合校2020届高三上学期期末考试化学试题(已下线)考点10 化学平衡常数及其图象分析-2020年高考化学命题预测与模拟试题分类精编天津市大港油田实验中学2020届高三开学考试化学试题(已下线)第二章 化学反应速率与化学平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)山西省运城市景胜中学2020-2021学年高二10月月考化学试题重庆市合川实验中学2020-2021学年高二上学期期中考试化学试题(已下线)专题讲座(五)反应速率、平衡图像题解题策略(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)天津市西青区杨柳青第一中学2022-2023学年高三上学期第一次适应性测试化学试题四川省自贡市田家柄中学教育集团2021-2022学年高二下学期入学考试化学试题(已下线)第2讲 化学平衡状态及化学平衡的移动福建省泉州市永春第一中学2023-2024学年高二上学期11月期中考试化学(选择性考试)试题江西省宜春市宜丰中学2023-2024学年高三上学期12月月考化学试题
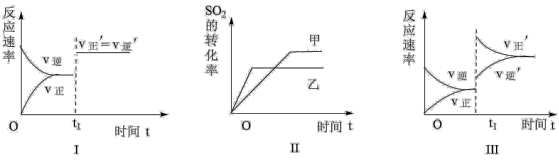
8 . 在容积不变的密闭容器中存在如下反应2SO2(g)+O2(g) 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
| A.图I表示的是t1时刻加入催化剂后对反应速率的影响 |
| B.图II表示的是压强对化学平衡的影响,且乙的压强较高 |
| C.图II表示的是温度对化学平衡的影响,且乙的温度较高 |
| D.图III表示的是t1时刻增大O2的浓度对反应速率的影响 |
您最近半年使用:0次
2022-10-25更新
|
140次组卷
|
4卷引用:湖南省岳阳市华容县2021-2022学年高二上学期期末教学质量监测化学试题
9 . 对于平衡体系mA(g)+nB(g) pC(g)+qD(g) △H<0。下列结论正确的是
pC(g)+qD(g) △H<0。下列结论正确的是
 pC(g)+qD(g) △H<0。下列结论正确的是
pC(g)+qD(g) △H<0。下列结论正确的是| A.若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n>p+q |
| B.若m+n=p+q,则向含有amol气体的平衡体系中再加入amol的B,达到新平衡时气体的总物质的量等于2amol |
| C.若平衡时,A.B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n |
| D.温度升高时,K值增大 |
您最近半年使用:0次
10 . 在某一温度下,某一密闭容器中,M、N、R三种气体浓度的变化如图a所示,若其它条件不变,当温度分别为T1和T2时,N的体积分数与时间关系如图b所示。则下列结论正确的是
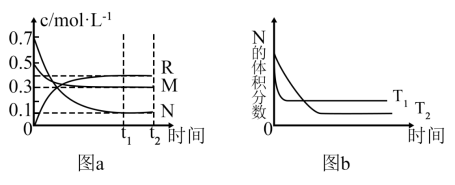

A.该反应的热化学方程式M(g)+3N(g) 2R(g) △H<0 2R(g) △H<0 |
| B.达到平衡后,若其他条件不变,减小容器体积,平衡向逆反应方向移动 |
| C.达到平衡后,若其它条件不变,升高温度,正、逆反应速度均增大,M的转化率增大 |
| D.达到平衡后,若其他条件不变,通入稀有气体,平衡一定向正反应方向移动 |
您最近半年使用:0次



