名校
1 . 课本里介绍的合成氨技术叫哈伯法,是德国诺贝尔化学奖获得者哈伯发明的。其合成原理为:N2(g) + 3H2(g)  2NH3(g) ΔH < 0,ΔS < 0 。
2NH3(g) ΔH < 0,ΔS < 0 。
(1)下列关于工业合成氨的说法正确的是________。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中 T 表示温度,n 表示H2物质的量)。
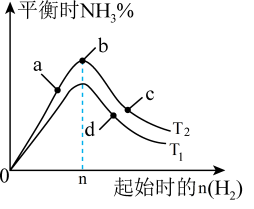
①图象中T2和T1的关系是:T2______ T1(填“>,<或=”,下同)
②a、 b、 c、 d 四点所处的平衡状态中,反应物N2的转化率最高的是______ (填字母)。
(3)恒温下, 往一个 4L 的密闭容器中充入5.2mol H2和 2mol N2,反应过程中对 NH3的浓度进行检测,得到的数据如下表所示:
①此条件下该反应的一定处于平衡状态的时间段是_______ 。
②若维持容器体积不变,温度不变,往原平衡体系中加入H2、N2和 NH3各 4mol,化学平衡将向_____ 反应方向移动(填“正”或“逆”)。请通过计算说明该方向的判断理由___________ 。
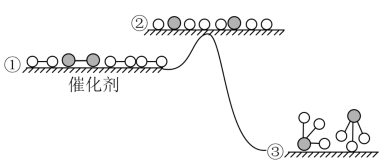
(4)工业合成氨反应在催化剂表面的反应历程及能量变化如图所示,下列说法正确的是_______。
 2NH3(g) ΔH < 0,ΔS < 0 。
2NH3(g) ΔH < 0,ΔS < 0 。(1)下列关于工业合成氨的说法正确的是________。
| A.因 为ΔH< 0,所以该反应一定能自发进行 |
| B.因为ΔS < 0,所以该反应一定不能自发进行 |
| C.在高温下进行是为了提高反应物的转化率 |
| D.使用催化剂加快反应速率是因为催化剂降低了反应的活化能 |
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中 T 表示温度,n 表示H2物质的量)。

①图象中T2和T1的关系是:T2
②a、 b、 c、 d 四点所处的平衡状态中,反应物N2的转化率最高的是
(3)恒温下, 往一个 4L 的密闭容器中充入5.2mol H2和 2mol N2,反应过程中对 NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L−1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
②若维持容器体积不变,温度不变,往原平衡体系中加入H2、N2和 NH3各 4mol,化学平衡将向
(4)工业合成氨反应在催化剂表面的反应历程及能量变化如图所示,下列说法正确的是_______。

| A.增大压强,① → ②之间的能量差值会增大 |
| B.合成氨的正、逆反应的焓变相同 |
| C.合成氨的过程是吸热过程 |
| D.若使用催化剂,生成等量的 NH3需要的时间更短 |
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题。
I.已知2C3H6(g)+2NH3(g)+3O2(g) 2C3H3N(g)+6H2O(g)
2C3H3N(g)+6H2O(g)  =-1030kJ/mol。
=-1030kJ/mol。
(1)上述为丙烯(C3H6)合成丙烯腈(C3H3N)的反应,则该反应___________。
(2)该反应
___________ 0(填>、<或=)。
(3)恒容时该反应生成丙烯腈的速率与时间的关系如图。
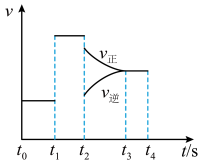
t1改变的条件为___________ ,t2改变的条件为___________ ;反应速率最大的时间段为___________ ,丙烯(C3H6)转化率最大的时间段为___________ 。
II.向1L密闭容器投入2molC3H6、2molNH3和3molO2反应5min,α(丙烯)与T的关系如图。
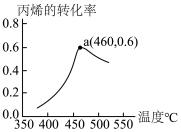
(4)460℃时平衡常数=___________ ,用O2表示反应速率v(O2)=___________ 。
(5)当温度低于460℃时,丙烯的转化率___________ (“是”或“不是”)所对应温度下的平衡转化率,理由是___________ 。
I.已知2C3H6(g)+2NH3(g)+3O2(g)
 2C3H3N(g)+6H2O(g)
2C3H3N(g)+6H2O(g)  =-1030kJ/mol。
=-1030kJ/mol。(1)上述为丙烯(C3H6)合成丙烯腈(C3H3N)的反应,则该反应___________。
| A.较高温度下自发进行 | B.较低温度下自发进行 |
| C.任何温度下都可自发进行 | D.任何温度下都不能自发进行 |
(2)该反应

(3)恒容时该反应生成丙烯腈的速率与时间的关系如图。

t1改变的条件为
II.向1L密闭容器投入2molC3H6、2molNH3和3molO2反应5min,α(丙烯)与T的关系如图。

(4)460℃时平衡常数=
(5)当温度低于460℃时,丙烯的转化率
您最近一年使用:0次
名校
3 . 科学家对汽车尾气进行无害化处理反应为: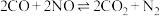 。一定条件下,在
。一定条件下,在 密闭容器中充入
密闭容器中充入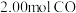 和
和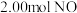 ,一段时间后测得
,一段时间后测得 、
、 浓度随时间变化如图1所示,
浓度随时间变化如图1所示, 的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比
的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比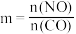 ,完成问题:
,完成问题:
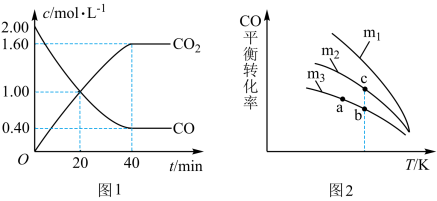
(1)该反应的化学平衡常数表达式是___________ 。根据图1,用 表示该反应达平衡过程中的平均反应速率是
表示该反应达平衡过程中的平均反应速率是___________  。
。
(2)已知:反应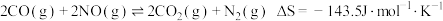 ,每生成14克
,每生成14克 时放出
时放出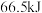 热量试写出上述反应的热化学方程式:
热量试写出上述反应的热化学方程式:___________ 。该反应在___________ 填入选项符号(A.高于、B.低于)___________  (填写温度数值)时,反应可以自发进行。
(填写温度数值)时,反应可以自发进行。
(3)图2中a、b、c三点对应的平衡常数 、
、 、
、 相对大小关系是
相对大小关系是___________ 。
(4)写出一条结论,可表明该反应已经达到平衡状态___________ 。
(5)下列关于该可逆反应的说法不正确的是___________。
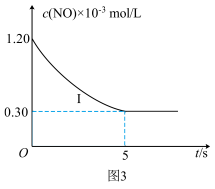
(6)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了验证倠化剂比表面积对反应速率的影响规律,在温度为 时,某同学设计了以下实验:
时,某同学设计了以下实验:
在图3中画出表中实验II条件下混合气体中 的浓度随时间变化的曲线
的浓度随时间变化的曲线___________ 。
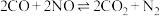 。一定条件下,在
。一定条件下,在 密闭容器中充入
密闭容器中充入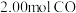 和
和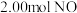 ,一段时间后测得
,一段时间后测得 、
、 浓度随时间变化如图1所示,
浓度随时间变化如图1所示, 的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比
的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比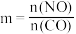 ,完成问题:
,完成问题:
(1)该反应的化学平衡常数表达式是
 表示该反应达平衡过程中的平均反应速率是
表示该反应达平衡过程中的平均反应速率是 。
。(2)已知:反应
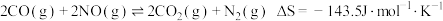 ,每生成14克
,每生成14克 时放出
时放出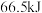 热量试写出上述反应的热化学方程式:
热量试写出上述反应的热化学方程式: (填写温度数值)时,反应可以自发进行。
(填写温度数值)时,反应可以自发进行。(3)图2中a、b、c三点对应的平衡常数
 、
、 、
、 相对大小关系是
相对大小关系是(4)写出一条结论,可表明该反应已经达到平衡状态
(5)下列关于该可逆反应的说法不正确的是___________。
A.其他条件不变,若充入 ,达到新平衡时, ,达到新平衡时, 、 、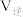 均增大 均增大 |
B.加入催化剂可提高 的平衡转化率 的平衡转化率 |
| C.若适当增大压强,则平衡正向移动 |
D.其他条件不变,若容器体积扩大一倍,达到新平衡时,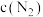 小于原来的一半 小于原来的一半 |
(6)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了验证倠化剂比表面积对反应速率的影响规律,在温度为
 时,某同学设计了以下实验:
时,某同学设计了以下实验:| 编号 | 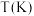 |  的初始浓度 的初始浓度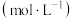 |  的初始浓度 的初始浓度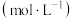 | 催化剂的比表面积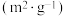 |
 |  |  | 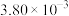 | 75 |
 |  |  | 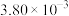 | 50 |
 的浓度随时间变化的曲线
的浓度随时间变化的曲线
您最近一年使用:0次
名校
解题方法
4 . Ⅰ.工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,反应为N2 (g)+3H2(g) 2NH3(g) △H =−92.4kJ·mol−1, △S=−200J·mol−1·K−1。请回答下列问题:
2NH3(g) △H =−92.4kJ·mol−1, △S=−200J·mol−1·K−1。请回答下列问题:
(1)常温下,合成氨反应________ (填“能”或“不能”)自发进行,其平衡常数表达式K=_______ 。
(2)______ 温(填“高”或“低”)有利于提高反应速率,______ 温(填“高”或“低”)有利于提高平衡转化率,综合考虑催化剂活性等因素,工业常采用400~500℃。
(3)针对反应速率与平衡产率的矛盾,我国科学家提出了解决方案:双温—双控—双催化剂。使用Fe-TiO2∙xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为 547℃,而TiO2∙xHy的温度为415℃)。

该方案的优势:___________ 。
Ⅱ.合成氨工艺可以进一步优化,实现尿素的合成,简易流程图如下:
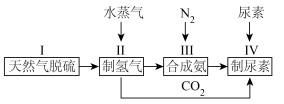
(4)步骤Ⅱ中制氢气原理如下:CH4(g)+H2O(g) CO(g)+3H2(g) ,CO(g)+H2O(g)
CO(g)+3H2(g) ,CO(g)+H2O(g) CO2(g)+H2(g),恒容容器中,对于以上反应,能加快反应速率的是___________。
CO2(g)+H2(g),恒容容器中,对于以上反应,能加快反应速率的是___________。
(5)已知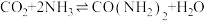 ,若合成尿素的流程中转化率为 80%时,100吨甲烷为原料能够合成
,若合成尿素的流程中转化率为 80%时,100吨甲烷为原料能够合成___________ 吨尿素。
Ⅲ.盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与 NH4Cl类似。
(6)写出盐酸肼第一步水解反应的离子方程式___________ 。
(7)盐酸肼水溶液中离子浓度的排列顺序正确的是___________。
 2NH3(g) △H =−92.4kJ·mol−1, △S=−200J·mol−1·K−1。请回答下列问题:
2NH3(g) △H =−92.4kJ·mol−1, △S=−200J·mol−1·K−1。请回答下列问题:(1)常温下,合成氨反应
(2)
(3)针对反应速率与平衡产率的矛盾,我国科学家提出了解决方案:双温—双控—双催化剂。使用Fe-TiO2∙xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为 547℃,而TiO2∙xHy的温度为415℃)。

该方案的优势:
Ⅱ.合成氨工艺可以进一步优化,实现尿素的合成,简易流程图如下:

(4)步骤Ⅱ中制氢气原理如下:CH4(g)+H2O(g)
 CO(g)+3H2(g) ,CO(g)+H2O(g)
CO(g)+3H2(g) ,CO(g)+H2O(g) CO2(g)+H2(g),恒容容器中,对于以上反应,能加快反应速率的是___________。
CO2(g)+H2(g),恒容容器中,对于以上反应,能加快反应速率的是___________。| A.升高温度 | B.充入 He | C.加入催化剂 | D.降低压强 |
(5)已知
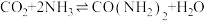 ,若合成尿素的流程中转化率为 80%时,100吨甲烷为原料能够合成
,若合成尿素的流程中转化率为 80%时,100吨甲烷为原料能够合成Ⅲ.盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与 NH4Cl类似。
(6)写出盐酸肼第一步水解反应的离子方程式
(7)盐酸肼水溶液中离子浓度的排列顺序正确的是___________。
A.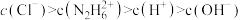 |
B.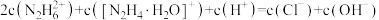 |
C.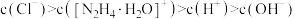 |
D.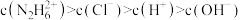 |
您最近一年使用:0次
名校
5 . 以煤炭为原料,通入一定比例空气和水蒸气,经过系列反应可得满足不同需求的原料气。
Ⅰ.在C和 的反应体系中:
的反应体系中:
反应1:

反应2:
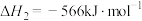
反应3:

(1)反应3对应的
___________ kJ/mol;
___________ 0(填“>、=或<”)。
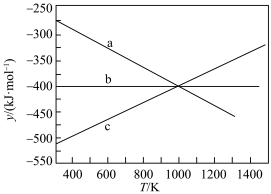
(2)设 ,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是
,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是___________ 。(填“a、b或c”)。
(3)一定压强下,随着温度升高,气体中CO与 的物质的量之比___________。
的物质的量之比___________。
(4)水煤气反应:
 。工业生产水煤气时,通常交替通入合适量的空气和水蒸气与煤炭反应,其理由是
。工业生产水煤气时,通常交替通入合适量的空气和水蒸气与煤炭反应,其理由是___________ 。
(5)已知 ,
, ,
, ,则水的沸点是
,则水的沸点是___________ K(结果保留一位小数,写出计算过程)。
Ⅱ.合成氨工业原料氢气用水、煤、天然气等为原料制得。反应如下: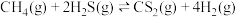

(6)在恒温恒容条件下,可作为反应达到平衡状态的判断依据是___________。
(7)在恒压条件下,以 的组成的混合气体发生反应,达到平衡状态时,四种组分物质的量分数随温度的变化如图所示。图中表示
的组成的混合气体发生反应,达到平衡状态时,四种组分物质的量分数随温度的变化如图所示。图中表示 、
、 变化的曲线分别是
变化的曲线分别是___________ 、___________ 。
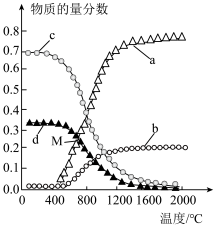
(8)M点对应温度下, 的转化率是
的转化率是___________ 。
(9)某温度下上述反应达到平衡后,保持其它条件不变,升高温度对反应速率影响的图像是___________(填编号)
(10)二氧化碳加氢制甲醇的总反应可表示为: ,该反应一般认为通过如下步骤实现:
,该反应一般认为通过如下步骤实现:
①

②

若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________(填编号)
Ⅰ.在C和
 的反应体系中:
的反应体系中:反应1:


反应2:

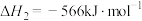
反应3:


(1)反应3对应的


(2)设
 ,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是
,反应1、2和3的y随温度的变化关系如图所示。图中对应于反应3的线条是
(3)一定压强下,随着温度升高,气体中CO与
 的物质的量之比___________。
的物质的量之比___________。| A.不变 | B.增大 | C.减小 | D.无法判断 |
(4)水煤气反应:

 。工业生产水煤气时,通常交替通入合适量的空气和水蒸气与煤炭反应,其理由是
。工业生产水煤气时,通常交替通入合适量的空气和水蒸气与煤炭反应,其理由是(5)已知
 ,
, ,
, ,则水的沸点是
,则水的沸点是Ⅱ.合成氨工业原料氢气用水、煤、天然气等为原料制得。反应如下:
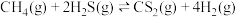

(6)在恒温恒容条件下,可作为反应达到平衡状态的判断依据是___________。
| A.混合气体密度不变 | B. 与 与 的物质的量之比为保持不变 的物质的量之比为保持不变 |
C. | D.容器内压强不变 |
(7)在恒压条件下,以
 的组成的混合气体发生反应,达到平衡状态时,四种组分物质的量分数随温度的变化如图所示。图中表示
的组成的混合气体发生反应,达到平衡状态时,四种组分物质的量分数随温度的变化如图所示。图中表示 、
、 变化的曲线分别是
变化的曲线分别是
(8)M点对应温度下,
 的转化率是
的转化率是(9)某温度下上述反应达到平衡后,保持其它条件不变,升高温度对反应速率影响的图像是___________(填编号)
A.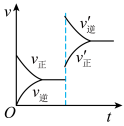 | B.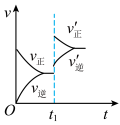 |
C.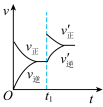 | D. |
(10)二氧化碳加氢制甲醇的总反应可表示为:
 ,该反应一般认为通过如下步骤实现:
,该反应一般认为通过如下步骤实现:①


②


若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________(填编号)
A.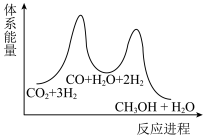 | B.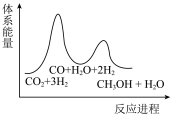 |
C.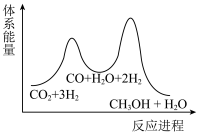 | D.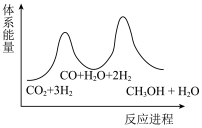 |
您最近一年使用:0次
名校
6 . 氨是化肥工业和基本有机化工的主要原料,合成氨的反应如下: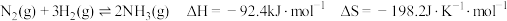
(1)判断合成氨的反应在_________ (选填“高温、低温”)能自发进行,推动反应在该条件下自发进行的主要因素是反应的_________ (选填“焓变、熵变”)。
(2)不同条件下,分别测得上述反应的反应速率,其中表示该反应进行得最快的是_______ 。
a.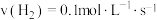 b.
b.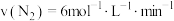
c.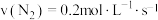 d.
d.
(3)一定温度下,向 密闭容器中加入
密闭容器中加入 和
和 ,发生上述反应,
,发生上述反应, 物质的量随时间的变化如下图所示。
物质的量随时间的变化如下图所示。
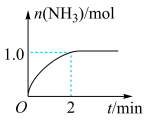
 内的平均反应速率
内的平均反应速率
________________ 。
根据反应条件,判断 内
内 变化趋势为
变化趋势为______ ,运用有效碰撞理论来解释该变化趋势:_______ 。
(4)在合成氨的实际生产过程中,常常加入含铁催化剂.请结合过渡态理论解释使用催化剂使反应速率加快的原因_______ 。
(1)判断合成氨的反应在
(2)不同条件下,分别测得上述反应的反应速率,其中表示该反应进行得最快的是
a.
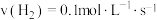 b.
b.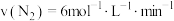
c.
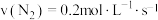 d.
d.
(3)一定温度下,向
 密闭容器中加入
密闭容器中加入 和
和 ,发生上述反应,
,发生上述反应, 物质的量随时间的变化如下图所示。
物质的量随时间的变化如下图所示。
 内的平均反应速率
内的平均反应速率
根据反应条件,判断
 内
内 变化趋势为
变化趋势为(4)在合成氨的实际生产过程中,常常加入含铁催化剂.请结合过渡态理论解释使用催化剂使反应速率加快的原因
您最近一年使用:0次
名校
7 . 尿素 是人类历史上首个由无机物人工合成的有机物。合成尿素的历程一般认为如下两步:
是人类历史上首个由无机物人工合成的有机物。合成尿素的历程一般认为如下两步:
Ⅰ.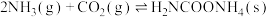
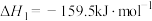
Ⅱ.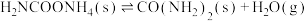
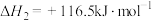
(1)将一定量的氨气和二氧化碳置于容器中,假设仅发生反应Ⅰ(假设容器体积不变,固体试样体积忽略不计),使其达到平衡。该条件下的平衡数据如下表,下列说法正确的是_______。
(2)如图中能定性表示反应Ⅰ的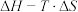 ,随温度变化的曲线是
,随温度变化的曲线是_______ 。
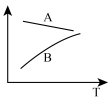
A.A曲线B.B曲线
(3)若反应Ⅱ为慢反应,下列示意图中能体现上述反应能量变化的是_______。
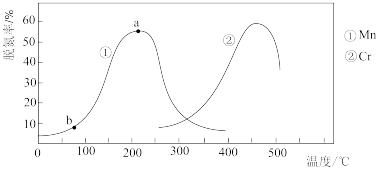
(4) 催化还原法能治理氮氧化物污染。如图所示是一定时间内,在不同温度下分别使用催化剂Mn和Cr时的脱氮率,由此可知工业上使用的最佳催化剂和相应最佳温度分别为
催化还原法能治理氮氧化物污染。如图所示是一定时间内,在不同温度下分别使用催化剂Mn和Cr时的脱氮率,由此可知工业上使用的最佳催化剂和相应最佳温度分别为_______ ;使用Mn作催化剂时,脱氮率b~a段呈现如图所示变化的原因可能是_______ 。
 是人类历史上首个由无机物人工合成的有机物。合成尿素的历程一般认为如下两步:
是人类历史上首个由无机物人工合成的有机物。合成尿素的历程一般认为如下两步:Ⅰ.
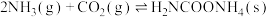
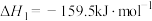
Ⅱ.
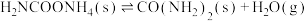
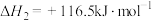
(1)将一定量的氨气和二氧化碳置于容器中,假设仅发生反应Ⅰ(假设容器体积不变,固体试样体积忽略不计),使其达到平衡。该条件下的平衡数据如下表,下列说法正确的是_______。
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度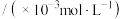 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A.该可逆反应达到平衡的标志之一是混合气体平均相对分子质量不变 |
B.因该反应熵变 小于0,焓变 小于0,焓变 小于0,所以在高温下正向自发进行 小于0,所以在高温下正向自发进行 |
C.达到平衡后,若在恒温下压缩容器体积, 固体的质量增加 固体的质量增加 |
D.根据表中数据,计算15.0℃时的 平衡浓度为 平衡浓度为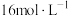 |
(2)如图中能定性表示反应Ⅰ的
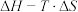 ,随温度变化的曲线是
,随温度变化的曲线是
A.A曲线B.B曲线
(3)若反应Ⅱ为慢反应,下列示意图中能体现上述反应能量变化的是_______。
A. | B.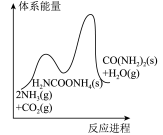 | C. | D.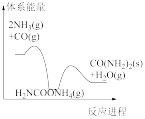 |
(4)
 催化还原法能治理氮氧化物污染。如图所示是一定时间内,在不同温度下分别使用催化剂Mn和Cr时的脱氮率,由此可知工业上使用的最佳催化剂和相应最佳温度分别为
催化还原法能治理氮氧化物污染。如图所示是一定时间内,在不同温度下分别使用催化剂Mn和Cr时的脱氮率,由此可知工业上使用的最佳催化剂和相应最佳温度分别为
您最近一年使用:0次
名校
8 . 我国向国际社会承诺2030年“碳达峰”,2060年实现“碳中和”。研发利用二氧化碳技术,降低空气中二氧化碳含量成为重要的任务。
(1)倡导绿色低碳的生活方式,下列措施与节能减碳矛盾的是_____
(2) 加氢合成
加氢合成 的反应为
的反应为 。
。
①下列说法正确的是_____
A.调控反应条件不能改变反应限度
B.投入 和
和 能得到
能得到
C.当 的消耗速率等于其生成速率时,该反应已停止
的消耗速率等于其生成速率时,该反应已停止
D.该反应在一定温度下能自发进行,则
②一般认为,该反应经过如下步骤来实现:
反应Ⅰ: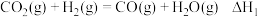 ;
;
反应Ⅱ: 。
。
则总反应的焓变
___________ (用包含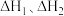 的代数式表示)。若某温度下,反应Ⅰ的平衡常数为
的代数式表示)。若某温度下,反应Ⅰ的平衡常数为 ,反应Ⅱ的平衡常数为
,反应Ⅱ的平衡常数为 ,则总反应的平衡常数
,则总反应的平衡常数
___________ (用包含 的代数式表示)
的代数式表示)
(3)二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一
甲烷化主反应: ;
;
①写出主反应的平衡常数表达式:___________
②某容器中加入一定量的 和
和 ,保持温度和压强不变的情况下,达平衡后再向该容器中注入
,保持温度和压强不变的情况下,达平衡后再向该容器中注入 稀释,主反应的化学平衡将
稀释,主反应的化学平衡将___________ (填“正向移动”、“逆向移动”或“不移动”),达到新平衡后, 的体积分数将
的体积分数将___________ (填“增大”、“减小”或“不变”)
(4) 与
与 是典型的温室气体,
是典型的温室气体, 重整制合成气提供了一条规模化综合利用碳源、氢源并转化温室气体的技术路线:
重整制合成气提供了一条规模化综合利用碳源、氢源并转化温室气体的技术路线: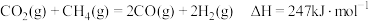
①该反应
___________ 0(填“>”或“<”)
②有传闻 重整制合成气可以在任何条件下自发进行,你认为此传闻是否正确?
重整制合成气可以在任何条件下自发进行,你认为此传闻是否正确?___________ (填“正确”或“错误”),并写出原因___________ 。
(1)倡导绿色低碳的生活方式,下列措施与节能减碳矛盾的是_____
| A.购物时使用环保袋 | B.就餐时践行光盘行动 |
| C.使用节能灯代替白炽灯 | D.为食品保鲜,冰箱温度越低越好 |
 加氢合成
加氢合成 的反应为
的反应为 。
。①下列说法正确的是
A.调控反应条件不能改变反应限度
B.投入
 和
和 能得到
能得到
C.当
 的消耗速率等于其生成速率时,该反应已停止
的消耗速率等于其生成速率时,该反应已停止D.该反应在一定温度下能自发进行,则

②一般认为,该反应经过如下步骤来实现:
反应Ⅰ:
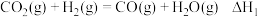 ;
;反应Ⅱ:
 。
。则总反应的焓变

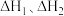 的代数式表示)。若某温度下,反应Ⅰ的平衡常数为
的代数式表示)。若某温度下,反应Ⅰ的平衡常数为 ,反应Ⅱ的平衡常数为
,反应Ⅱ的平衡常数为 ,则总反应的平衡常数
,则总反应的平衡常数
 的代数式表示)
的代数式表示)(3)二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一
甲烷化主反应:
 ;
;①写出主反应的平衡常数表达式:
②某容器中加入一定量的
 和
和 ,保持温度和压强不变的情况下,达平衡后再向该容器中注入
,保持温度和压强不变的情况下,达平衡后再向该容器中注入 稀释,主反应的化学平衡将
稀释,主反应的化学平衡将 的体积分数将
的体积分数将(4)
 与
与 是典型的温室气体,
是典型的温室气体, 重整制合成气提供了一条规模化综合利用碳源、氢源并转化温室气体的技术路线:
重整制合成气提供了一条规模化综合利用碳源、氢源并转化温室气体的技术路线: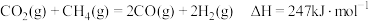
①该反应

②有传闻
 重整制合成气可以在任何条件下自发进行,你认为此传闻是否正确?
重整制合成气可以在任何条件下自发进行,你认为此传闻是否正确?
您最近一年使用:0次
名校
9 . 室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:① ;②
;② 。反应体系中组分M、Z的浓度随时间变化情况如图所示。
。反应体系中组分M、Z的浓度随时间变化情况如图所示。
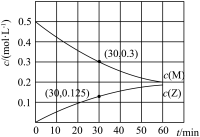
(1)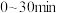 时间段内,
时间段内, 的平均反应速率为
的平均反应速率为___________ 。
(2)其中,反应①的速率可以表示为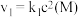 ,反应②的速率可以表示为
,反应②的速率可以表示为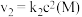 (
( 、
、 为速率常数)。下列说法正确的是___________。
为速率常数)。下列说法正确的是___________。
 ;②
;② 。反应体系中组分M、Z的浓度随时间变化情况如图所示。
。反应体系中组分M、Z的浓度随时间变化情况如图所示。
(1)
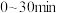 时间段内,
时间段内, 的平均反应速率为
的平均反应速率为(2)其中,反应①的速率可以表示为
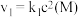 ,反应②的速率可以表示为
,反应②的速率可以表示为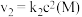 (
( 、
、 为速率常数)。下列说法正确的是___________。
为速率常数)。下列说法正确的是___________。A.反应开始后,系统中 和 和 的浓度之比保持不变 的浓度之比保持不变 |
B.如果反应能进行到底,则反应结束时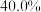 的M能转化为 的M能转化为 |
C.该温度下,两个反应的 与 与 一定都小于0 一定都小于0 |
D.该温度下,两个反应 |
您最近一年使用:0次
名校
10 . 地下水中的氮污染主要是由 引起的,人们对
引起的,人们对 的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,H2将硝酸盐还原成氮气:
的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,H2将硝酸盐还原成氮气: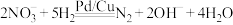 。
。
(1)氮肥NH4NO3溶于水的过程中熵值_______ (填“增大”或“减小”),Pd/Cu双金属催化剂_______ (填“是”或“不是”)决定反应自发发生的决定因素。
(2)已知: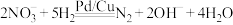 的
的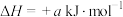 ,
,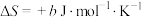 (a、b均为正值),该反应
(a、b均为正值),该反应_______ (填“能”“不能”或“无法判断是否能”)自发进行。
 引起的,人们对
引起的,人们对 的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,H2将硝酸盐还原成氮气:
的转化进行了长时间的研究,目前主要有物理方法、化学方法和生物方法,其中化学方法主要包含活泼金属还原法和催化反硝化法。催化反硝化法是一种经济可行的脱氮方法,其原理是在Pd/Cu双金属催化剂作用下,H2将硝酸盐还原成氮气: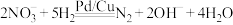 。
。(1)氮肥NH4NO3溶于水的过程中熵值
(2)已知:
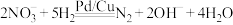 的
的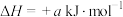 ,
,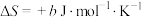 (a、b均为正值),该反应
(a、b均为正值),该反应
您最近一年使用:0次



