名校
解题方法
1 . 能源是现代社会发展的支柱之一,请按要求完成以下填空:
(1)下列反应中,属于放热反应的是_______ (填序号)。
a.Ba(OH)2•8H2O与NH4Cl混合搅拌 b.高温煅烧石灰石 c.铝与盐酸反应
(2)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式_______ 。
(3)实验测得,1g甲醇(CH3OH,常温下为液态)在氧气中充分燃烧生成二氧化碳和液态水释放出22.7kJ的热量,试写出甲醇摩尔燃烧焓的热化学方程式:_______ 。
(4)火箭推进器常以气态联氨(N2H4)为燃料、液态过氧化氢为助燃剂进行热能提供。反应过程中生成的气体可参与大气循环。测得当反应过程中有1mol水蒸气生成时放出161kJ的热量。试写出反应过程中的热化学方程式:_______ 。
(5)将 转化为
转化为 是工业冶炼金属钛的主要反应之一。已知:
是工业冶炼金属钛的主要反应之一。已知:

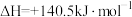
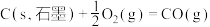
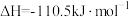
则反应 的
的 是
是_______
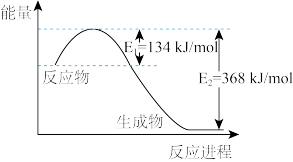
(6)工业上用二氧化碳催化加氢可合成乙醇,过程能量变化如图所示,其反应原理为2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) △H。该反应的△H
C2H5OH(g)+3H2O(g) △H。该反应的△H_______ (填“>”、“<”或“=”)0;其正反应在_______ (填“高温”“低温”或“任何温度”)下能自发进行。
(1)下列反应中,属于放热反应的是
a.Ba(OH)2•8H2O与NH4Cl混合搅拌 b.高温煅烧石灰石 c.铝与盐酸反应
(2)已知稀溶液中,1mol H2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式
(3)实验测得,1g甲醇(CH3OH,常温下为液态)在氧气中充分燃烧生成二氧化碳和液态水释放出22.7kJ的热量,试写出甲醇摩尔燃烧焓的热化学方程式:
(4)火箭推进器常以气态联氨(N2H4)为燃料、液态过氧化氢为助燃剂进行热能提供。反应过程中生成的气体可参与大气循环。测得当反应过程中有1mol水蒸气生成时放出161kJ的热量。试写出反应过程中的热化学方程式:
(5)将
 转化为
转化为 是工业冶炼金属钛的主要反应之一。已知:
是工业冶炼金属钛的主要反应之一。已知:
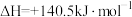
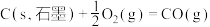
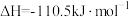
则反应
 的
的 是
是(6)工业上用二氧化碳催化加氢可合成乙醇,过程能量变化如图所示,其反应原理为2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g) △H。该反应的△H
C2H5OH(g)+3H2O(g) △H。该反应的△H
您最近一年使用:0次
名校
2 . 氢气和氧气发生反应生成水的过程用如下模型表示,“—”表示化学键。下列说法正确的是


| A.过程I是放热过程 |
| B.该反应的能量转化形式只能以热能的形式进行 |
| C.a的总能量大于d的总能量 |
| D.1 mol H2O在不同状态时的熵值:S[H2O(l)]<S[H2O(s)] |
您最近一年使用:0次
2022-12-08更新
|
163次组卷
|
2卷引用:福建省南安市侨光中学2022-2023学年高二上学期12月月考化学试题
3 . 下列说法中正确的是
| A.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
B.已知反应 的平衡常数为 的平衡常数为 ,则 ,则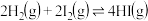 的平衡常数为 的平衡常数为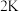 |
| C.由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程 |
| D.电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 |
您最近一年使用:0次
4 . 汽车尾气(含烃类、CO、NO与SO2等)是城市主要污染源之一,治理的办法之一是在汽车排气管上装催化转化器,它使NO与CO反应生成可参与大气生态循环的无毒气体,其反应原理是2NO(g)+2CO(g)=N2(g)+2CO2(g)。由此可知,下列说法中正确的是
| A.该反应是熵增大的反应 |
| B.该反应不能自发进行,因此需要合适的催化剂 |
| C.该反应常温下能自发进行,高温和催化剂条件只是加快反应的速率 |
| D.该反应常温下能自发进行,因为正反应是吸热反应 |
您最近一年使用:0次
2022-12-05更新
|
75次组卷
|
3卷引用:福建省建瓯市芝华中学2021-2022学年高二上学期期中考试化学试题
解题方法
5 . 化学在日常生活和生产中有着重要的应用。下列说法不正确的是
| A.热的纯碱溶液去油污效果好 |
B.焊接钢材时,常用饱和 溶液处理焊接点 溶液处理焊接点 |
| C.冰在室温下自动融化成水,是熵增的重要结果 |
| D.使用高效催化剂是提高原料平衡转化率的有效方法 |
您最近一年使用:0次
6 . 下列说法不正确的是
A.恒温恒压下, 且 且 的反应正向能自发进行 的反应正向能自发进行 |
| B.相同物质的量的同种物质气态时熵值最大,固态时熵值最小 |
C.反应 在室温下可自发进行,则该反应的 在室温下可自发进行,则该反应的 |
| D.非自发的反应一定可以通过改变条件使其成为自发反应 |
您最近一年使用:0次
22-23高二上·广东深圳·期中
名校
7 . 某反应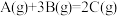 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是

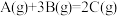 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
| A.反应物比生成物稳定 | B.该反应为吸热反应 |
| C.该反应在低温下可以自发进行 | D.温度升高会降低该反应的正反应速率 |
您最近一年使用:0次
8 . 工业废气的排放对环境造成了极大的影响,研究其吸收或再利用对缓解环境污染有重要意义。请根据所学知识回答下列问题。
(1)工业废气中的H2S可用Fe2(SO4)3溶液吸收,反应后的溶液可在硫杆菌的作用下实现吸收液的再生。用Fe2(SO4)3吸收液脱除H2S经历以下三步:
I: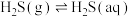 ΔH<0
ΔH<0
II: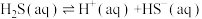
III: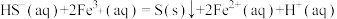
①步骤I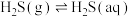 在
在_______ (填“高温下”“低温下”或“任何条件下”)有利于自发进行。
②第II步的电离平衡常数的表达式为_______ 。
③反应后的溶液在硫杆菌的作用下进行的再生反应为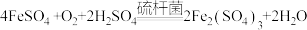 。该反应中每消耗标准状况下11.2LO2,可以再生出
。该反应中每消耗标准状况下11.2LO2,可以再生出_______ mol Fe2(SO4)3.该再生反应_______ (填“能”或“不能”)在高温下进行,理由是_______ 。
(2)CO2的大量排放会加剧温室效应,实现CO2的资源化利用不但能有效减少CO2排放,还可以变废为宝。CO2催化加氢合成二甲醚是一种CO2转化方法,转化过程中主要发生下列反应:
反应I: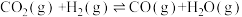 ΔH1=+41.2kJ·mol-1
ΔH1=+41.2kJ·mol-1
反应II: ΔH2=-122.5kJ·mol-1
ΔH2=-122.5kJ·mol-1
① ΔH3=
ΔH3=_______ kJ·mol-1
②在一压强为170kPa的恒压密闭容器中充入1molCO2和1mol H2发生反应I、II,CO2平衡转化率和平衡时CH3OCH3的选择性(CH3OCH3的选择性=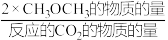 ×100%)随温度的变化如图。
×100%)随温度的变化如图。
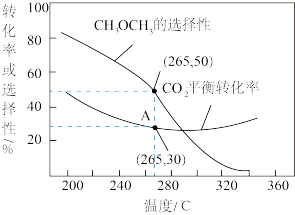
计算A点时H2(g)的转化率为_______ %,此温度下反应I的分压(分压=物质的量分数×总压)平衡常数Kp=_______ (保留一位有效数字)。
(1)工业废气中的H2S可用Fe2(SO4)3溶液吸收,反应后的溶液可在硫杆菌的作用下实现吸收液的再生。用Fe2(SO4)3吸收液脱除H2S经历以下三步:
I:
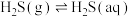 ΔH<0
ΔH<0II:
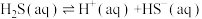
III:
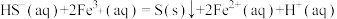
①步骤I
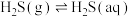 在
在②第II步的电离平衡常数的表达式为
③反应后的溶液在硫杆菌的作用下进行的再生反应为
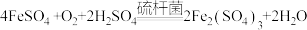 。该反应中每消耗标准状况下11.2LO2,可以再生出
。该反应中每消耗标准状况下11.2LO2,可以再生出(2)CO2的大量排放会加剧温室效应,实现CO2的资源化利用不但能有效减少CO2排放,还可以变废为宝。CO2催化加氢合成二甲醚是一种CO2转化方法,转化过程中主要发生下列反应:
反应I:
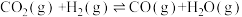 ΔH1=+41.2kJ·mol-1
ΔH1=+41.2kJ·mol-1反应II:
 ΔH2=-122.5kJ·mol-1
ΔH2=-122.5kJ·mol-1①
 ΔH3=
ΔH3=②在一压强为170kPa的恒压密闭容器中充入1molCO2和1mol H2发生反应I、II,CO2平衡转化率和平衡时CH3OCH3的选择性(CH3OCH3的选择性=
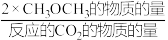 ×100%)随温度的变化如图。
×100%)随温度的变化如图。
计算A点时H2(g)的转化率为
您最近一年使用:0次
2022-11-14更新
|
165次组卷
|
3卷引用:福建省永泰县城关中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
9 . 下列反应既是氧化还原反应且在任何温度下都能正向自发进行的是
A.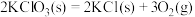  |
B.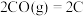 (s,石墨) (s,石墨)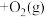  |
C.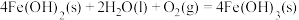  |
D.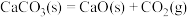  |
您最近一年使用:0次
2022-11-13更新
|
189次组卷
|
4卷引用:福建省福州市六校2023-2024学年高二上学期期中联考化学试题
10 . 下列说法正确的是
| A.反应3C(s)+CaO(s) =CaC2(s)+CO(g)在常温下不能自发进行,说明该反应的ΔH>0 |
B.同温同压下, 在光照和点燃条件的 在光照和点燃条件的 不同 不同 |
| C.夏天,打开啤酒瓶时会在瓶口逸出气体,不可以用勒夏特列原理加以解释 |
D.恒温恒压容器中发生反应N2+O2 2NO,若在容器中充入He,正逆反应的速率均不变 2NO,若在容器中充入He,正逆反应的速率均不变 |
您最近一年使用:0次
2022-11-12更新
|
103次组卷
|
2卷引用:福建省龙岩市一级校联盟(九校)联考2022-2023学年高二上学期半期考化学试题



