名校
1 . 下列说法中错误的是
| A.焓降低且熵增加的反应,在任何温度下都能自发进行 |
| B.凡是能量达到活化能的分子发生的碰撞均为有效碰撞 |
| C.平衡常数K值越大,该反应进行得越完全,平衡时反应物的转化率越大 |
| D.对于等物质的量的同一物质在不同状态时的熵值:气态>液态>固态 |
您最近一年使用:0次
名校
解题方法
2 . 甲醇是重要的化工原料之一,也可用作燃料,利用合成气(主要成分为CO、 和
和 )可以合成甲醇,涉及的反应如下:
)可以合成甲醇,涉及的反应如下:
反应i:

反应ii:
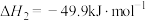
反应iii:

(1)在某催化剂作用下,反应i的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*表示吸附在催化剂上):
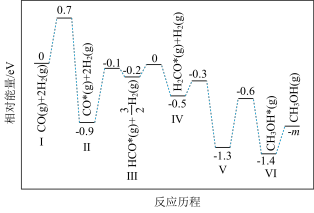
①反应i在________ (填“较低”或“较高”)温度下才能自发进行。
②结合反应历程,写出反应i中生成甲醇的决速步骤的反应方程式:________ 。
(2)将一定量的 和
和 充入密闭容器中并加入合适的催化剂,只发生反应ii和iii。一定条件下,测得
充入密闭容器中并加入合适的催化剂,只发生反应ii和iii。一定条件下,测得 的平衡转化率、
的平衡转化率、 的选择性
的选择性 和CO的选择性
和CO的选择性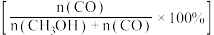 随压强的变化曲线如图所示。
随压强的变化曲线如图所示。

①图中表示 的平衡转化率的曲线是
的平衡转化率的曲线是________ (填“m”、“n”或“p”下同) 的选择性曲线是
的选择性曲线是________ CO的选择性曲线是________ 。
②有利于提高提高甲醇选择性的条件是________ 。
A.低温高压 B.低温低压 C.高温高压 D.高温低压
(3)有研究认为,在某催化剂作用下反应ii先后通过反应iii、i来实现。保持温度T不变,向一2L恒容密闭容器中充入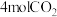 和
和 ,在该催化剂作用下发生反应,经5min达到平衡,测得
,在该催化剂作用下发生反应,经5min达到平衡,测得 的物质的量为3mol,起始及达平衡时容器的总压强比为3:2,则从开始到平衡用
的物质的量为3mol,起始及达平衡时容器的总压强比为3:2,则从开始到平衡用 表示的平均反应速率为
表示的平均反应速率为________  。
。
 和
和 )可以合成甲醇,涉及的反应如下:
)可以合成甲醇,涉及的反应如下:反应i:


反应ii:

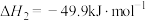
反应iii:


(1)在某催化剂作用下,反应i的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*表示吸附在催化剂上):
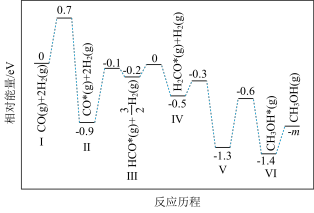
①反应i在
②结合反应历程,写出反应i中生成甲醇的决速步骤的反应方程式:
(2)将一定量的
 和
和 充入密闭容器中并加入合适的催化剂,只发生反应ii和iii。一定条件下,测得
充入密闭容器中并加入合适的催化剂,只发生反应ii和iii。一定条件下,测得 的平衡转化率、
的平衡转化率、 的选择性
的选择性 和CO的选择性
和CO的选择性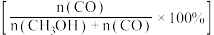 随压强的变化曲线如图所示。
随压强的变化曲线如图所示。
①图中表示
 的平衡转化率的曲线是
的平衡转化率的曲线是 的选择性曲线是
的选择性曲线是②有利于提高提高甲醇选择性的条件是
A.低温高压 B.低温低压 C.高温高压 D.高温低压
(3)有研究认为,在某催化剂作用下反应ii先后通过反应iii、i来实现。保持温度T不变,向一2L恒容密闭容器中充入
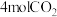 和
和 ,在该催化剂作用下发生反应,经5min达到平衡,测得
,在该催化剂作用下发生反应,经5min达到平衡,测得 的物质的量为3mol,起始及达平衡时容器的总压强比为3:2,则从开始到平衡用
的物质的量为3mol,起始及达平衡时容器的总压强比为3:2,则从开始到平衡用 表示的平均反应速率为
表示的平均反应速率为 。
。
您最近一年使用:0次
名校
3 . 化学与科学、技术、社会和环境密切相关。下列说法错误的是
| A.工业生产中使用催化剂不能改变化学反应的焓变 |
B.已知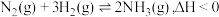 ,工业上采用高温提高 ,工业上采用高温提高 的转化率 的转化率 |
C.工业上用 合成 合成 ,增加氧气的量可提高 ,增加氧气的量可提高 的利用率 的利用率 |
D.工业上 ,高温下能自发进行 ,高温下能自发进行 |
您最近一年使用:0次
2023-12-14更新
|
93次组卷
|
2卷引用:广东省江门市新会第一中学2023-2024学年高二上学期期中考试化学试题
名校
4 . 下列关于化学反应的自发性和进行方向的说法,其中正确的是
| A.多数自发反应都是吸热反应。 |
B.一定温度下,反应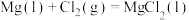 的 的 , , |
C.由 可知,所有放热反应都能自发进行 可知,所有放热反应都能自发进行 |
D.当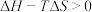 时,则反应能自发进行 时,则反应能自发进行 |
您最近一年使用:0次
名校
5 . 在一定条件下,工业上可采用下列反应合成甲酸:
 ,下列有关说法正确的是
,下列有关说法正确的是

 ,下列有关说法正确的是
,下列有关说法正确的是| A.升高温度,正反应速率减小,逆反应速率增大 |
| B.恒温条件下,增大压强,化学平衡常数增大 |
| C.恒温恒压下,使用合适的催化剂,平衡产率会提高 |
| D.该反应在低温下可能自发进行 |
您最近一年使用:0次
解题方法
6 . 下列说法正确的是
| A.同一物质的固、液、气三种状态的熵值相同 |
| B.自发反应一定是熵增大的反应,非自发反应一定是熵减小或不变的反应 |
| C.自发反应在一定条件下才能实现 |
| D.自发反应在任何条件下都能实现 |
您最近一年使用:0次
7 . 将 转化为燃料甲醇是实现碳中和的途径之一、在恒温恒容密闭容器中进行反应:
转化为燃料甲醇是实现碳中和的途径之一、在恒温恒容密闭容器中进行反应:

 ,下列有关说法正确的是
,下列有关说法正确的是
 转化为燃料甲醇是实现碳中和的途径之一、在恒温恒容密闭容器中进行反应:
转化为燃料甲醇是实现碳中和的途径之一、在恒温恒容密闭容器中进行反应:

 ,下列有关说法正确的是
,下列有关说法正确的是A.若升高温度,反应逆向进行,则 |
B.正反应为熵增过程( ),若该反应为放热反应,则在任何温度下均可自发 ),若该反应为放热反应,则在任何温度下均可自发 |
| C.若混合气体的密度不随时间变化,可说明反应达到平衡 |
D.加入催化剂,可提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次
名校
8 . 根据所学知识完成下列问题:
(1)某小组同学用量筒分别量取50mL的0.50mol∙L-1HC1溶液与50mL的0.55mol∙L-1NaOH溶液来测定中和热。
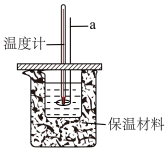
①仪器a是___________ (填名称)。
②近似认为0.55mol/L的NaOH溶液和0.50mol/L的HCl溶液的密度都是1g/mL,中和后生成溶液的比热容c=4.18J∙g-1∙℃-1,并忽略量热计的比热容;测得反应前、后体系的温度值(℃)分别为T0、T1,则所测中和热为△H=___________ kJ·mol-1(用含T0、T1的代数式表示)。
③若量取盐酸时候俯视刻度线,且其他操作无误,最终会使测得的中和热△H___________ (填“不变”、“变大”或“变小”)。
(2)研究氮和硫的氧化物的无害化处理对治理大气污染有着重要意义:
①已知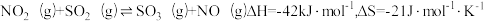 ,该反应能够自发进行的温度条件是
,该反应能够自发进行的温度条件是___________ K。
②将NO2和SO2以物质的量比1:2置于一体积不变的密闭容器中,在绝热条件下发生上述反应,下列不能说明该反应到达平衡状态的是:___________
a.每消耗1molNO2同时生成1molSO3 b.混合气体的颜色保持不变
c.体系的压强保持不变 d.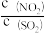 保持不变
保持不变
e.混合气体的平均摩尔质量保持不变
(3)HCN的电子式为___________ 。25℃时,HCN溶液与同浓度同体积的NaOH溶液充分反应后,最终pH为11.9,用离子方程式说明最终溶液虽碱性的原因:___________ 。
(4)阻燃剂Sb2O3(三氧化二铋)一般由SbCl3水解制备。实验室模拟制备过程如下:先将SbC13于一定条件下水解生成SbOC1白色沉淀,这一步的化学方程式为___________ ,再往其中加入少量氨水并搅拌,最终生成Sb2O3。
(1)某小组同学用量筒分别量取50mL的0.50mol∙L-1HC1溶液与50mL的0.55mol∙L-1NaOH溶液来测定中和热。

①仪器a是
②近似认为0.55mol/L的NaOH溶液和0.50mol/L的HCl溶液的密度都是1g/mL,中和后生成溶液的比热容c=4.18J∙g-1∙℃-1,并忽略量热计的比热容;测得反应前、后体系的温度值(℃)分别为T0、T1,则所测中和热为△H=
③若量取盐酸时候俯视刻度线,且其他操作无误,最终会使测得的中和热△H
(2)研究氮和硫的氧化物的无害化处理对治理大气污染有着重要意义:
①已知
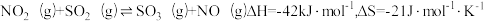 ,该反应能够自发进行的温度条件是
,该反应能够自发进行的温度条件是②将NO2和SO2以物质的量比1:2置于一体积不变的密闭容器中,在绝热条件下发生上述反应,下列不能说明该反应到达平衡状态的是:
a.每消耗1molNO2同时生成1molSO3 b.混合气体的颜色保持不变
c.体系的压强保持不变 d.
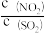 保持不变
保持不变e.混合气体的平均摩尔质量保持不变
(3)HCN的电子式为
(4)阻燃剂Sb2O3(三氧化二铋)一般由SbCl3水解制备。实验室模拟制备过程如下:先将SbC13于一定条件下水解生成SbOC1白色沉淀,这一步的化学方程式为
您最近一年使用:0次
2023-12-13更新
|
143次组卷
|
2卷引用:广东省东莞市东莞中学2023-2024学年高二上学期期中考试化学试题
名校
9 . 由下列实验事实所得出的结论正确的是
| 选项 | 实验事实 | 结论 |
| A | 某温度下,向容积可变的密闭容器中加入足量CaCO3,发生反应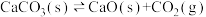 ,并达到平衡,将容器容积增大为原来的2倍 ,并达到平衡,将容器容积增大为原来的2倍 | 当体系再次达到平衡时,气体密度不变 |
| B | 恒温恒容条件下, ,增加 ,增加 的物质的量 的物质的量 | H2O的平衡转化率提高,且增大其反应速率 |
| C | 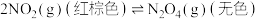  ,在反应达到平衡后,对平衡体系采取缩小容积、增大压强的措施, ,在反应达到平衡后,对平衡体系采取缩小容积、增大压强的措施, | 因为平衡向正反应方向移动,故体系颜色变浅 |
| D | 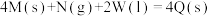 常温下,自发进行 常温下,自发进行 | 则ΔH>0 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 下列关于化学反应方向及其判据的说法中正确的是
| A.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH>0 |
| B.1molSO3在不同状态时的熵值:S[SO3(s)]>S[SO3(l)]>S[SO3(g)] |
| C.凡是需要加热的反应都不能自发进行 |
| D.反应2KClO3(s)=2KCl(s)+3O2(g) ΔH>0能否自发进行与温度无关 |
您最近一年使用:0次



