名校
1 . 将一定量纯净的氨基甲酸铵(NH2COONH4)粉末置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)⇌2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据列于下表,下列说法正确的是
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A.该反应的ΔH<0 | B.该反应在较低温度下能自发进行 |
| C.反应过程中气体平均摩尔质量保持不变 | D.再加入少量NH2COONH4平衡正向移动 |
您最近一年使用:0次
名校
解题方法
2 . 2009年12月7日~18日在丹麦首都哥本哈根召开了世界气候大会,商讨《京都议定书》一期承诺到期后的后续方案,即2012年至2020年的全球减排协议,大会倡导“节能减排” 和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。过渡排放CO2会造成“温室效应”,科学家正在研究如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),如图表示该反应过程中能量(单位为kJ·mol-1)的变化:
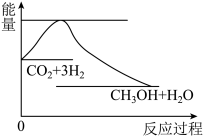
(1)关于该反应的下列说法中,正确的是______ (填字母)。
A.△H>0,△S>0 B.△H>0,△S<0 C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),经测得CO2和CH3OH(g)的浓度随时间变化如图所示。
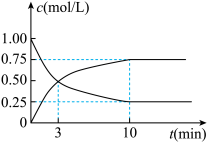
①从反应开始到平衡,CO2的平均反应速率v(CO2) =______ 。
②该反应的平衡常数表达式K=______ 。温度升高,平衡常数K______ (填增大、减小或不变)
③下列措施中能使化学平衡向正反应方向移动的是______ (填字母)。
A.升高温度
B.将CH3OH(g)及时液化抽出
C.选择高效催化剂
D.保持容器的容积不变,再充入l molCO2和3 molH2
④不能说明该反应达到化学平衡状态的是______ 。
a.容器中混合气体的平均相对分子质量不再改变
b.混合气体中c(CO2)不变
c.v正(H2)=v逆(H2O)
d.容器内的压强保持不变

(1)关于该反应的下列说法中,正确的是
A.△H>0,△S>0 B.△H>0,△S<0 C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),经测得CO2和CH3OH(g)的浓度随时间变化如图所示。

①从反应开始到平衡,CO2的平均反应速率v(CO2) =
②该反应的平衡常数表达式K=
③下列措施中能使化学平衡向正反应方向移动的是
A.升高温度
B.将CH3OH(g)及时液化抽出
C.选择高效催化剂
D.保持容器的容积不变,再充入l molCO2和3 molH2
④不能说明该反应达到化学平衡状态的是
a.容器中混合气体的平均相对分子质量不再改变
b.混合气体中c(CO2)不变
c.v正(H2)=v逆(H2O)
d.容器内的压强保持不变
您最近一年使用:0次
名校
3 . 下列利用相关数据作出的推理或判断一定正确的是
| A.利用焓变数据判断反应能否自发进行 |
| B.利用反应热数据判断反应速率的大小 |
| C.利用平衡常数判断反应进行的程度大小 |
| D.利用反应的活化能数据判断反应热的大小 |
您最近一年使用:0次
2020-12-29更新
|
385次组卷
|
4卷引用:重庆复旦中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
4 . 下列变化过程属于熵增的是
A.N2(g) + 3H2(g) 2NH3(g) 2NH3(g) | B.NaOH(aq)+ HCl(aq) = NaCl(aq)+ H2O(l) |
| C.C(s) + CO2(g) =2CO(g) | D.NH3(g) + HCl(g) = NH4Cl(s) |
您最近一年使用:0次
2020-12-28更新
|
440次组卷
|
4卷引用:重庆市朝阳中学高2020-2021学年高二上学期期中考试化学试题
重庆市朝阳中学高2020-2021学年高二上学期期中考试化学试题安徽省六安市新安中学2020-2021学年高二上学期期末考试(重点班)化学试题(已下线)2.4 化学反应进行的方向-2021-2022学年高二化学课后培优练(人教版选修4)天津市部分区2021-2022学年高二上学期期中练习化学试题
名校
解题方法
5 . 二氧化碳的捕集、存储和转化是当今化学研究的热点问题之一。
(1)用钌的配合物作催化剂,可直接光催化分解CO2,发生反应2CO2(g) 2CO(g)+O2(g),该反应的△H
2CO(g)+O2(g),该反应的△H_______ (填">""<"或"=",下同)0,△S_______ 0,在低温下,该反应_______ (填"能"或"不能")自发进行。
(2)在密闭容器中发生如下反应:C(s)+CO2(g)⇌2CO(g),以下能够证明该反应达到平衡状态的是_______ 。
①相同时间内生成1 mol CO2,同时消耗0.5 mol CO
②温度一定时,在恒容容器中压强不变
③相同时间,断裂1NA C=O键同时断裂1NA C≡O
④恒容容器内气体密度不变
⑤绝热容器内,体系温度不变
⑥反应到某时刻c(CO2):c(CO)=1:2
⑦气体平均摩尔质量不变
(1)用钌的配合物作催化剂,可直接光催化分解CO2,发生反应2CO2(g)
 2CO(g)+O2(g),该反应的△H
2CO(g)+O2(g),该反应的△H(2)在密闭容器中发生如下反应:C(s)+CO2(g)⇌2CO(g),以下能够证明该反应达到平衡状态的是
①相同时间内生成1 mol CO2,同时消耗0.5 mol CO
②温度一定时,在恒容容器中压强不变
③相同时间,断裂1NA C=O键同时断裂1NA C≡O
④恒容容器内气体密度不变
⑤绝热容器内,体系温度不变
⑥反应到某时刻c(CO2):c(CO)=1:2
⑦气体平均摩尔质量不变
您最近一年使用:0次
6 . 下列有关说法正确的是
| A.吸热反应只有加热才能发生 |
| B.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
| C.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH>0 |
| D.N2(g)+3H2(g)=2NH3(g) ΔH<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大 |
您最近一年使用:0次
2020-11-29更新
|
109次组卷
|
3卷引用:重庆市2023-2024学年高二下学期开学考试化学试题
名校
7 . 可逆反应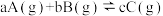 中生成物C的体积分数(C%)与压强(P)、温度(T)的关系如图所示,关于该反应的判断正确的是
中生成物C的体积分数(C%)与压强(P)、温度(T)的关系如图所示,关于该反应的判断正确的是
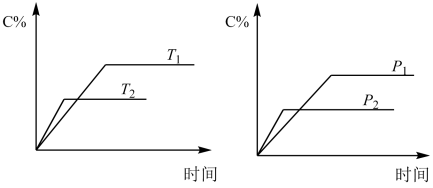
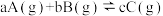 中生成物C的体积分数(C%)与压强(P)、温度(T)的关系如图所示,关于该反应的判断正确的是
中生成物C的体积分数(C%)与压强(P)、温度(T)的关系如图所示,关于该反应的判断正确的是
| A.该反应不能自发 | B.该反应能自发进行 |
C. , , | D. , , |
您最近一年使用:0次
名校
解题方法
8 . 以下判断正确的是
A.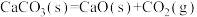 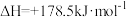 ,该反应低温才能自发 ,该反应低温才能自发 |
B.通常化学反应的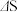 越大,越有利于反应自发进行,所以 越大,越有利于反应自发进行,所以 时反应必能自发 时反应必能自发 |
C.常温下,反应 不能自发进行,则该反应的 不能自发进行,则该反应的 |
| D.放热反应都可以自发进行,而吸热反应不能自发进行 |
您最近一年使用:0次
2020-11-24更新
|
331次组卷
|
4卷引用:重庆市朝阳中学2021-2022学年高二上学期期中考试化学试题
9 . 肌肉中大量肌红蛋白Mb可以结合O2形成MbO2维持人体的生理活动,发生反应:Mb(aq)+O2(g) MbO2(aq) ΔH,该过程可自发进行。温度为T时,平衡常数K=
MbO2(aq) ΔH,该过程可自发进行。温度为T时,平衡常数K= 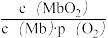 =2.0 kPa-1(气体分压=气体总压
=2.0 kPa-1(气体分压=气体总压 体积分数),下列说法中不正确的是
体积分数),下列说法中不正确的是
 MbO2(aq) ΔH,该过程可自发进行。温度为T时,平衡常数K=
MbO2(aq) ΔH,该过程可自发进行。温度为T时,平衡常数K= 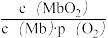 =2.0 kPa-1(气体分压=气体总压
=2.0 kPa-1(气体分压=气体总压 体积分数),下列说法中不正确的是
体积分数),下列说法中不正确的是| A.ΔH<0 |
| B.提高p(O2),K值变大 |
| C.提高氧气浓度,有利于Mb(aq)的转化 |
| D.当n(MbO2)/n(Mb)=4.0时,吸入的空气中p(O2)=21 kPa,该反应正向进行 |
您最近一年使用:0次
2020-11-16更新
|
307次组卷
|
2卷引用:重庆市乌江新高考协作体2023-2024学年高二上学期1月期末化学试题
名校
解题方法
10 . 已如:(NH4)2CO3(s)=NH4HCO3(s)+NH3(g)△H=+74.9kJ/mol。下列说法中正确的是( )
| A.该反应中△S>0,△H>0 |
| B.该反应是吸热反应,因此一定不能自发进行 |
| C.判断反应能否自发进行需要根据△H与△S综合考虑 |
| D.碳酸盐分解反应中熵增加,因此所有碳酸盐分解一定自发进行 |
您最近一年使用:0次
2020-11-12更新
|
160次组卷
|
2卷引用:重庆市璧山来凤中学2023-2024学年高二上学期9月月考化学试题



