名校
1 . 恒容密闭容器中发生反应
 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是A.室温下能自发进行,表明该反应的 |
| B.保持温度一定,充入氩气使反应速率加快 |
| C.加入合适的催化剂,既能改变反应历程又能降低活化能 |
D.其他条件一定,再通入适量 , , 和 和 的转化率都将增大 的转化率都将增大 |
您最近一年使用:0次
2024-02-29更新
|
82次组卷
|
2卷引用:四川省德阳市高中2023-2024学年学年高二上学期期末教学质量检测考试化学试题
2 . 化学是与生活联系十分紧密的一门学科,化学知识可以体现在生活各个方面,下面说法中正确的
| A.“煮豆燃豆萁”,这个过程中能量变化为化学能全部转化为热能 |
B.“白毛浮绿水”,“白毛”为烃的衍生物,不溶于水,密度比水小,燃烧生成 和 和 |
| C.“烈火焚烧若等闲”,说明反应物很稳定,没有发生化学变化 |
| D.“唯有暗香来”,是一个熵增的过程 |
您最近一年使用:0次
2024-02-24更新
|
66次组卷
|
2卷引用:四川省广元市川师大万达中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
3 . 工业燃烧煤、石油等化石燃料释放出大量氮氧化物、一氧化碳、二氧化碳等气体,严重污染空气。通过对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
(1)甲醇不仅是重要的化工原料,而且还是性能优良的能源和车用燃料。甲醇和水蒸气制取 的反应如下:
的反应如下:
反应Ⅰ: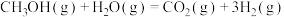
 平衡常数为
平衡常数为
反应Ⅱ:
 平衡常数为
平衡常数为
反应 的
的
______ (用含 的式子表示),平衡常数
的式子表示),平衡常数
______ (用含 的式子表示)。
的式子表示)。
(2)二氧化碳可以合成甲醇,一氧化碳也可以合成甲醇,用CO和 合成
合成 的化学方程式为
的化学方程式为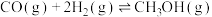
 ,向2L恒容密闭容器中加入2mol CO和4mol
,向2L恒容密闭容器中加入2mol CO和4mol  ,在适当的催化剂作用下,此反应能自发进行。
,在适当的催化剂作用下,此反应能自发进行。
①该反应
______ 0(填“>”、“<”或“=”)
②下列叙述能说明此反应达到平衡状态的是______ 。(填字母)
A.混合气体的平均相对分子质量保持不变 B.CO的转化率和 的转化率相等
的转化率相等
C.1mol CO生成的同时有2mol H-H键断裂 D.混合气体的密度保持不变
③按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,请分析:
温度:
______  ;正反应速率:
;正反应速率: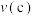
______ 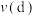 (填“>”、“<”或“=”)
(填“>”、“<”或“=”) kPa的容器中加入2mol CO和4mol
kPa的容器中加入2mol CO和4mol  ,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率
,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率
______ ,反应平衡常数表示为
______ ( 就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含
就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含 的式子表示)
的式子表示)
(1)甲醇不仅是重要的化工原料,而且还是性能优良的能源和车用燃料。甲醇和水蒸气制取
 的反应如下:
的反应如下:反应Ⅰ:
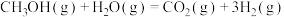
 平衡常数为
平衡常数为
反应Ⅱ:

 平衡常数为
平衡常数为
反应
 的
的
 的式子表示),平衡常数
的式子表示),平衡常数
 的式子表示)。
的式子表示)。(2)二氧化碳可以合成甲醇,一氧化碳也可以合成甲醇,用CO和
 合成
合成 的化学方程式为
的化学方程式为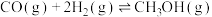
 ,向2L恒容密闭容器中加入2mol CO和4mol
,向2L恒容密闭容器中加入2mol CO和4mol  ,在适当的催化剂作用下,此反应能自发进行。
,在适当的催化剂作用下,此反应能自发进行。①该反应

②下列叙述能说明此反应达到平衡状态的是
A.混合气体的平均相对分子质量保持不变 B.CO的转化率和
 的转化率相等
的转化率相等C.1mol CO生成的同时有2mol H-H键断裂 D.混合气体的密度保持不变
③按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示,请分析:
温度:

 ;正反应速率:
;正反应速率: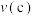
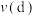 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)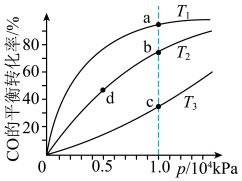
 kPa的容器中加入2mol CO和4mol
kPa的容器中加入2mol CO和4mol  ,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率
,发生反应,达到平衡。甲醇在平衡体系中所占的物质的量分数为0.25,则CO的平衡转化率

 就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含
就是用各物质的分压代替各物质的平衡浓度来表示化学平衡常数,分压=总压×物质的量分数,用含 的式子表示)
的式子表示)
您最近一年使用:0次
2024-02-21更新
|
67次组卷
|
2卷引用:四川省巴中中学2023-2024学年高二下学期3月月考化学试题
解题方法
4 .  与
与 在催化剂
在催化剂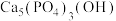 (简写为HAP)表面催化生成
(简写为HAP)表面催化生成 和
和 的历程示意图如图所示。已知该反应
的历程示意图如图所示。已知该反应 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是
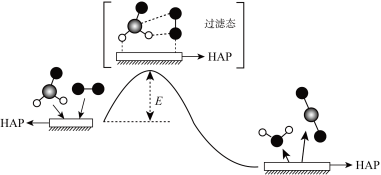
 与
与 在催化剂
在催化剂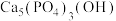 (简写为HAP)表面催化生成
(简写为HAP)表面催化生成 和
和 的历程示意图如图所示。已知该反应
的历程示意图如图所示。已知该反应 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是
| A.该反应发生时,环境温度升高 |
| B.HAP的作用是降低反应的反应热 |
C.任何条件下,HCHO和 的内能大于 的内能大于 和 和 的内能 的内能 |
| D.在高温条件自发进行 |
您最近一年使用:0次
名校
5 . 下列过程属于熵减的是
| A.-10℃的液态水自动结冰成为固态 | B.常温下,H2O2分解成H2O和O2 |
| C.NaCl晶体溶于水 | D.一盒粉笔无序散落一地 |
您最近一年使用:0次
解题方法
6 . “碳中和”目标如期实现的关键技术之一是 的再资源化利用。
的再资源化利用。
(1)氨的饱和食盐水捕获 是其利用的方法之一,反应原理为:
是其利用的方法之一,反应原理为: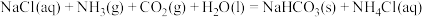 。该反应常温下能自发进行的原因是
。该反应常温下能自发进行的原因是___________ 。
(2)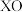 基掺杂
基掺杂 形成
形成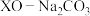 (
(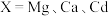 等),能用于捕获
等),能用于捕获 ,原理如下图所示。已知阳离子电荷数越高、半径越小,阴离子越易受其影响而分解。
,原理如下图所示。已知阳离子电荷数越高、半径越小,阴离子越易受其影响而分解。
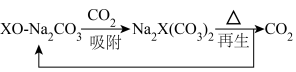
①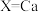 时,再生的化学方程式为
时,再生的化学方程式为___________ 。
②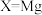 相比
相比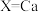 ,其优点有
,其优点有___________ 。
(3)催化电解吸收 的
的 溶液可将
溶液可将 转化为有机物。
转化为有机物。
① 在阴极放电生成
在阴极放电生成 的电极反应式为
的电极反应式为___________ 。
②碱性溶液有利于抑制阴极上副产物的产生,该副产物的化学式为___________ 。
(4)在催化剂作用下,以 和
和 为原料合成
为原料合成 ,主要反应为:
,主要反应为:
反应Ⅰ: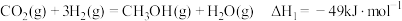
反应Ⅱ:
保持压强 ,将起始
,将起始 的混合气体匀速通过装有催化剂的反应管,测得出口处
的混合气体匀速通过装有催化剂的反应管,测得出口处 的转化率和甲醇的选择性
的转化率和甲醇的选择性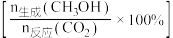 与温度的关系如题图1、题图2所示。
与温度的关系如题图1、题图2所示。
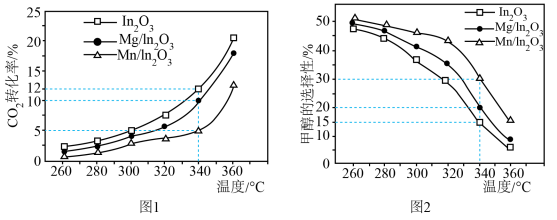
①随着温度的升高, 转化率增大、但甲醇选择性降低的原因是
转化率增大、但甲醇选择性降低的原因是___________ 。
②假设定义催化剂催化效率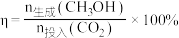 ,计算
,计算 时三种催化剂的催化效率之比
时三种催化剂的催化效率之比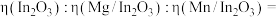
___________ (写出计算过程)。
 的再资源化利用。
的再资源化利用。(1)氨的饱和食盐水捕获
 是其利用的方法之一,反应原理为:
是其利用的方法之一,反应原理为: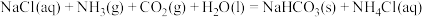 。该反应常温下能自发进行的原因是
。该反应常温下能自发进行的原因是(2)
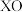 基掺杂
基掺杂 形成
形成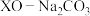 (
(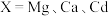 等),能用于捕获
等),能用于捕获 ,原理如下图所示。已知阳离子电荷数越高、半径越小,阴离子越易受其影响而分解。
,原理如下图所示。已知阳离子电荷数越高、半径越小,阴离子越易受其影响而分解。
①
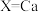 时,再生的化学方程式为
时,再生的化学方程式为②
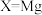 相比
相比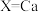 ,其优点有
,其优点有(3)催化电解吸收
 的
的 溶液可将
溶液可将 转化为有机物。
转化为有机物。①
 在阴极放电生成
在阴极放电生成 的电极反应式为
的电极反应式为②碱性溶液有利于抑制阴极上副产物的产生,该副产物的化学式为
(4)在催化剂作用下,以
 和
和 为原料合成
为原料合成 ,主要反应为:
,主要反应为:反应Ⅰ:
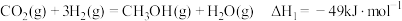
反应Ⅱ:

保持压强
 ,将起始
,将起始 的混合气体匀速通过装有催化剂的反应管,测得出口处
的混合气体匀速通过装有催化剂的反应管,测得出口处 的转化率和甲醇的选择性
的转化率和甲醇的选择性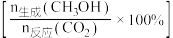 与温度的关系如题图1、题图2所示。
与温度的关系如题图1、题图2所示。
①随着温度的升高,
 转化率增大、但甲醇选择性降低的原因是
转化率增大、但甲醇选择性降低的原因是②假设定义催化剂催化效率
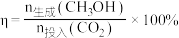 ,计算
,计算 时三种催化剂的催化效率之比
时三种催化剂的催化效率之比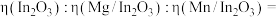
您最近一年使用:0次
2024-02-11更新
|
575次组卷
|
3卷引用:四川省宜宾市叙州区第二中学校2023-2024学年高二上学期1月期末化学试题
7 .  与
与 催化重整制取
催化重整制取 的反应方程式为
的反应方程式为 ,下列关于该反应的说法正确的是
,下列关于该反应的说法正确的是
 与
与 催化重整制取
催化重整制取 的反应方程式为
的反应方程式为 ,下列关于该反应的说法正确的是
,下列关于该反应的说法正确的是A. ,表明反应达平衡状态 ,表明反应达平衡状态 |
| B.该反应放热,在任意温度下都能自发进行 |
C.增大压强,平衡向右移动,平衡常数 增大 增大 |
D.升温可加快反应速率并提高 的平衡产率 的平衡产率 |
您最近一年使用:0次
8 . 下列说法正确的是
| A.非自发的反应一定不能发生 |
| B.反应NH3(g)+ CO2(g)+H2O(l)=NH4HCO3(s)在室温下可自发进行,则该反应的ΔH<0 |
| C.相同质量的同种物质气态时熵值最小,固态时熵值最大 |
| D.恒温恒压下,ΔH<0且ΔS>0的反应不能自发进行 |
您最近一年使用:0次
9 . 以下过程在常温下都可以自发进行,可利用焓判据来解释的是
| A.2N2O5(g)=4N2O4(g)+O2(g) ΔH=+56.7kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ·mol-1 |
| C.硝酸铵自发地溶于水 |
| D.湿衣服经过晾晒变干 |
您最近一年使用:0次
2024-01-28更新
|
40次组卷
|
2卷引用:四川省成都市成华区某校2023-2024学年高二上学期12月月考化学试题
名校
解题方法
10 . 下列推论正确的是
| A.S(g)+O2(g)=SO2(g)ΔH1,S(s)+O2(g)=SO2(g) ΔH2,则:ΔH1>ΔH2 |
| B.石墨燃烧热为393.5kJ·mol-1,则有2C(s)+O2(g)=2CO(g)ΔH=-393.5kJ·mol-1 |
| C.中和热为57.4kJ/mol,则有Ba(OH)2(aq)+H2SO4(aq)=BaSO4(s)+2H2O(l) ΔH<-114.8kJ/mol |
| D.已知CaCO3(s)=CaO(s)+CO2(g)ΔH>0,该反应任何温度下都能自发进行 |
您最近一年使用:0次
2024-01-28更新
|
29次组卷
|
2卷引用:四川省成都市成华区某校2023-2024学年高二上学期12月月考化学试题



