名校
解题方法
1 . 如图所示为工业合成氨的流程图。下列说法错误的是
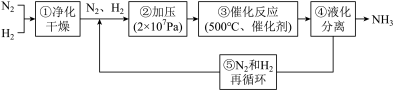

| A.步骤①中“净化”可以防止催化剂“中毒” |
| B.步骤③、④、⑤均有利于提高原料的平衡转化率 |
| C.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率 |
D.工业合成氨反应 ,该反应能在低温自发进行 ,该反应能在低温自发进行 |
您最近一年使用:0次
名校
解题方法
2 . 下列诗词中,包含ΔH>0、ΔS>0的化学变化的是
| A.日照香炉生紫烟,遥看瀑布挂前川 |
| B.千锤万凿出深山,烈火焚烧若等闲 |
| C.春蚕到死丝方,蜡炬成灰泪始干 |
| D.美人首饰侯王印,尽是沙中浪底来 |
您最近一年使用:0次
名校
3 . 下列说法中不正确的是
A.已知 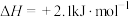 ,则灰锡更稳定,且常温常压下为灰锡状态 ,则灰锡更稳定,且常温常压下为灰锡状态 |
| B.只有活化分子之间发生的碰撞才可能是有效碰撞 |
| C.升高温度,使单位体积内活化分子数增多,因而反应速率加快 |
D.对于 且一定条件下能自发进行的化学反应,其 且一定条件下能自发进行的化学反应,其 |
您最近一年使用:0次
名校
解题方法
4 . I.课本里介绍的合成氨技术叫哈伯法,是德国诺贝尔化学奖获得者哈伯发明的。其合成原理为:N2(g)+3H2(g) 2NH3(g)∆H<0,∆S<0。
2NH3(g)∆H<0,∆S<0。
(1)下列关于工业合成氨的说法不正确的是___________
a.因为∆H<0,所以该反应一定能自发进行
b.因为∆S<0,所以该反应一定不能自发进行
c.增大N2的浓度,可以提高H2的转化率
d.使用催化剂可大大提高生产效率
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示H2物质的量)。

①图象中T2和T1的关系是:T2___________ T1(填“>,<或=”)
②a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是___________ (填字母)。
(3)在实验室中,一定条件下,加入1molN2和3molH2,反应N2(g)+3H2(g) 2NH3(g) ∆H<0,达平衡后,若改变下列条件:
2NH3(g) ∆H<0,达平衡后,若改变下列条件:
①保持温度和压强不变,充入惰性气体,则NH3的物质的量___________ 。(填“变大”、“变小”或“不变”,下同)
②保持温度和体积不变,再加入2molNH3,则H2的体积分数___________ 。
II.在1 200℃时,天然气脱硫工艺中会发生下列反应:
H2S(g)+ O2(g)=SO2(g)+H2O(g) ΔH1
O2(g)=SO2(g)+H2O(g) ΔH1
2H2S(g)+SO2(g)= S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2
H2S(g)+ O2(g)=S(g)+H2O(g) ΔH3
O2(g)=S(g)+H2O(g) ΔH3
2S(g)=S2(g) ΔH4
(4)则用ΔH1、ΔH2、ΔH3来表示ΔH4的表达式为___________ 。
 2NH3(g)∆H<0,∆S<0。
2NH3(g)∆H<0,∆S<0。(1)下列关于工业合成氨的说法不正确的是
a.因为∆H<0,所以该反应一定能自发进行
b.因为∆S<0,所以该反应一定不能自发进行
c.增大N2的浓度,可以提高H2的转化率
d.使用催化剂可大大提高生产效率
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示H2物质的量)。

①图象中T2和T1的关系是:T2
②a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是
(3)在实验室中,一定条件下,加入1molN2和3molH2,反应N2(g)+3H2(g)
 2NH3(g) ∆H<0,达平衡后,若改变下列条件:
2NH3(g) ∆H<0,达平衡后,若改变下列条件:①保持温度和压强不变,充入惰性气体,则NH3的物质的量
②保持温度和体积不变,再加入2molNH3,则H2的体积分数
II.在1 200℃时,天然气脱硫工艺中会发生下列反应:
H2S(g)+
 O2(g)=SO2(g)+H2O(g) ΔH1
O2(g)=SO2(g)+H2O(g) ΔH1 2H2S(g)+SO2(g)=
 S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2H2S(g)+
 O2(g)=S(g)+H2O(g) ΔH3
O2(g)=S(g)+H2O(g) ΔH3 2S(g)=S2(g) ΔH4
(4)则用ΔH1、ΔH2、ΔH3来表示ΔH4的表达式为
您最近一年使用:0次
名校
解题方法
5 . 完成下列问题。
(1)已知石灰石分解反应CaCO3(s)=CaO(s)+CO2(g)的ΔH>0,该反应能够自发进行的反应条件是___________ (填“高温”或“低温”)。
(2)合成氨在工业生产中具有重要意义。在合成氨工业中I2O5常用于定量测量CO的含量。已知:2I2(s)+5O2(g)=2I2O5(s) ΔH=-76 kJ·mol-1;2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1.则该测定反应的热化学方程式为___________ 。
(3)实现“碳中和”,综合利用CO2具有重要的意义。一定条件下,CO2与H2制备气态甲醇CH3OH的反应方程式为 。在容积为
。在容积为 的恒温密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。
的恒温密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。
①3~6min内,v(H2)=___________ 。
②12min末时,混合气体中CH3OH的物质的量分数为___________ 。
③第3min时v正(CH3OH)___________ 第9min时v逆(CH3OH)(填“>”、“<”或“=”,),第12min时,v正(CH3OH)___________ v逆(H2)(填“>”、“<”或“=”)。
(4)保持压强为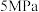 ,向密闭容器中投入一定量CO2和H2发生上述反应,若投料比
,向密闭容器中投入一定量CO2和H2发生上述反应,若投料比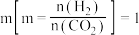 ,一定温度下发生上述反应,下列说法不能作为反应是否达到平衡的判断依据的是
,一定温度下发生上述反应,下列说法不能作为反应是否达到平衡的判断依据的是___________ (填标号)。
a.容器内气体的密度不再变化 b.容器内气体的平均相对分子质量不再变化
c.CO2的体积分数不再变化 d.断裂3NA个H-H键的同时生成NA个水分子
(5)CO2经催化加氢可以生成低碳烃,主要有以下两个竞争反应:
反应Ⅰ: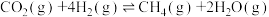
反应Ⅱ: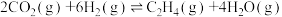
为分析催化剂对反应的选择性,在1 L密闭容器中充入2 mol CO2和4 mol H2,测得有关物质的物质的量随温度变化如图所示:
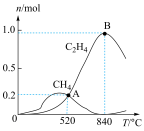
该催化剂在较低温度时主要选择___________ (填“反应Ⅰ”或“反应Ⅱ”)。520 ℃时,反应Ⅰ的平衡常数K=___________ (只列算式不计算)。
(6)温度为T时,将NH4HS(s)置于抽真空的容器中,当反应 达到平衡时,测得总压强为p,则该反应的压强平衡常数Kp为
达到平衡时,测得总压强为p,则该反应的压强平衡常数Kp为___________ 。
(1)已知石灰石分解反应CaCO3(s)=CaO(s)+CO2(g)的ΔH>0,该反应能够自发进行的反应条件是
(2)合成氨在工业生产中具有重要意义。在合成氨工业中I2O5常用于定量测量CO的含量。已知:2I2(s)+5O2(g)=2I2O5(s) ΔH=-76 kJ·mol-1;2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1.则该测定反应的热化学方程式为
(3)实现“碳中和”,综合利用CO2具有重要的意义。一定条件下,CO2与H2制备气态甲醇CH3OH的反应方程式为
 。在容积为
。在容积为 的恒温密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。
的恒温密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的物质的量随时间的变化情况如下表。| 时间 | 0min | 3min | 6min | 9min | 12min |
| n(CH3OH)/mol | 0 | 0.50 | a | 0.75 | 0.75 |
| n(CO2)/mol | 1 | 0.50 | 0.35 | 0.25 | 0.25 |
②12min末时,混合气体中CH3OH的物质的量分数为
③第3min时v正(CH3OH)
(4)保持压强为
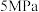 ,向密闭容器中投入一定量CO2和H2发生上述反应,若投料比
,向密闭容器中投入一定量CO2和H2发生上述反应,若投料比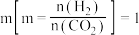 ,一定温度下发生上述反应,下列说法不能作为反应是否达到平衡的判断依据的是
,一定温度下发生上述反应,下列说法不能作为反应是否达到平衡的判断依据的是a.容器内气体的密度不再变化 b.容器内气体的平均相对分子质量不再变化
c.CO2的体积分数不再变化 d.断裂3NA个H-H键的同时生成NA个水分子
(5)CO2经催化加氢可以生成低碳烃,主要有以下两个竞争反应:
反应Ⅰ:
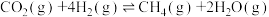
反应Ⅱ:
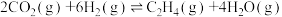
为分析催化剂对反应的选择性,在1 L密闭容器中充入2 mol CO2和4 mol H2,测得有关物质的物质的量随温度变化如图所示:

该催化剂在较低温度时主要选择
(6)温度为T时,将NH4HS(s)置于抽真空的容器中,当反应
 达到平衡时,测得总压强为p,则该反应的压强平衡常数Kp为
达到平衡时,测得总压强为p,则该反应的压强平衡常数Kp为
您最近一年使用:0次
2023-12-06更新
|
93次组卷
|
2卷引用:四川省内江市威远中学校2023-2024学年高二上学期期中考试化学试题
名校
6 . 关于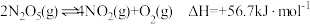 。下列说法正确的是
。下列说法正确的是
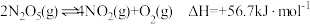 。下列说法正确的是
。下列说法正确的是| A.该反应在任何温度下都不能自发进行 |
| B.缩小体积增大压强平衡逆方向移动,达到新平衡后颜色比原来深 |
| C.恒温恒容密度不变说明达到平衡 |
D.升温正反应速率加快逆反应速率减慢,平衡正向移动 的转化率提高 的转化率提高 |
您最近一年使用:0次
2023-12-01更新
|
140次组卷
|
3卷引用:四川省安宁河联盟2023-2024学年高二上学期11月期中考试化学试题
7 . 下列对于化学反应方向说法正确的是
A.一定温度下,反应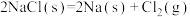 的 的 , , |
B.反应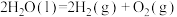  ,则该反应在低温下能自发进行 ,则该反应在低温下能自发进行 |
C.常温下反应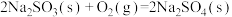 能自发进行,则 能自发进行,则 |
D.反应 在一定条件下能自发进行,则该反应的 在一定条件下能自发进行,则该反应的 |
您最近一年使用:0次
2023-11-29更新
|
131次组卷
|
2卷引用:四川省达州外国语学校2023-2024学年高二上学期12月月考化学试题
名校
解题方法
8 . 中华优秀传统文化涉及了很多化学知识,下列有关说法错误的是
| A.《本草纲目拾遗》中对强水的记载:“性最猛烈,能蚀五金。”强水涉及到强电解质 |
| B.《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”,利用的是盐类的水解 |
| C.刘长卿诗云“水声冰下咽,砂路雪中平”,固态冰转化为液态水为熵增的过程 |
D.《本草图经》记载“盖此矾色绿,味酸,烧之则赤”,因绿矾能电离出 ,所以“味酸” ,所以“味酸” |
您最近一年使用:0次
2023-11-29更新
|
259次组卷
|
2卷引用:四川省成都市郫都区绵实外国语学校2023-2024学年高二上学期12月检测化学试题
名校
9 . 下列叙述正确的是
A.在浓硫酸中滴加浓盐酸,产生 的原因是升温促进平衡 的原因是升温促进平衡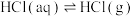 向右移动 向右移动 |
| B.从海水中提取溴,通入氯气之前用硫酸酸化的目的是增强氯气的氧化性 |
C.在高温下,CO分解生成 和 和 能自发进行 能自发进行 |
| D.铝和硫酸反应生成氢气,硫酸浓度越大,氢气生成速率越快 |
您最近一年使用:0次
2023-11-22更新
|
65次组卷
|
2卷引用:四川省泸县第一中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
10 . 下列说法正确的是
| A.增大压强,活化分子百分数增多,化学反应速率一定增大 |
| B.C(石墨,s)=C(金刚石,s) ∆H=+1.9 kJ/mol,则金刚石比石墨稳定 |
| C.CaCO3(s)=CaO(s)+CO2(g) ∆H>0,∆S>0,则不论在何种条件下都不可能自发进行 |
| D.用CH3COOH溶液和NaOH溶液反应测定中和热:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(aq) ∆H>-57.3 kJ/mol |
您最近一年使用:0次
2023-11-21更新
|
104次组卷
|
2卷引用:四川省成都列五中学2023-2024学年高二上学期10月月考化学试题



