解题方法
1 . 以CO、 为原料合成甲醇的反应为
为原料合成甲醇的反应为
 ,在容积相同的三个恒容密闭容器
,在容积相同的三个恒容密闭容器 、
、 、
、 中均充入1molCO和
中均充入1molCO和 ,三个容器的反应温度分别为
,三个容器的反应温度分别为 、
、 、
、 且恒定不变。三个容器中反应均进行到tmin时CO的体积分数示意图如图,下列说法错误的是
且恒定不变。三个容器中反应均进行到tmin时CO的体积分数示意图如图,下列说法错误的是
 为原料合成甲醇的反应为
为原料合成甲醇的反应为
 ,在容积相同的三个恒容密闭容器
,在容积相同的三个恒容密闭容器 、
、 、
、 中均充入1molCO和
中均充入1molCO和 ,三个容器的反应温度分别为
,三个容器的反应温度分别为 、
、 、
、 且恒定不变。三个容器中反应均进行到tmin时CO的体积分数示意图如图,下列说法错误的是
且恒定不变。三个容器中反应均进行到tmin时CO的体积分数示意图如图,下列说法错误的是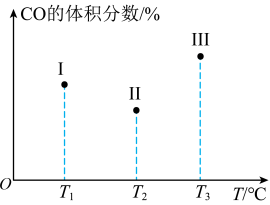
| A.该反应的反应物的总能量大于生成物的总能量 |
B.在容器 或 或 中,无论反应进行到何种程度,一定存在 中,无论反应进行到何种程度,一定存在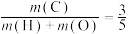 |
| C.高温条件有利于该反应自发进行 |
D.tmin时,容器 中的反应一定没有达到平衡,容器 中的反应一定没有达到平衡,容器 中的反应一定达到了平衡 中的反应一定达到了平衡 |
您最近一年使用:0次
名校
2 . 工业上以CO2和NH3为原料合成尿素,在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1
H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1
反应Ⅱ:H2NCOONH4(s) CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;
CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ∆H3
CO(NH2)2(s)+H2O(g) ∆H3
(1)反应Ⅰ的熵变ΔS___________  填“
填“ ”“
”“ ”或“
”或“ ”
” 。反应Ⅲ的
。反应Ⅲ的 H3=
H3=___________ ,反应Ⅲ自发进行的条件是___________ (填“低温”、“高温”、“任何温度”)。
(2)下列关于尿素合成的说法正确的是___________。
(3)1mol CO(NH2)2(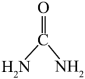 )中含有
)中含有___________ molπ键。NH 离子的VSEPR模型是
离子的VSEPR模型是___________ ,空间构型是___________ 。
(4)对于尿素分子中N、O两种基态原子,下列说法正确的是___________。
反应Ⅰ:2NH3(g)+CO2(g)
 H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1
H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272kJ·mol -1反应Ⅱ:H2NCOONH4(s)
 CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;
CO(NH2)2(s)+H2O(g) ΔH2=+138kJ·mol-1;总反应Ⅲ:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ∆H3
CO(NH2)2(s)+H2O(g) ∆H3(1)反应Ⅰ的熵变ΔS
 填“
填“ ”“
”“ ”或“
”或“ ”
” 。反应Ⅲ的
。反应Ⅲ的 H3=
H3=(2)下列关于尿素合成的说法正确的是___________。
| A.及时分离出尿素可促使反应Ⅱ向正反应方向移动 |
| B.从合成塔出来的混合气体分离出水蒸气后其余气体可以循环使用 |
| C.保持容积不变,充入惰性气体增大压强,可提高总反应Ⅲ的反应速率 |
| D.保持压强不变,降低氨碳比[n(NH3)/n(CO2)]可提高反应Ⅰ中NH3的平衡转化率 |
 )中含有
)中含有 离子的VSEPR模型是
离子的VSEPR模型是(4)对于尿素分子中N、O两种基态原子,下列说法正确的是___________。
| A.N的半径较小 | B.N的未成对电子数较多 |
| C.N的电负性较大 | D.N的第一电离能较高 |
您最近一年使用:0次
3 . 氨氧化法是工业制硝酸的常见方法。
第一步:合成氨。
(1)传统方法:在恒温恒容的密闭容器中,进行如下化学反应: ,对该反应的条件进行探究,下列实验措施与结论正确对应的是___________(填字母)。
,对该反应的条件进行探究,下列实验措施与结论正确对应的是___________(填字母)。
(2)铁基循环制氨:如图所示,工作时,使用熔融的电解质通过两步循环实现氨的合成,该工艺合成氨的化学方程式为___________ 。 的微观示意图如图所示,其中电解液为溶有三氟甲硝酸锂和乙醇的惰性有机溶剂。电极上生成
的微观示意图如图所示,其中电解液为溶有三氟甲硝酸锂和乙醇的惰性有机溶剂。电极上生成 的电极反应式为
的电极反应式为___________ 。
(4)氨催化氧化生成 后,
后, 氧化生成
氧化生成 的总反应为
的总反应为 ,可分两步进行,其反应过程中的能量变化示意图如图所示:
,可分两步进行,其反应过程中的能量变化示意图如图所示: .
.
 .
.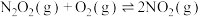
决定 氧化反应速率的步骤是
氧化反应速率的步骤是___________ (填“ ”或“
”或“ ”)。
”)。
(5)已知: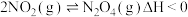 ,将一定物质的量的
,将一定物质的量的 充入某恒容密闭容器中,测得不同温度下
充入某恒容密闭容器中,测得不同温度下 和
和 的平衡体积分数如图所示:
的平衡体积分数如图所示: 的曲线是
的曲线是___________ (填“ ”或“
”或“ ”)。
”)。
②假设平衡时体系的总压为 ,则A点温度下的平衡常数
,则A点温度下的平衡常数
___________ (用含 的表达式表示),
的表达式表示), 的平衡转化率
的平衡转化率
___________ (保留3位有效数字)。
第三步;硝酸的制备。
(6)已知: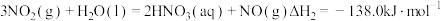 ,则
,则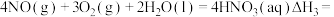
___________  。
。
第一步:合成氨。
(1)传统方法:在恒温恒容的密闭容器中,进行如下化学反应:
 ,对该反应的条件进行探究,下列实验措施与结论正确对应的是___________(填字母)。
,对该反应的条件进行探究,下列实验措施与结论正确对应的是___________(填字母)。| A.通过更换不同种类的催化剂,可以调节平衡时原料的转化率 |
| B.反应装置保持在相对较低的温度下,将有利于该反应的自发进行 |
| C.在反应过程中任意时刻移除部分产物,都可以使反应正向进行,但该反应的平衡常数保持不变 |
D.当检测到装置内的 保持不变时,不一定能说明反应已经达到平衡状态 保持不变时,不一定能说明反应已经达到平衡状态 |
(2)铁基循环制氨:如图所示,工作时,使用熔融的电解质通过两步循环实现氨的合成,该工艺合成氨的化学方程式为
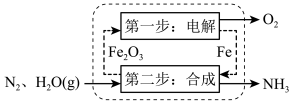
 的微观示意图如图所示,其中电解液为溶有三氟甲硝酸锂和乙醇的惰性有机溶剂。电极上生成
的微观示意图如图所示,其中电解液为溶有三氟甲硝酸锂和乙醇的惰性有机溶剂。电极上生成 的电极反应式为
的电极反应式为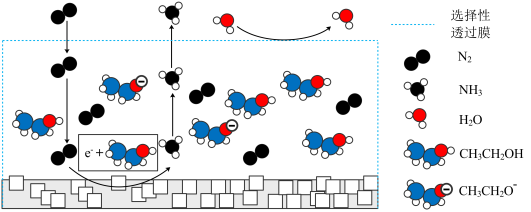
(4)氨催化氧化生成
 后,
后, 氧化生成
氧化生成 的总反应为
的总反应为 ,可分两步进行,其反应过程中的能量变化示意图如图所示:
,可分两步进行,其反应过程中的能量变化示意图如图所示: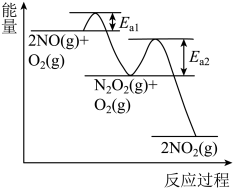
 .
.
 .
.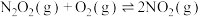
决定
 氧化反应速率的步骤是
氧化反应速率的步骤是 ”或“
”或“ ”)。
”)。(5)已知:
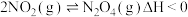 ,将一定物质的量的
,将一定物质的量的 充入某恒容密闭容器中,测得不同温度下
充入某恒容密闭容器中,测得不同温度下 和
和 的平衡体积分数如图所示:
的平衡体积分数如图所示: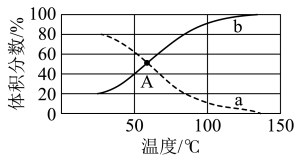
 的曲线是
的曲线是 ”或“
”或“ ”)。
”)。②假设平衡时体系的总压为
 ,则A点温度下的平衡常数
,则A点温度下的平衡常数
 的表达式表示),
的表达式表示), 的平衡转化率
的平衡转化率
第三步;硝酸的制备。
(6)已知:
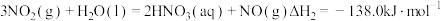 ,则
,则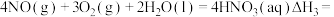
 。
。
您最近一年使用:0次
2024-08-21更新
|
51次组卷
|
2卷引用:贵州省贵州大学附属中学2023-2024学年高二下学期7月期末考试化学试卷
4 . Ⅰ.中国科学家首次实现了二氧化碳到淀粉的全合成,相关成果由国际知名学术期刊《科学》在线发表。 的捕集、利用与封存是科学家研究的重要课题,利用
的捕集、利用与封存是科学家研究的重要课题,利用 与
与 制备“合成气”
制备“合成气” 、
、 ,合成气可直接制备甲醇,反应原理为:
,合成气可直接制备甲醇,反应原理为: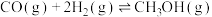
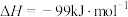
(1)若要该反应自发进行,_____ (填“高温”或“低温”)更有利。
(2)在恒温,恒容密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是_____ (填字母序号)。
A.反应物的物质的量的比值不变
B.混合气体的密度不再变化
C. 的百分含量不再变化
的百分含量不再变化
D.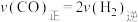
E.混合气体的平均相对分子质量不再变化
(3)把 转化为
转化为 是降碳并生产化工原料的常用方法,有关反应如下:
是降碳并生产化工原料的常用方法,有关反应如下:
①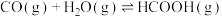
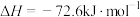
②

③
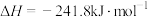
则 与
与 合成
合成 反应的热化学方程式:
反应的热化学方程式:_____
(4)受绿色植物光合作用的启示,太阳能固碳装置被设计出来,则固碳电极反应为_____ 。
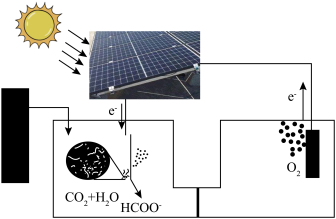
Ⅱ.我国学者结合实验与计算机模拟结果,研究了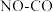 的反应历程。在催化剂作用下,此反应为
的反应历程。在催化剂作用下,此反应为  l可有效降低汽车尾气污染物排放。
l可有效降低汽车尾气污染物排放。
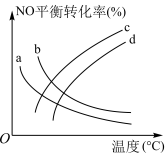
(5)探究温度、压强(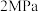 ,
,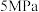 )对反应
)对反应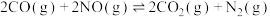 的影响,如图所示,表示
的影响,如图所示,表示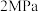 的是
的是_____ (填标号)。
(6)一定温度下,向一容积为1L的恒容密闭容器按体积3∶2比例充入CO和NO,压强为5MPa发生上述反应,当反应达到平衡时容器内压强变为起始时的 ,此温度下该反应的平衡常数
,此温度下该反应的平衡常数 =
=_____ ( 为压强平衡常数)。
为压强平衡常数)。
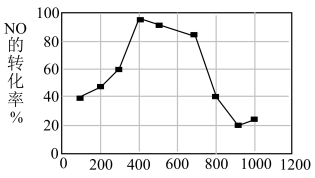
(7)若在相同时间内测得NO的转化率随温度的变化曲线如图,解释NO的转化率随温度的升高由上升到下降、下降由缓到急的主要原因是_____ 。
 的捕集、利用与封存是科学家研究的重要课题,利用
的捕集、利用与封存是科学家研究的重要课题,利用 与
与 制备“合成气”
制备“合成气” 、
、 ,合成气可直接制备甲醇,反应原理为:
,合成气可直接制备甲醇,反应原理为: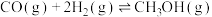
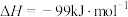
(1)若要该反应自发进行,
(2)在恒温,恒容密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是
A.反应物的物质的量的比值不变
B.混合气体的密度不再变化
C.
 的百分含量不再变化
的百分含量不再变化D.
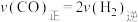
E.混合气体的平均相对分子质量不再变化
(3)把
 转化为
转化为 是降碳并生产化工原料的常用方法,有关反应如下:
是降碳并生产化工原料的常用方法,有关反应如下:①
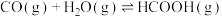
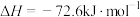
②


③

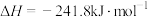
则
 与
与 合成
合成 反应的热化学方程式:
反应的热化学方程式:(4)受绿色植物光合作用的启示,太阳能固碳装置被设计出来,则固碳电极反应为

Ⅱ.我国学者结合实验与计算机模拟结果,研究了
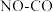 的反应历程。在催化剂作用下,此反应为
的反应历程。在催化剂作用下,此反应为  l可有效降低汽车尾气污染物排放。
l可有效降低汽车尾气污染物排放。(5)探究温度、压强(
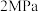 ,
,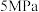 )对反应
)对反应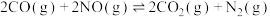 的影响,如图所示,表示
的影响,如图所示,表示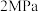 的是
的是
(6)一定温度下,向一容积为1L的恒容密闭容器按体积3∶2比例充入CO和NO,压强为5MPa发生上述反应,当反应达到平衡时容器内压强变为起始时的
 ,此温度下该反应的平衡常数
,此温度下该反应的平衡常数 =
= 为压强平衡常数)。
为压强平衡常数)。
(7)若在相同时间内测得NO的转化率随温度的变化曲线如图,解释NO的转化率随温度的升高由上升到下降、下降由缓到急的主要原因是
您最近一年使用:0次
5 . 含氮化合物是化工、能源、环保等领域的研究热点。
(1)工业上常用NH3和CO2合成尿素[CO(NH2)2],利用该反应可以在一定程度上减缓温室效应。该反应可分两步进行,其能量变化和反应历程如图所示___________ ;
②合成尿素总反应自发进行的条件是___________ (填“高温”或“低温”)。
(2)一定温度下,将NH3和CO2按2:1的物质的量之比充入一容积恒为10L的密闭容器中发生总反应。15min时达到平衡,各物质的浓度变化曲线如图所示。___________ g min﹣1。
min﹣1。
②下列叙述中能说明该反应达到平衡状态的是___________ (填选项字母)。
A.体系压强不再变化
B.NH3和CO2的浓度之比为2:1
C.气体平均摩尔质量不再变化
D.NH3的消耗速率和CO2的消耗速率之比为2:1
③25min时再向容器中充入2mol的NH3、1molCO2和2molH2O,则此时平衡___________ (填“正向移动”或“逆向移动”),再次平衡时总反应的平衡常数为 ___________ 。
(3)汽车尾气已成为许多大城市空气的主要污染源,其中存在大量NO。中国科学家在以H2为还原剂清除NO的研究方面取得了显著成果,其化学方程式为2NO(g)+2H2(g)⇌N2(g)+2H2O(g) ΔH<0。当固定比例的NO(g)和H2(g)的混合气体,以相同流速分别通过填充有两种催化剂的反应器,测得NO的转化率与温度的关系如图所示。___________ 。
②M、N、P、Q四点中一定未达到平衡状态的是___________ (填字母)。
(1)工业上常用NH3和CO2合成尿素[CO(NH2)2],利用该反应可以在一定程度上减缓温室效应。该反应可分两步进行,其能量变化和反应历程如图所示

②合成尿素总反应自发进行的条件是
(2)一定温度下,将NH3和CO2按2:1的物质的量之比充入一容积恒为10L的密闭容器中发生总反应。15min时达到平衡,各物质的浓度变化曲线如图所示。

 min﹣1。
min﹣1。②下列叙述中能说明该反应达到平衡状态的是
A.体系压强不再变化
B.NH3和CO2的浓度之比为2:1
C.气体平均摩尔质量不再变化
D.NH3的消耗速率和CO2的消耗速率之比为2:1
③25min时再向容器中充入2mol的NH3、1molCO2和2molH2O,则此时平衡
(3)汽车尾气已成为许多大城市空气的主要污染源,其中存在大量NO。中国科学家在以H2为还原剂清除NO的研究方面取得了显著成果,其化学方程式为2NO(g)+2H2(g)⇌N2(g)+2H2O(g) ΔH<0。当固定比例的NO(g)和H2(g)的混合气体,以相同流速分别通过填充有两种催化剂的反应器,测得NO的转化率与温度的关系如图所示。
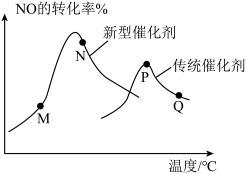
②M、N、P、Q四点中一定未达到平衡状态的是
您最近一年使用:0次
2024-04-24更新
|
301次组卷
|
2卷引用:广东省广州市五校(省实、广雅、执信、二中、六中)2023-2024学年高二上学期期末联考化学试题
解题方法
6 . 合成气(CO+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品。
(1)煤化工中生产合成气的反应为:C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.5kJ·mol-1
CO(g)+H2(g) ΔH=+131.5kJ·mol-1
①判断该反应的自发性条件___________ ;
②在恒温恒容下,同时放入C(s)、H2O(g)、CO(g)、H2(g)四种物质,下列事实能够说明反应C(s)+H2O(g) CO(g)+H2(g)已达到平衡的是
CO(g)+H2(g)已达到平衡的是___________ 。
A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有2molH—O键断裂的同时有1molH—H键断裂
D.混合气体的平均相对分子质量保持不变
(2)天然气化工中生产合成气的主要反应为:2CH4(g)+O2(g) 2CO(g)+4H2(g) ΔH=akJ·mol-1,在恒容容器中按物质的量之比1︰2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
2CO(g)+4H2(g) ΔH=akJ·mol-1,在恒容容器中按物质的量之比1︰2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
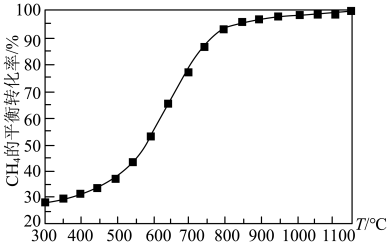
①请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线________ 。
②现有实验测得反应2CH4(g)+O2(g) 2CO(g)+4H2(g)在750℃下,以不同碳氧比[n(CH4)/n(O2)]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示。(已知:选择性=目标产物的产率/反应原料的转化率)
2CO(g)+4H2(g)在750℃下,以不同碳氧比[n(CH4)/n(O2)]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示。(已知:选择性=目标产物的产率/反应原料的转化率)
最佳碳氧比[n(CH4)/n(O2)]为___________ 。
(1)煤化工中生产合成气的反应为:C(s)+H2O(g)
 CO(g)+H2(g) ΔH=+131.5kJ·mol-1
CO(g)+H2(g) ΔH=+131.5kJ·mol-1①判断该反应的自发性条件
②在恒温恒容下,同时放入C(s)、H2O(g)、CO(g)、H2(g)四种物质,下列事实能够说明反应C(s)+H2O(g)
 CO(g)+H2(g)已达到平衡的是
CO(g)+H2(g)已达到平衡的是A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有2molH—O键断裂的同时有1molH—H键断裂
D.混合气体的平均相对分子质量保持不变
(2)天然气化工中生产合成气的主要反应为:2CH4(g)+O2(g)
 2CO(g)+4H2(g) ΔH=akJ·mol-1,在恒容容器中按物质的量之比1︰2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
2CO(g)+4H2(g) ΔH=akJ·mol-1,在恒容容器中按物质的量之比1︰2加入一定量的CH4和O2,在压强为1.01×105Pa、不同温度下测得CH4的平衡转化率如图所示:
①请在图中画出压强为5.05×105Pa时CH4的平衡转化率随温度的变化曲线
②现有实验测得反应2CH4(g)+O2(g)
 2CO(g)+4H2(g)在750℃下,以不同碳氧比[n(CH4)/n(O2)]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示。(已知:选择性=目标产物的产率/反应原料的转化率)
2CO(g)+4H2(g)在750℃下,以不同碳氧比[n(CH4)/n(O2)]投料时反应达平衡后CH4的转化率及H2、CO的选择性,所测数据如表所示。(已知:选择性=目标产物的产率/反应原料的转化率)| 碳氧比[n(CH4)/n(O2)] | 1︰0.25 | 1︰0.5 | 1︰1 | 1︰1.25 |
| CH4转化率 | 0.40 | 0.88 | 0.98 | 0.99 |
| H2选择性 | 0.98 | 0.93 | 0.67 | 0.40 |
| CO选择性 | 0.99 | 0.94 | 0.65 | 0.32 |
您最近一年使用:0次
名校
7 . 合成氨工艺是人工固氮最重要的途径。回答下列问题:
(1)工业合成氨的反应为 。在容积为2L的密闭容器中,通入amolN2和bmolH2,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN2.
。在容积为2L的密闭容器中,通入amolN2和bmolH2,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN2.
①该反应的平衡常数表达式
_____ 。
②达到平衡时,H2的转化率为_____ 。
③在tmin内以NH3的浓度变化表示的化学反应速率为_____ 。
④若把容器的容积缩小一半,则正反应速率_____ (填“增大”、“减小”或“不变”,下同),N2的转化率_____ 。
(2)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:
 。铜氨液吸收CO适宜的生产条件是
。铜氨液吸收CO适宜的生产条件是_____ 。
(3)合成氨工业中采用循环操作,主要是为了_____ (填序号)。
a.增大化学反应速率b.提高平衡混合物中氨的含量
c.降低氨的沸点d.提高氮气和氢气的利用率
(4)合成氨气的氢气可由天然气制备。
①其反应为
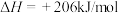 ,该反应自发的条件是
,该反应自发的条件是_____ (填“低温自发”、“高温自发”或“任意温度自发”)。
②为提高CH4的平衡转化率,可采用的措施是_____ (填序号)。
a.使用合适的催化剂b.采用较高的温度
c.采用较高的压强d.延长反应时间
(1)工业合成氨的反应为
 。在容积为2L的密闭容器中,通入amolN2和bmolH2,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN2.
。在容积为2L的密闭容器中,通入amolN2和bmolH2,若在一定条件下tmin后反应达到平衡,平衡后容器中剩余cmolN2.①该反应的平衡常数表达式

②达到平衡时,H2的转化率为
③在tmin内以NH3的浓度变化表示的化学反应速率为
④若把容器的容积缩小一半,则正反应速率
(2)在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经过铜氨液处理,目的是除去其中的CO,其反应为:

 。铜氨液吸收CO适宜的生产条件是
。铜氨液吸收CO适宜的生产条件是(3)合成氨工业中采用循环操作,主要是为了
a.增大化学反应速率b.提高平衡混合物中氨的含量
c.降低氨的沸点d.提高氮气和氢气的利用率
(4)合成氨气的氢气可由天然气制备。
①其反应为

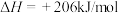 ,该反应自发的条件是
,该反应自发的条件是②为提高CH4的平衡转化率,可采用的措施是
a.使用合适的催化剂b.采用较高的温度
c.采用较高的压强d.延长反应时间
您最近一年使用:0次
2023-11-26更新
|
208次组卷
|
2卷引用:天津市南开区2023-2024学年高二上学期11月期中考试化学试题
解题方法
8 . “碳中和”目标如期实现的关键技术之一是 的再资源化利用。
的再资源化利用。
(1)氨的饱和食盐水捕获 是其利用的方法之一,反应原理为:
是其利用的方法之一,反应原理为: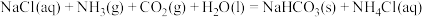 。该反应常温下能自发进行的原因是
。该反应常温下能自发进行的原因是___________ 。
(2)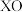 基掺杂
基掺杂 形成
形成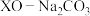 (
(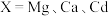 等),能用于捕获
等),能用于捕获 ,原理如下图所示。已知阳离子电荷数越高、半径越小,阴离子越易受其影响而分解。
,原理如下图所示。已知阳离子电荷数越高、半径越小,阴离子越易受其影响而分解。
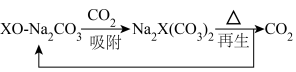
①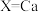 时,再生的化学方程式为
时,再生的化学方程式为___________ 。
②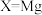 相比
相比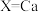 ,其优点有
,其优点有___________ 。
(3)催化电解吸收 的
的 溶液可将
溶液可将 转化为有机物。
转化为有机物。
① 在阴极放电生成
在阴极放电生成 的电极反应式为
的电极反应式为___________ 。
②碱性溶液有利于抑制阴极上副产物的产生,该副产物的化学式为___________ 。
(4)在催化剂作用下,以 和
和 为原料合成
为原料合成 ,主要反应为:
,主要反应为:
反应Ⅰ: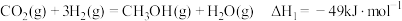
反应Ⅱ:
保持压强 ,将起始
,将起始 的混合气体匀速通过装有催化剂的反应管,测得出口处
的混合气体匀速通过装有催化剂的反应管,测得出口处 的转化率和甲醇的选择性
的转化率和甲醇的选择性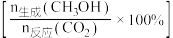 与温度的关系如题图1、题图2所示。
与温度的关系如题图1、题图2所示。
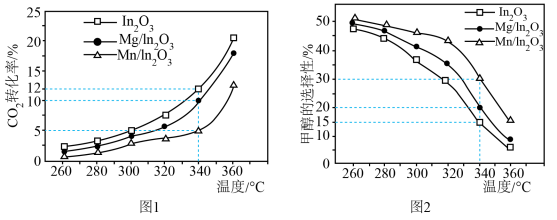
①随着温度的升高, 转化率增大、但甲醇选择性降低的原因是
转化率增大、但甲醇选择性降低的原因是___________ 。
②假设定义催化剂催化效率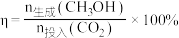 ,计算
,计算 时三种催化剂的催化效率之比
时三种催化剂的催化效率之比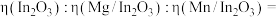
___________ (写出计算过程)。
 的再资源化利用。
的再资源化利用。(1)氨的饱和食盐水捕获
 是其利用的方法之一,反应原理为:
是其利用的方法之一,反应原理为: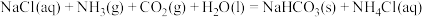 。该反应常温下能自发进行的原因是
。该反应常温下能自发进行的原因是(2)
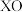 基掺杂
基掺杂 形成
形成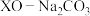 (
(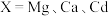 等),能用于捕获
等),能用于捕获 ,原理如下图所示。已知阳离子电荷数越高、半径越小,阴离子越易受其影响而分解。
,原理如下图所示。已知阳离子电荷数越高、半径越小,阴离子越易受其影响而分解。
①
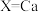 时,再生的化学方程式为
时,再生的化学方程式为②
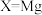 相比
相比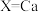 ,其优点有
,其优点有(3)催化电解吸收
 的
的 溶液可将
溶液可将 转化为有机物。
转化为有机物。①
 在阴极放电生成
在阴极放电生成 的电极反应式为
的电极反应式为②碱性溶液有利于抑制阴极上副产物的产生,该副产物的化学式为
(4)在催化剂作用下,以
 和
和 为原料合成
为原料合成 ,主要反应为:
,主要反应为:反应Ⅰ:
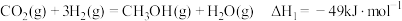
反应Ⅱ:

保持压强
 ,将起始
,将起始 的混合气体匀速通过装有催化剂的反应管,测得出口处
的混合气体匀速通过装有催化剂的反应管,测得出口处 的转化率和甲醇的选择性
的转化率和甲醇的选择性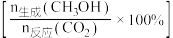 与温度的关系如题图1、题图2所示。
与温度的关系如题图1、题图2所示。
①随着温度的升高,
 转化率增大、但甲醇选择性降低的原因是
转化率增大、但甲醇选择性降低的原因是②假设定义催化剂催化效率
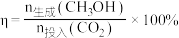 ,计算
,计算 时三种催化剂的催化效率之比
时三种催化剂的催化效率之比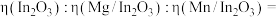
您最近一年使用:0次
2024-02-11更新
|
676次组卷
|
3卷引用:四川省宜宾市叙州区第二中学校2023-2024学年高二上学期1月期末化学试题
名校
9 . 甲醇是重要的化工原料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,相关反应的热化学方程式为:
ⅰ.CO(g)+2H2(g) CH3OH(g) ΔH=a kJ/mol;
CH3OH(g) ΔH=a kJ/mol;
ⅱ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=b kJ/mol;
CH3OH(g)+H2O(g) ΔH=b kJ/mol;
ⅲ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH=−c kJ/mol。
CO(g)+H2O(g) ΔH=−c kJ/mol。
回答下列问题:
(1)a=______ (用b、c表示),已知反应ⅱ在一定条件下可自发进行,则b______ (填“>”“<”或“=”)0。
(2)在一定温度下,向体积为1L的恒容密闭容器中通入等物质的量的CO2与H2,在催化剂的作用下仅发生反应ⅲ。该反应达到平衡时,其他条件不变,通入CO2时,则v(正)___ (填“>”“<”或“=”)v(逆),平衡常数_______ (填“变大”“变小”或“不变”)。
(3)一定温度下,向体积为2L的恒容密闭容器中通入CO、H2、CH3OH,发生反应ⅰ,其中X、Y的物质的量与时间的关系如图所示,反应进行1min时三种物质的体积分数均相等。
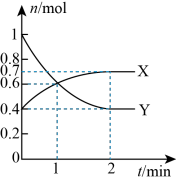
①Y为_____ (填化学式)。
②0~1min时v(CO)为_____ mol/(L·min)。
③该温度下,该反应的平衡常数Kc=______ 。
(4)工业上以 和
和 为原料可制备合成气(CO、H2),已知
为原料可制备合成气(CO、H2),已知 、
、 、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应
、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应

______ 。若该反应的 ,
, (
(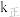 、
、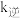 为速率常数,只与温度有关),平衡后降低温度,则
为速率常数,只与温度有关),平衡后降低温度,则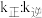
_______ (填“增大”“不变”或“减小”)。
(5)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式Q=cm△T计算获得。
①热量的测定:取0.5000mol/LNaOH溶液和0.5500mol/L盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,(c和 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
_____  。
。
②下列操作会使所测得的焓变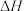 偏小的是
偏小的是______ 。
a.用等物质的量浓度的醋酸代替盐酸实验 b.量热装置绝热效果欠佳 c.NaOH溶液量多了
ⅰ.CO(g)+2H2(g)
 CH3OH(g) ΔH=a kJ/mol;
CH3OH(g) ΔH=a kJ/mol;ⅱ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=b kJ/mol;
CH3OH(g)+H2O(g) ΔH=b kJ/mol;ⅲ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=−c kJ/mol。
CO(g)+H2O(g) ΔH=−c kJ/mol。回答下列问题:
(1)a=
(2)在一定温度下,向体积为1L的恒容密闭容器中通入等物质的量的CO2与H2,在催化剂的作用下仅发生反应ⅲ。该反应达到平衡时,其他条件不变,通入CO2时,则v(正)
(3)一定温度下,向体积为2L的恒容密闭容器中通入CO、H2、CH3OH,发生反应ⅰ,其中X、Y的物质的量与时间的关系如图所示,反应进行1min时三种物质的体积分数均相等。
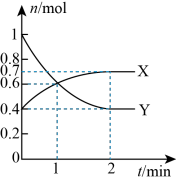
①Y为
②0~1min时v(CO)为
③该温度下,该反应的平衡常数Kc=
(4)工业上以
 和
和 为原料可制备合成气(CO、H2),已知
为原料可制备合成气(CO、H2),已知 、
、 、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应
、CO的燃烧热分别为890 kJ/mol、285kJ/mol、283kJ/mol,则反应

 ,
, (
(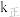 、
、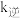 为速率常数,只与温度有关),平衡后降低温度,则
为速率常数,只与温度有关),平衡后降低温度,则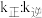
(5)化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式Q=cm△T计算获得。
①热量的测定:取0.5000mol/LNaOH溶液和0.5500mol/L盐酸各50mL进行反应,测得反应前后体系的温度值(℃)分别为T0、T1,(c和
 分别取
分别取 和
和 ,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
,忽略水以外各物质吸收的热量,后同),则该实验测得中和热
 。
。②下列操作会使所测得的焓变
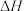 偏小的是
偏小的是a.用等物质的量浓度的醋酸代替盐酸实验 b.量热装置绝热效果欠佳 c.NaOH溶液量多了
您最近一年使用:0次
名校
10 . 以 为原料合成
为原料合成 涉及的反应如下:
涉及的反应如下:
I.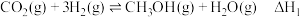
Ⅱ.
Ⅲ.
回答下列问题:
(1)计算反应I的
___________  ,该反应在
,该反应在___________ (填“高温”、“低温”或“任意温度”)下能自发。
(2)在 下,按照
下,按照 投料,假设只发生反应I和Ⅱ,平衡时,
投料,假设只发生反应I和Ⅱ,平衡时, 和
和 在含碳产物物质的量分数及
在含碳产物物质的量分数及 的转化率随温度的变化如图:
的转化率随温度的变化如图:
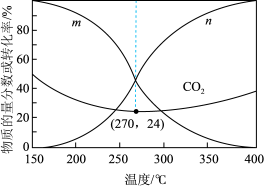
①图中代表 的曲线为
的曲线为___________ (填“m”或“n”)。
②解释 范围内
范围内 转化率随温度升高而降低的原因
转化率随温度升高而降低的原因___________ 。
③下列说法正确的是___________ (填字母)。
A.温度越高,越有利于工业生产
B.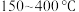 范围内,温度升高,
范围内,温度升高, 的平衡产量先减小后增大
的平衡产量先减小后增大
C.随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回起始的状态
④已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ;则
;则 时
时 的分压为
的分压为___________  (用最简分数),反应II的平衡常数
(用最简分数),反应II的平衡常数 为
为___________ (列出算式即可)。
 为原料合成
为原料合成 涉及的反应如下:
涉及的反应如下:I.
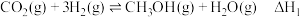
Ⅱ.

Ⅲ.

回答下列问题:
(1)计算反应I的

 ,该反应在
,该反应在(2)在
 下,按照
下,按照 投料,假设只发生反应I和Ⅱ,平衡时,
投料,假设只发生反应I和Ⅱ,平衡时, 和
和 在含碳产物物质的量分数及
在含碳产物物质的量分数及 的转化率随温度的变化如图:
的转化率随温度的变化如图:
①图中代表
 的曲线为
的曲线为②解释
 范围内
范围内 转化率随温度升高而降低的原因
转化率随温度升高而降低的原因③下列说法正确的是
A.温度越高,越有利于工业生产

B.
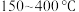 范围内,温度升高,
范围内,温度升高, 的平衡产量先减小后增大
的平衡产量先减小后增大C.随着温度逐渐升高,混合气体的平均相对分子质量几乎又变回起始的状态
④已知气体分压=气体总压×气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
 ;则
;则 时
时 的分压为
的分压为 (用最简分数),反应II的平衡常数
(用最简分数),反应II的平衡常数 为
为
您最近一年使用:0次
2024-03-02更新
|
141次组卷
|
2卷引用:安徽省六安第一中学2023-2024学年高二上学期期末考试化学试题



