1 . 关于水的离子积常数 ,溶液的酸碱性,下列说法错误的是
,溶液的酸碱性,下列说法错误的是
 ,溶液的酸碱性,下列说法错误的是
,溶液的酸碱性,下列说法错误的是| A.pH<7的溶液一定显酸性 |
B.25℃时,在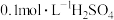 溶液中的 溶液中的 |
C. 的溶液一定呈中性 的溶液一定呈中性 |
D.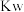 值随温度升高而增大 值随温度升高而增大 |
您最近一年使用:0次
名校
2 . 下列溶液一定显酸性的是
A.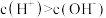 | B.含有 | C. | D.酚酞变红 |
您最近一年使用:0次
2021-01-22更新
|
244次组卷
|
6卷引用:内蒙古呼伦贝尔市满洲里远方中学2023-2024学年高二上学期第三次考试化学试卷
3 . 水的电离平衡曲线如下图所示,下列说法不正确的是
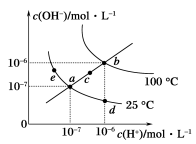

| A.图中五点Kw间的关系:b>c>a=d=e |
| B.若从a点到d点,可采用在水中加入少量酸的方法 |
| C.若从a点到c点,可采用温度不变时在水中加入适量NH4Cl固体的方法 |
| D.若处在b点时,将pH=2的硫酸与pH=10的KOH等体积混合后,溶液显中性 |
您最近一年使用:0次
2021-01-06更新
|
556次组卷
|
31卷引用:2015-2016学年内蒙古赤峰二中高二上学期期末化学试卷
2015-2016学年内蒙古赤峰二中高二上学期期末化学试卷内蒙古呼和浩特市土默特左旗第一中学2019-2020学年高二上学期第二次月考化学试题(已下线)2011届河北省正定中学高三上学期第三次考试化学试卷(已下线)2011届宁夏银川二中高三第一次模拟考试试题(理综)化学部分(已下线)2011届江西省赣县中学高三适应性考试(理科)化学部分(已下线)2012届黑龙江省大庆市第三十五中学高三期中考试化学试卷(已下线)2014年高考化学苏教版总复习 8-2 溶液的酸碱性练习卷(已下线)2013-2014江苏省盐城中学第二学期期中考试高二化学试卷(已下线)2014届黑龙江哈尔滨市第六中学高二上学期期中化学试卷(已下线)2014届江苏省盐城中学第二学期期中考试高二化学试卷(已下线)2015安徽望江中学同步课时练(人教选修4)3.2.2 pH的计算试卷2015届山东省肥城市高三二模理综化学试卷2015-2016学年浙江余姚中学高二上学期期中考试化学试卷2015-2016学年吉林省吉林五十五中高二上学期期中(理)化学试卷2016届重庆市育才中学高三下第一次月考理综化学试卷2016-2017学年青海师大附中高二上期中化学试卷2017届重庆市育才中学高三上12月考前测试化学卷安徽省安庆市第一中学2016-2017学年高二下学期期中考试化学试题河南省商丘市第一高级中学2017-2018学年高二10月月考化学试题河南省商丘市第一高级中学2017-2018学年高二上学期10月份月考化学试题湖北省咸丰县第一中学2017-2018学年高二上学期期中考试化学试题(已下线)2018年10月4日 《每日一题》一轮复习-水的电离及其影响因素河北省唐山市第一中学2018-2019学年高二上学期10月月考化学试题吉林省延边第二中学2019-2020学年高二上学期期中考化学(理)试题河北省石家庄外国语学校2019-2020学年高二上学期期末考试化学试题黑龙江省双鸭山市第一中学2020-2021学年高二上学期期中考试化学试题黑龙江省大庆中学2020-2021学年高二上学期期中考试化学试题江西省南昌市新建区第一中学2020-2021学年高二上学期第二次月考化学试题宁夏银川市长庆高级中学2020-2021学年高二上学期期末考试化学试题河南省宏力学校2020-2021学年高二上学期期末考试化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2021年高考化学临考题号押题(课标全国卷)
解题方法
4 . 室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
下列判断不正确的是
| 实验编号 | 起始浓度/( mol∙L−1) | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
| A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+) |
| B.0.1 mol·L−1HA的溶液中由水电离出的c(H+)=1×10−13mol·L−1 |
| C.实验②反应后的溶液中:c(A-)+c(HA)>0.1 mol·L−1 |
| D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+) |
您最近一年使用:0次
10-11高二上·黑龙江大庆·期中
名校
解题方法
5 . 将纯水加热至较高温度,下列叙述正确的是
A.水的离子积变大、pH变小、呈酸性 | B.水的离子积不变、pH不变、呈中性 |
C.水的离子积变小、pH变大、呈碱性 | D.水的离子积变大、pH变小、呈中性 |
您最近一年使用:0次
2020-11-25更新
|
839次组卷
|
73卷引用:2010—2011学年内蒙古赤峰二中高一下学期期末考试化学试卷
(已下线)2010—2011学年内蒙古赤峰二中高一下学期期末考试化学试卷2014-2015内蒙古满洲里市七中高二上学期第二次月考化学试卷2015-2016学年内蒙古赤峰市宁城县高二上学期期末考试化学试卷(已下线)2010年黑龙江大庆实验中学高二上学期期中考试化学试卷(已下线)2010年贵州册亨民族中学高二上学期期末考试化学卷(理)(已下线)2010—2011学年浙江省杭州师范大学附属中学高二下学期期中考试化学试卷(已下线)2010-2011学年辽宁省师大附中高二下学期期中考试化学试卷(已下线)2011—2012河北省南宫中学高二期中考试化学(理)试卷(已下线)2011-2012学年山东省沂南一中高二上学期期中模块学分认定考试化学试卷(已下线)2011-2012学年广东省培正中学高二上学期期中考试化学试卷(已下线)2011-2012学年天津市青光中学高二第一学期期末考试化学试卷(已下线)2011-2012学年海南省嘉积中学高二上学期教学质量监测三化学(理)试卷(已下线)2011-2012学年浙江省浙东北三校高二下学期期中联考化学试卷(已下线)2012-2013学年河南省河南大学附中高二上学期期中考试化学试卷(已下线)2013-2014学年贵州省册亨县民族中学高二上学期期末考试化学试卷(已下线)2014-2015学年吉林省汪清县第六中学高二上学期期中考试化学试卷(已下线)2014秋湖南省浏阳市第一中学高二上学期期中化学(理)试卷(已下线)2014-2015学年江西省景德镇市高二上学期期中化学(理)试卷2014-2015学年宁夏育才中学高二上学期期中化学试卷2014-2015湖南省怀化市中小学课改高二上学期期末化学试卷2014—2015陕西岐山县高二上学期期末考试化学(理)试卷2015-2016学年江西省铅山一中 、横峰中学高二上期中测试化学试卷2015-2016学年山东枣庄八中南校区高二12月月考化学卷2015-2016学年西藏日喀则中学高二上12月月考化学试卷2015-2016学年湖南省怀化市会同三中高二上12月月考化学试卷2015-2016学年安徽省亳州市高二上学期期末质检化学试卷2016-2017学年甘肃省武威二中高二上10月月考化学试卷2016-2017学年河北省秦皇岛北戴河中学高二上月考化学试卷2016-2017学年吉林省汪清六中高二上学期期中化学试卷黑龙江省大庆市大庆十中、二中、二十三中、二十八中2017-2018学年高二第一次联考化学试题河南省鹤壁市淇滨高级中学2017-2018学年高二上学期第二次月考化学试题广东省东莞市七校2017-2018学年高二上学期期中联考化学试题湖南省临武一中、嘉禾一中2017-2018学年高二12月联考化学试题湖北省襄阳市第四中学2017-2018学年高二12月月考化学试题河北省唐山一中2017-2018学年高二上学期12月月考化学试题贵州省毕节市实验高级中学2017-2018学年高二上学期期末考试化学试题河北省磁县滏滨中学2017-2018学年高二下学期期末考试化学试题【全国百强校】广西陆川县中学2017-2018学年高二下学期期末考试化学试题【全国百强校】山东省济南第一中学2018-2019学年高二上学期期中考试化学试题黑龙江省伊春市第二中学2019届高三上学期期中考试化学试题【全国百强校】安徽省铜陵市第一中学2018-2019学年高二上学期期中考试化学试题新疆自治区昌吉市第九中学2018-2019学年高二上学期第二次月考化学试题甘肃省岷县二中2018-2019学年高二上学期第三次月考化学试题上海市嘉定区封浜高中2018-2019学年高一第二学期期终考试化学试题陕西省吴起高级中学2019-2020学年高二上学期第一次月考(能力卷)化学试题陕西省吴起高级中学2019-2020学年高二上学期第一次月考(基础卷)化学试题河南省安阳市安阳县第一高级中学2019-2020学年高二上学期期中考试化学试题黑龙江省鸡西市鸡东县第二中学2019-2020学年高二上学期期中考试化学试题山西省太原市第五十三中学2019-2020学年高二上学期12月月考化学(理)试题宁夏银川市兴庆区长庆高级中学2019-2020学年高二上学期期末考试化学试题甘肃省永昌四中2019-2020学年高二上学期期末考试化学试题(已下线)上海市卢湾区2012届高三上学期期末考试化学试题新疆哈密市第十五中学2019-2020学年高二下学期期中考试化学试题云南省保山市第九中学2020-2021学年高二上学期质量检测化学试题上海市复旦大学附属中学2021届高三上学期第一次教学质量检测化学试题吉林省汪清县第六中学2020-2021学年高二上学期期中考试化学试题黑龙江省肇东市第四中学校2020-2021学年高二上学期期中考试化学试题河南省漯河市临颍县南街高中2020-2021学年高二上学期期中考试化学试题黑龙江省双鸭山市第一中学2020-2021学年高二第二次月考化学试题湖南省湘潭电机子弟中学2019-2020学年高二下学期期中考试化学(理)试题辽宁省盘锦市育才学校2020-2021学年高二下学期期初考试化学试题河南省宏力学校2020-2021学年高二上学期期末考试化学试题浙江省诸暨市2016-2017学年高二上学期期末考试化学试题 黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期期中考试化学试题河南省三门峡市渑池县第二高级中学2021-2022学年高二上学期第二次月考化学试题(已下线)3.2.1 水的电离和溶液的酸碱性-同步学习必备知识北京市清华大学附属中学2022-2023学年高二上学期12月月考化学试题陕西省西安市阎良区关山中学2022-2023学年高二上学期第三次质量检测化学试题山东省威海市文登新一中2021-2022学年高二上学期第一次阶段检测化学试题陕西省西安市高陵区第一中学2022-2023学年高二下学期开学考试化学试题四川省内江市第二中学2023-2024学年高二上学期期中考试化学试题陕西省宝鸡市扶风县法门高中2023-2024学年高二上学期期末考试化学试题陕西省宝鸡市扶风县法门高中2023-2024学年高二上学期期中考试化学试题
名校
解题方法
6 . 下列说法中正确的是
A.当溶液中存在的离子只有Cl−、OH−、 、H+时,该溶液中离子浓度大小关系可能为c(Cl−)>c( 、H+时,该溶液中离子浓度大小关系可能为c(Cl−)>c( )>c(OH−)>c(H+) )>c(OH−)>c(H+) |
B.常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c( )、c(H+)均下降 )、c(H+)均下降 |
C.常温下,c( )相等的①(NH4)2SO4②(NH4)2Fe(SO4)2③NH4Cl ④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ )相等的①(NH4)2SO4②(NH4)2Fe(SO4)2③NH4Cl ④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ |
D.常温下,pH=8.3的NaHCO3溶液:c(Na+)>c( )>c( )>c( )>c(H2CO3) )>c(H2CO3) |
您最近一年使用:0次
2020-11-24更新
|
1216次组卷
|
4卷引用:内蒙古翁牛特旗乌丹第二中学、呼和浩特市第二十一中学2017-2018学年高二上学期期末联考化学试题
名校
解题方法
7 . 实验室中有一未知浓度的稀盐酸,某学生用0.10 mol·L-1 NaOH标准溶液进行测定盐酸的浓度的实验。取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。完成下列填空:
I.(1)滴定达到终点的标志是_________ 。
(2)根据上述数据,可计算出该盐酸的浓度约为___________ (保留小数点后3位)。
(3)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有___________ 。
A.用酸式滴定管取20.00 mL待测盐酸,使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体时,有小部分NaOH潮解
D.滴定终点读数时俯视
E.碱式滴定管尖嘴部分有气泡,滴定后消失
Ⅱ.硼酸(H3BO3)是生产其它硼化物的基本原料。已知H3BO3的电离常数为5.8×10-10,H2CO3的电离常数为K1=4.4×10-7、K2=4.7×10-11。向盛有饱和硼酸溶液的试管中,滴加0.1 mol/LNa2CO3溶液,____________ (填“能”或“不能”)观察到气泡逸出。
Ⅲ.某温度时测得0.01 mol/L的NaOH溶液pH为11,求该温度下水的离子积常数KW =_________
| 实验编号 | 待测盐酸的体积(mL) | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) |
| 1 | 20.00 | 0.10 | 24.18 |
| 2 | 20.00 | 0.10 | 23.06 |
| 3 | 20.00 | 0.10 | 22.96 |
(2)根据上述数据,可计算出该盐酸的浓度约为
(3)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有
A.用酸式滴定管取20.00 mL待测盐酸,使用前,水洗后未用待测盐酸润洗
B.锥形瓶水洗后未干燥
C.称量NaOH固体时,有小部分NaOH潮解
D.滴定终点读数时俯视
E.碱式滴定管尖嘴部分有气泡,滴定后消失
Ⅱ.硼酸(H3BO3)是生产其它硼化物的基本原料。已知H3BO3的电离常数为5.8×10-10,H2CO3的电离常数为K1=4.4×10-7、K2=4.7×10-11。向盛有饱和硼酸溶液的试管中,滴加0.1 mol/LNa2CO3溶液,
Ⅲ.某温度时测得0.01 mol/L的NaOH溶液pH为11,求该温度下水的离子积常数KW =
您最近一年使用:0次
名校
解题方法
8 . 在不同温度下的水溶液中,c(H+)和c(OH-)的关系如图所示:
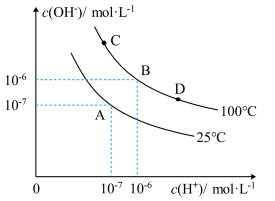
(1)A点水的离子积为________ ,C点水的离子积为_______ ,对纯水由25℃升高温度至100℃时水的离子积______ (填“增大”、“减小”或“不变”)。
(2)100℃时,若向B点溶液中滴加硫酸,体系将由B点移向_____ 点(填C或D),为什么_________ 。
(3)25℃时,0.001mol/L的盐酸溶液pH=_______ ;0.001mol/L的氢氧化钠溶液pH=_________ ;若将二者温度都升高至100℃,_________ (填“盐酸”、“氢氧化钠”、“盐酸和氢氧化钠”)的pH会改变。

(1)A点水的离子积为
(2)100℃时,若向B点溶液中滴加硫酸,体系将由B点移向
(3)25℃时,0.001mol/L的盐酸溶液pH=
您最近一年使用:0次
2020-11-14更新
|
702次组卷
|
4卷引用:内蒙古自治区乌兰察布市集宁一中(西校区)2020-2021学年高二上学期期中考试化学试题
内蒙古自治区乌兰察布市集宁一中(西校区)2020-2021学年高二上学期期中考试化学试题(已下线)第三章 水溶液中的离子反应与平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)(已下线)第三单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)新疆喀什地区疏附县第一中学2022-2023学年高二上学期期末考试化学试题
解题方法
9 . 已知水的电离平衡曲线如图示,试回答下列问题:
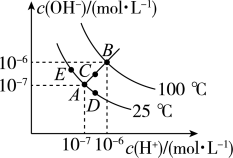
(1)图中五点Kw间的关系是_________ 。
(2)若从A点到D点,可采用的措施是_________ 。
A 升温 B 加入少量的盐酸 C 加入少量的NH4Cl
(3)B对应温度下,将pH=11的苛性钠溶液V1 L与0.05mol/L的稀硫酸V2L 混合(设混合前后溶液的体积不变),所得混合溶液的pH=2,则 V1∶V2=__________ 。
(4)常温下,将V mL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L-1醋酸溶液中充分反应。如果溶液pH=7,此时V的取值___________ 20.00(填“>”“<”或“=”)(忽略溶液体积的变化)。而溶液 中c(Na+)、c(CH3COO-)、c(H+)、c(OH-)的大小关系为___________ 。
(5)在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=____________ mol·L-1。(Ksp[Cu(OH)2]=2.2×10-20)

(1)图中五点Kw间的关系是
(2)若从A点到D点,可采用的措施是
A 升温 B 加入少量的盐酸 C 加入少量的NH4Cl
(3)B对应温度下,将pH=11的苛性钠溶液V1 L与0.05mol/L的稀硫酸V2L 混合(设混合前后溶液的体积不变),所得混合溶液的pH=2,则 V1∶V2=
(4)常温下,将V mL、0.1000mol·L-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol·L-1醋酸溶液中充分反应。如果溶液pH=7,此时V的取值
(5)在0.10 mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=
您最近一年使用:0次
解题方法
10 . 某温度下,水的离子积常数Kw=1×10-12。该温度下,将pH=4的H2SO4溶液与pH=9的NaOH溶液混合并保持恒温,忽略溶液体积变化。欲使混合溶液的pH=6,则稀硫酸与NaOH溶液的体积比为( )
| A.1:10 | B.9:1 | C.1:9 | D.10:1 |
您最近一年使用:0次
2020-11-12更新
|
545次组卷
|
3卷引用:内蒙古自治区第二地质中学2023-2024学年高二上学期12月期中考试化学试题
内蒙古自治区第二地质中学2023-2024学年高二上学期12月期中考试化学试题成都市实验外国语学校(西区)2020-2021学年高二上学期化学学科期中测试卷(已下线)第三章 水溶液中的离子反应与平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)



