名校
解题方法
1 . 在菠菜等植物中含有丰富的草酸,草酸对生命活动有重要影响。
 溶液的pH,溶液中的
溶液的pH,溶液中的 、
、 、
、 的物质的量分数
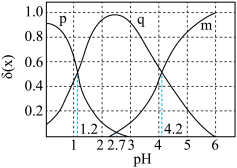
的物质的量分数 随pH的变化如图所示
随pH的变化如图所示
(1)草酸( )在水中的电离方程式:
)在水中的电离方程式:_______ 。
(2)要使溶液中草酸的电离程度增大,采取的措施为_______ 。(写两点)
(3)草酸溶液中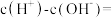
_______ 。(用含碳微粒表示)
(4)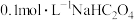 溶液中
溶液中
_______  。(填“<”“>”“=”)
。(填“<”“>”“=”)
(5) 时,
时,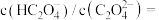
_______ 。
(6)为测定某实验样品中 的含量。称量mg样品,溶于水,加硫酸酸化,配成250mL溶液。取25.00mL于锥形瓶,用
的含量。称量mg样品,溶于水,加硫酸酸化,配成250mL溶液。取25.00mL于锥形瓶,用 标准液滴定,平均消耗vmL。
标准液滴定,平均消耗vmL。
① 与
与 反应的离子方程式:
反应的离子方程式:_______ 。
②滴定终点的现象:_______ 。
③样品中 的质量分数为
的质量分数为_______ 。(用含c,v,m字母表示)

 溶液的pH,溶液中的
溶液的pH,溶液中的 、
、 、
、 的物质的量分数
的物质的量分数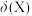 随pH的变化如图所示
随pH的变化如图所示
(1)草酸(
 )在水中的电离方程式:
)在水中的电离方程式:(2)要使溶液中草酸的电离程度增大,采取的措施为
(3)草酸溶液中
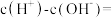
(4)
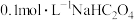 溶液中
溶液中
 。(填“<”“>”“=”)
。(填“<”“>”“=”)(5)
 时,
时,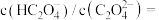
(6)为测定某实验样品中
 的含量。称量mg样品,溶于水,加硫酸酸化,配成250mL溶液。取25.00mL于锥形瓶,用
的含量。称量mg样品,溶于水,加硫酸酸化,配成250mL溶液。取25.00mL于锥形瓶,用 标准液滴定,平均消耗vmL。
标准液滴定,平均消耗vmL。①
 与
与 反应的离子方程式:
反应的离子方程式:②滴定终点的现象:
③样品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2023-04-15更新
|
310次组卷
|
2卷引用:福建省福州格致中学2022-2023学年高二下学期期中考试化学试题
名校
2 . 回答下列问题
(1) 催化释氢。在催化剂作用下,
催化释氢。在催化剂作用下, 与水反应生成
与水反应生成 ,可能的反应机理如图所示:
,可能的反应机理如图所示:

①其他条件不变时,以 代替
代替 催化释氢,所得气体的分子式为
催化释氢,所得气体的分子式为___________ 。
②已知: 为一元弱酸,
为一元弱酸, 水溶液呈酸性的原因是
水溶液呈酸性的原因是___________ (用离子方程式表示)。
(2)将 和
和 以一定的流速分别通过甲、乙两种催化剂进行反应,相同时间内测量逸出气体中
以一定的流速分别通过甲、乙两种催化剂进行反应,相同时间内测量逸出气体中 含量,从而确定尾气脱氮率(即
含量,从而确定尾气脱氮率(即 的转化率),结果如图所示,a点
的转化率),结果如图所示,a点___________ (填“是”或“不是”)平衡状态,原因是___________ 。

(3)氨是重要的基础化工产品之一,在一定条件下,向某反应容器中投入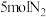 、
、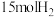 在不同温度下反应生成
在不同温度下反应生成 ,平衡体系中
,平衡体系中 的质量分数随压强变化曲线如图所示:
的质量分数随压强变化曲线如图所示:

①温度 、
、 、
、 中,最大的是
中,最大的是___________ ,M点 的转化率为
的转化率为___________ 。
②1939年捷姆金和佩热夫推出氨合成反应在接近平衡时净速率方程式为 ,
, 、
、 分别为正反应和逆反应的速率常数;
分别为正反应和逆反应的速率常数;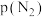 、
、 、
、 代表各组分的分压(分压=总压×物质的量分数);a是常数,工业上以铁为催化剂时,
代表各组分的分压(分压=总压×物质的量分数);a是常数,工业上以铁为催化剂时,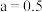 ,由M点数据计算
,由M点数据计算
___________ 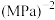 (保留两位有效数字)。
(保留两位有效数字)。
(1)
 催化释氢。在催化剂作用下,
催化释氢。在催化剂作用下, 与水反应生成
与水反应生成 ,可能的反应机理如图所示:
,可能的反应机理如图所示:
①其他条件不变时,以
 代替
代替 催化释氢,所得气体的分子式为
催化释氢,所得气体的分子式为②已知:
 为一元弱酸,
为一元弱酸, 水溶液呈酸性的原因是
水溶液呈酸性的原因是(2)将
 和
和 以一定的流速分别通过甲、乙两种催化剂进行反应,相同时间内测量逸出气体中
以一定的流速分别通过甲、乙两种催化剂进行反应,相同时间内测量逸出气体中 含量,从而确定尾气脱氮率(即
含量,从而确定尾气脱氮率(即 的转化率),结果如图所示,a点
的转化率),结果如图所示,a点
(3)氨是重要的基础化工产品之一,在一定条件下,向某反应容器中投入
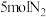 、
、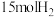 在不同温度下反应生成
在不同温度下反应生成 ,平衡体系中
,平衡体系中 的质量分数随压强变化曲线如图所示:
的质量分数随压强变化曲线如图所示:
①温度
 、
、 、
、 中,最大的是
中,最大的是 的转化率为
的转化率为②1939年捷姆金和佩热夫推出氨合成反应在接近平衡时净速率方程式为
 ,
, 、
、 分别为正反应和逆反应的速率常数;
分别为正反应和逆反应的速率常数;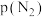 、
、 、
、 代表各组分的分压(分压=总压×物质的量分数);a是常数,工业上以铁为催化剂时,
代表各组分的分压(分压=总压×物质的量分数);a是常数,工业上以铁为催化剂时,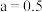 ,由M点数据计算
,由M点数据计算
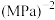 (保留两位有效数字)。
(保留两位有效数字)。
您最近一年使用:0次
名校
解题方法
3 . 草酸( )是一种常见的二元弱酸,常温下的电离常数为
)是一种常见的二元弱酸,常温下的电离常数为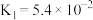 ,
,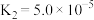 ,其盐草酸钠(
,其盐草酸钠(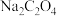 )可作血液抗凝剂。请回答下列问题。(已知
)可作血液抗凝剂。请回答下列问题。(已知 )
)
(1)常温下,向0.1 mol/L的 溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示,图中Y点对应的pH为
溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示,图中Y点对应的pH为_______ 。

(2)常温下HF的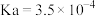 ,等体积的1 mol/L HF与0.5 mol/L
,等体积的1 mol/L HF与0.5 mol/L 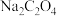 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为_______ 。
(3)在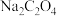 溶液中,下列关系正确的是_______。
溶液中,下列关系正确的是_______。
(4)现有一瓶含草酸钠的血液抗凝剂样品,某化学课外兴趣小组设计如下实验方案测定样品中草酸钠的含量(假设杂质都不与酸性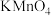 溶液反应)。
溶液反应)。
①样品溶液配制:准确称取4.00 g样品,加入10 mL蒸馏水和30 mL 4 mol/L硫酸溶液溶解,冷却后转入250 mL容量瓶中,定容;
②滴定:准确量取25.00 mL样品溶液于锥形瓶中,利用0.020 mol/L酸性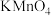 溶液进行滴定、达到滴定终点时,记录相关数据。重复滴定操作两次;
溶液进行滴定、达到滴定终点时,记录相关数据。重复滴定操作两次;
③计算:相关实验数据如下表:
①酸性高锰酸钾与草酸钠反应的离子方程式为_______ 。
②此样品中草酸钠的质量分数为_______ 。
 )是一种常见的二元弱酸,常温下的电离常数为
)是一种常见的二元弱酸,常温下的电离常数为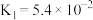 ,
,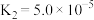 ,其盐草酸钠(
,其盐草酸钠(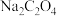 )可作血液抗凝剂。请回答下列问题。(已知
)可作血液抗凝剂。请回答下列问题。(已知 )
)(1)常温下,向0.1 mol/L的
 溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示,图中Y点对应的pH为
溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示,图中Y点对应的pH为
(2)常温下HF的
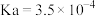 ,等体积的1 mol/L HF与0.5 mol/L
,等体积的1 mol/L HF与0.5 mol/L 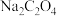 溶液发生反应的离子方程式为
溶液发生反应的离子方程式为(3)在
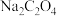 溶液中,下列关系正确的是_______。
溶液中,下列关系正确的是_______。A.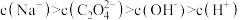 |
B.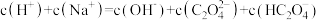 |
C.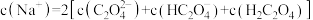 |
D.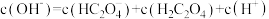 |
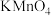 溶液反应)。
溶液反应)。①样品溶液配制:准确称取4.00 g样品,加入10 mL蒸馏水和30 mL 4 mol/L硫酸溶液溶解,冷却后转入250 mL容量瓶中,定容;
②滴定:准确量取25.00 mL样品溶液于锥形瓶中,利用0.020 mol/L酸性
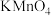 溶液进行滴定、达到滴定终点时,记录相关数据。重复滴定操作两次;
溶液进行滴定、达到滴定终点时,记录相关数据。重复滴定操作两次;③计算:相关实验数据如下表:
| 序号 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 0.10 | 20.00 |
| 2 | 1.20 | 21.30 |
| 3 | 0.40 | 18.90 |
②此样品中草酸钠的质量分数为
您最近一年使用:0次
名校
4 . 硒是人体所需微量元素之一,也是一种重要的工业原料。
Ⅰ.硒在元素周期表中的位置如图所示:
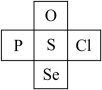
(1)从原子结构的角度解释硫的非金属性比硒强的原因是__ 。
Ⅱ.工业上从铜阳极泥(含有Se、Au、Ag、Cu、CuSe、Ag2Se等)中提取硒的过程如图:
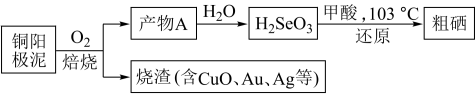
(2)焙烧时,产物A的化学式为__ 。
(3)将甲酸(HCOOH)还原H2SeO3反应的化学方程式补充完整:H2SeO3+2HCOOH Se+
Se+ +
+ 。
。______ 。
(4)常温下,H2SeO3电离平衡体系中含Se(+4价)微粒的物质的量分数与pH的关系如图所示。
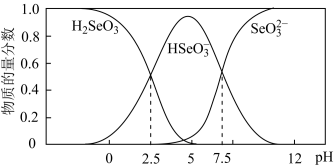
向亚硒酸溶液滴入氨水至pH=2.5,过程中主要反应的离子方程式__ 。
(5)还原时,进行了下述实验:向10mL2.5mol·L-1亚硒酸溶液中先加入10mL氨水,再加入10mL甲酸溶液(甲酸浓度分别为5、7.5及10mol·L-1),加热至沸腾(103℃),反应10小时,实验数据如图所示。
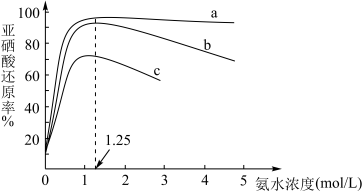
①曲线___ (填曲线字母编号)对应甲酸浓度为10mol·L-1,判断的理由是___ 。
②当氨水浓度在0~1.25mol·L-1之间,随着氨水浓度逐渐增大,亚硒酸还原率逐渐升高,其可能的原因是__ 。
(6)粗硒中硒含量测定:
在一定条件下,将0.1000g粗硒中的Se完全转化为H2SeO3溶液,用V1mL0.1000mol·L-1Na2S2O3溶液进行滴定。终点前加入KI淀粉溶液做指示剂,继续用V2mL0.1000mol·L-1Na2S2O3溶液滴定至溶液蓝色消失。发生的反应:
H2SeO3+4S2O +4H+=Se+2S4O
+4H+=Se+2S4O +3H2O
+3H2O ;
;
H2SeO3+4I-+4H+=Se+2I2+3H2O;
I2+2S2O =2I-+S4O
=2I-+S4O 。则粗硒中Se的质量分数为
。则粗硒中Se的质量分数为___ 。
Ⅰ.硒在元素周期表中的位置如图所示:

(1)从原子结构的角度解释硫的非金属性比硒强的原因是
Ⅱ.工业上从铜阳极泥(含有Se、Au、Ag、Cu、CuSe、Ag2Se等)中提取硒的过程如图:

(2)焙烧时,产物A的化学式为
(3)将甲酸(HCOOH)还原H2SeO3反应的化学方程式补充完整:H2SeO3+2HCOOH
 Se+
Se+ +
+ 。
。(4)常温下,H2SeO3电离平衡体系中含Se(+4价)微粒的物质的量分数与pH的关系如图所示。

向亚硒酸溶液滴入氨水至pH=2.5,过程中主要反应的离子方程式
(5)还原时,进行了下述实验:向10mL2.5mol·L-1亚硒酸溶液中先加入10mL氨水,再加入10mL甲酸溶液(甲酸浓度分别为5、7.5及10mol·L-1),加热至沸腾(103℃),反应10小时,实验数据如图所示。

①曲线
②当氨水浓度在0~1.25mol·L-1之间,随着氨水浓度逐渐增大,亚硒酸还原率逐渐升高,其可能的原因是
(6)粗硒中硒含量测定:
在一定条件下,将0.1000g粗硒中的Se完全转化为H2SeO3溶液,用V1mL0.1000mol·L-1Na2S2O3溶液进行滴定。终点前加入KI淀粉溶液做指示剂,继续用V2mL0.1000mol·L-1Na2S2O3溶液滴定至溶液蓝色消失。发生的反应:
H2SeO3+4S2O
 +4H+=Se+2S4O
+4H+=Se+2S4O +3H2O
+3H2O ;
;H2SeO3+4I-+4H+=Se+2I2+3H2O;
I2+2S2O
 =2I-+S4O
=2I-+S4O 。则粗硒中Se的质量分数为
。则粗硒中Se的质量分数为
您最近一年使用:0次
2021-04-19更新
|
325次组卷
|
3卷引用:北京市顺义区2021届高三第二次统练化学试题
北京市顺义区2021届高三第二次统练化学试题(已下线)押全国卷理综第27题 工业流程-备战2021年高考化学临考题号押题(课标全国卷)北京市第一七一中学2021-2022学年高三下学期开学考试化学试卷
解题方法
5 . 钪(Sc)可用于制造特种玻璃、轻质耐高温合金及半导体器件等,在航天,航空、核反应、医疗等方面有广泛应用。以制铝工业提取氧化铝时排出的废渣(含有Se2O3,Al2O3、Fe2O3、SiO2等)为原料提取氧化钪(Sc2O3)的流程如下:
②25℃时,Ka1(H2C2O4)=5.0×10-2、Ka2(H2C2O4)=5.0×10-5。
回答下列问题:
(1)废渣酸浸时,为了提高浸出率,可采取的措施有___________ (任写两条);浸渣的主要用途有___________ 。
(2)“萃取”时选用酸性磷酸酯(P507)为主的复合萃取剂,其中P507的质量分数(ω)对萃取率的影响如图1所示,料液温度对分离系数[分离系数指分离后混合体系中某物质的物质的量分数,如βSc/Fe= ×100%]的影响如图2所示:
×100%]的影响如图2所示:___________ ,料液的最适合温度为___________ 。
(3)一般认为c≤1.0×10-5mol/L时沉淀完全,已知lg2≈0.3,反萃取时,为了让Sc3+沉淀完全,应控制溶液pH的最小值为___________ 。
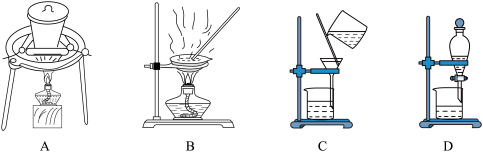
(4)在实验室中完成操作A和煅烧草酸钪晶体,所需装置分别为___________ (填字母)。___________ 。
(6)25℃时,pH=2的草酸溶液中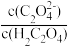 =
=___________ 。
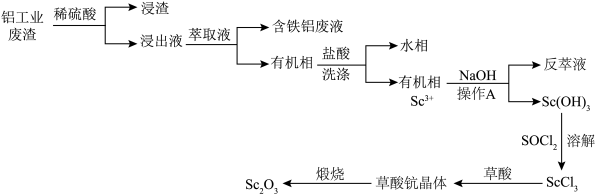
②25℃时,Ka1(H2C2O4)=5.0×10-2、Ka2(H2C2O4)=5.0×10-5。
回答下列问题:
(1)废渣酸浸时,为了提高浸出率,可采取的措施有
(2)“萃取”时选用酸性磷酸酯(P507)为主的复合萃取剂,其中P507的质量分数(ω)对萃取率的影响如图1所示,料液温度对分离系数[分离系数指分离后混合体系中某物质的物质的量分数,如βSc/Fe=
 ×100%]的影响如图2所示:
×100%]的影响如图2所示:
(3)一般认为c≤1.0×10-5mol/L时沉淀完全,已知lg2≈0.3,反萃取时,为了让Sc3+沉淀完全,应控制溶液pH的最小值为
(4)在实验室中完成操作A和煅烧草酸钪晶体,所需装置分别为
(6)25℃时,pH=2的草酸溶液中
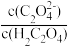 =
=
您最近一年使用:0次
6 . 回答下列问题:
(1)已知 时,水的离子积常数
时,水的离子积常数 ,该温度下测得
,该温度下测得 溶液的
溶液的 。则
。则
___________ 25℃(填“>”、“<”或“=”)。 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ 。
(2)已知氢氟酸、次氯酸、碳酸在室温下的电离常数分别为:
根据上述数据,回答下列问题:
①比较同浓度的 、
、 溶液的
溶液的 值大小:
值大小:
___________  。(填“>”、“<”或“=”)
。(填“>”、“<”或“=”)
②少量的 通入
通入 溶液中,写出反应的离子方程式
溶液中,写出反应的离子方程式___________ 。
(3)用氧化还原滴定方法测定粗品中Na2S2O3•5H2O的质量分数(Na2S2O3•5H2O的式量为248)。
实验步骤:称取6g粗品配制250mL的溶液待用。用酸式滴定管取25.00mL0.01mol•L-1K2Cr2O7溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的Na2S2O3溶液滴定至终点(反应为I2+2S2O =2I-+S4O
=2I-+S4O ),消耗Na2S2O3溶液25.00mL。
),消耗Na2S2O3溶液25.00mL。
回答下列问题:
①向K2Cr2O7溶液中加入过量的KI溶液并酸化,Cr2O 被还原成Cr3+,写出该反应的离子方程式:
被还原成Cr3+,写出该反应的离子方程式:___________ 。
②用Na2S2O3溶液滴定至终点的现象为___________ 。
③粗品中Na2S2O3•5H2O的质量分数为___________ 。
④若在取K2Cr2O7溶液时有部分溶液滴到了锥形瓶外。则测定结果______ (填“偏高”“偏低”或“不变”)。
(1)已知
 时,水的离子积常数
时,水的离子积常数 ,该温度下测得
,该温度下测得 溶液的
溶液的 。则
。则
 在水溶液中的电离方程式为
在水溶液中的电离方程式为(2)已知氢氟酸、次氯酸、碳酸在室温下的电离常数分别为:
 | 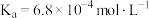 |
 |  |
 |   |
①比较同浓度的
 、
、 溶液的
溶液的 值大小:
值大小:
 。(填“>”、“<”或“=”)
。(填“>”、“<”或“=”)②少量的
 通入
通入 溶液中,写出反应的离子方程式
溶液中,写出反应的离子方程式(3)用氧化还原滴定方法测定粗品中Na2S2O3•5H2O的质量分数(Na2S2O3•5H2O的式量为248)。
实验步骤:称取6g粗品配制250mL的溶液待用。用酸式滴定管取25.00mL0.01mol•L-1K2Cr2O7溶液于锥形瓶中,然后加入过量的KI溶液并酸化,加几滴淀粉溶液,立即用配制的Na2S2O3溶液滴定至终点(反应为I2+2S2O
 =2I-+S4O
=2I-+S4O ),消耗Na2S2O3溶液25.00mL。
),消耗Na2S2O3溶液25.00mL。回答下列问题:
①向K2Cr2O7溶液中加入过量的KI溶液并酸化,Cr2O
 被还原成Cr3+,写出该反应的离子方程式:
被还原成Cr3+,写出该反应的离子方程式:②用Na2S2O3溶液滴定至终点的现象为
③粗品中Na2S2O3•5H2O的质量分数为
④若在取K2Cr2O7溶液时有部分溶液滴到了锥形瓶外。则测定结果
您最近一年使用:0次
7 . 钪的特殊性质,使其在电子工业、航天、核技术、激光技术、冶金、化工、医学、农业等各方面得到广泛应用。一种利用高温沸腾氯化烟尘(主要成分为AlCl3、FeCl3、TiCl4、ScCl3等,还含有其他难溶于酸的物质)回收Sc的工艺流程如图。

已知:钪(原子序数为21)与铝类似,其氢氧化物具有两性;钪离子可以在不同pH下生成[Sc(OH)n]3-n(n=1~6)。
请回答以下问题:
(1)某次实验中需要使用480mL3mol·L-1的盐酸,用浓盐酸(密度为1.2g·cm-3,质量分数为36.5%)配制实验所需要的盐酸,则需要量取浓盐酸的体积为_______ mL,需要使用的玻璃仪器除烧杯、量筒、玻璃棒外,还需要的是_______ 。
(2)钪的一种核素可用作示踪原子,用于对恶性肿瘤放射治疗,该种核素的中子数为25,则该核素的符号为_______ 。
(3)“反萃取”时,若加入的氢氧化钠溶液过量,则Sc(OH)3沉淀会溶解。写出Se(OH)3与过量NaOH溶液反应生成n=6的含钪产物的化学方程式:_______ 。
(4)加入草酸进行“沉淀转化”,将Sc(OH)3沉淀转化为Sc2(C2O4)3。25°C时pH=2的草酸溶液中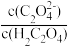 =
=_______ 。(25°C时,草酸的电离平衡常数为Ka1=5.0×10-2,Ka2=5.4×10-5)
(5)草酸钪在空气中“灼烧”可制得Sc2O3,写出反应的化学方程式:_______ 。
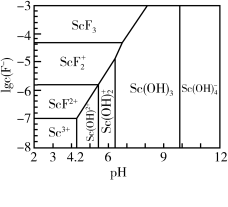
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[lgc(F-)、pH的关系如图所示。若溶液中c(F-)=1×10-5mol·L-1,“调pH”过程中控制pH=5,此时三价Sc的主要存在形式为_______ (填化学式)。

已知:钪(原子序数为21)与铝类似,其氢氧化物具有两性;钪离子可以在不同pH下生成[Sc(OH)n]3-n(n=1~6)。
请回答以下问题:
(1)某次实验中需要使用480mL3mol·L-1的盐酸,用浓盐酸(密度为1.2g·cm-3,质量分数为36.5%)配制实验所需要的盐酸,则需要量取浓盐酸的体积为
(2)钪的一种核素可用作示踪原子,用于对恶性肿瘤放射治疗,该种核素的中子数为25,则该核素的符号为
(3)“反萃取”时,若加入的氢氧化钠溶液过量,则Sc(OH)3沉淀会溶解。写出Se(OH)3与过量NaOH溶液反应生成n=6的含钪产物的化学方程式:
(4)加入草酸进行“沉淀转化”,将Sc(OH)3沉淀转化为Sc2(C2O4)3。25°C时pH=2的草酸溶液中
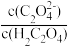 =
=(5)草酸钪在空气中“灼烧”可制得Sc2O3,写出反应的化学方程式:
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[lgc(F-)、pH的关系如图所示。若溶液中c(F-)=1×10-5mol·L-1,“调pH”过程中控制pH=5,此时三价Sc的主要存在形式为

您最近一年使用:0次
名校
解题方法
8 . 硒和碲是重要的稀散元素,都可以作为半导体材料。一种从碲碱渣(碲和硒的含量较高,还含有少量 、
、 等元素)分离硒回收碲的工艺流程如下:
等元素)分离硒回收碲的工艺流程如下: 、
、 及少量可溶性的铜、铅化合物等。
及少量可溶性的铜、铅化合物等。
② 为两性氧化物,微溶于水。
为两性氧化物,微溶于水。
③亚硒酸为二元弱酸,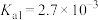 、
、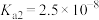
回答下列问题:
(1)硒与氧同族,基态 原子价电子排布式为
原子价电子排布式为___________ 。比较键角大小:
___________  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是___________ 。
(2)“除杂渣”的主要成分为___________ 。
(3)“中和”时控制 为
为 ,生成
,生成 沉淀,若硫酸过量,将导致
沉淀,若硫酸过量,将导致 的回收率下降的原因是
的回收率下降的原因是___________ 。
(4)“酸浸液”中硒主要以亚硒酸的形式存在。若控制“酸浸液”的 为2,此时溶液中
为2,此时溶液中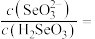
___________ 。
(5)“沉硒”时生成了一种无污染的单质气体,写出“沉硒”时发生的主要反应的化学方程式___________ 。
(6)一种以 和
和 为电极、
为电极、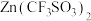 水溶液为电解质的电池,放电时,
水溶液为电解质的电池,放电时, 插入
插入 层间形成
层间形成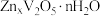 。写出该电池放电时正极的电极反应式
。写出该电池放电时正极的电极反应式___________ 。
 、
、 等元素)分离硒回收碲的工艺流程如下:
等元素)分离硒回收碲的工艺流程如下:
 、
、 及少量可溶性的铜、铅化合物等。
及少量可溶性的铜、铅化合物等。②
 为两性氧化物,微溶于水。
为两性氧化物,微溶于水。③亚硒酸为二元弱酸,
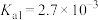 、
、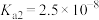
回答下列问题:
(1)硒与氧同族,基态
 原子价电子排布式为
原子价电子排布式为
 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是(2)“除杂渣”的主要成分为
(3)“中和”时控制
 为
为 ,生成
,生成 沉淀,若硫酸过量,将导致
沉淀,若硫酸过量,将导致 的回收率下降的原因是
的回收率下降的原因是(4)“酸浸液”中硒主要以亚硒酸的形式存在。若控制“酸浸液”的
 为2,此时溶液中
为2,此时溶液中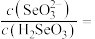
(5)“沉硒”时生成了一种无污染的单质气体,写出“沉硒”时发生的主要反应的化学方程式
(6)一种以
 和
和 为电极、
为电极、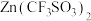 水溶液为电解质的电池,放电时,
水溶液为电解质的电池,放电时, 插入
插入 层间形成
层间形成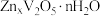 。写出该电池放电时正极的电极反应式
。写出该电池放电时正极的电极反应式
您最近一年使用:0次
2024-05-04更新
|
147次组卷
|
2卷引用:江西省新余市2024届高三下学期第二次模拟考试化学试题
9 . 实验室模拟拉希法用氨和次氯酸钠反应制备肼(N2H4),并探究肼的性质,制备装置如图所示。
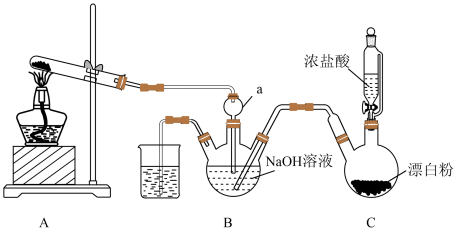
回答下列问题:
(1)肼的电子式为_______ 。
(2)装置A试管中的试剂为_______ 。
(3)装置B中制备肼的化学方程式为_______ 。
(4)上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是_______ 。
(5)①探究性质。
已知N2H4是一种二元弱碱,在水中的电离与NH3相似,请写出肼的第二步电离的电离方程式:_______ ,室温下向N2H4水溶液中滴加某强酸,溶液的pH与 或
或 的变化关系如图所示,下列说法正确的是
的变化关系如图所示,下列说法正确的是_______ (填标号)。

A.N2H4在水溶液中第二步电离的平衡常数为10-1
B. 的平衡常数为109
的平衡常数为109
C. 的水解能力大于其电离能力
的水解能力大于其电离能力
D.N2H6Cl2溶液中: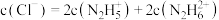
②测定产品中肼的质量分数。
称取装置B中溶液m g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH=6),加水配成100 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2~3滴指示剂,用c mol/L的碘标准溶液滴定,滴定过程中有无色无味无毒气体产生,定终点时平均消耗标准溶液V mL,产品中肼的质量分数为_______ (用含m、c、V的式子表示)。

回答下列问题:
(1)肼的电子式为
(2)装置A试管中的试剂为
(3)装置B中制备肼的化学方程式为
(4)上述装置中存在一处缺陷,会导致肼的产率降低,改进方法是
(5)①探究性质。
已知N2H4是一种二元弱碱,在水中的电离与NH3相似,请写出肼的第二步电离的电离方程式:
 或
或 的变化关系如图所示,下列说法正确的是
的变化关系如图所示,下列说法正确的是
A.N2H4在水溶液中第二步电离的平衡常数为10-1
B.
 的平衡常数为109
的平衡常数为109C.
 的水解能力大于其电离能力
的水解能力大于其电离能力D.N2H6Cl2溶液中:
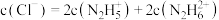
②测定产品中肼的质量分数。
称取装置B中溶液m g,加入适量NaHCO3固体(滴定过程中,调节溶液的pH=6),加水配成100 mL溶液,移取25.00 mL置于锥形瓶中,并滴加2~3滴指示剂,用c mol/L的碘标准溶液滴定,滴定过程中有无色无味无毒气体产生,定终点时平均消耗标准溶液V mL,产品中肼的质量分数为
您最近一年使用:0次
名校
解题方法
10 . 三氯氧磷( )可用作半导体掺杂剂。工业上采用直接氧化法由
)可用作半导体掺杂剂。工业上采用直接氧化法由 制备
制备 ,反应原理为:
,反应原理为: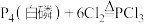 ,
, 。
。
已知: 、
、 的部分性质如下:
的部分性质如下:
某实验小组模拟该工艺设计实验装置如图(部分加热和夹持装置已略去):___________ 。
(2)装置乙的主要作用为:①干燥气体,②___________ ,③___________ 。
(3)装置丙的温度需控制在60-65°℃的原因是___________ 。
(4)提纯 (含少量杂质
(含少量杂质 ),可采用的方法是
),可采用的方法是___________ 。
(5) 遇水生成弱电解质亚磷酸
遇水生成弱电解质亚磷酸 ,已知
,已知 与过量NaOH反应生成
与过量NaOH反应生成 。
。
①写出 的电离方程式:
的电离方程式:___________ 。
② 溶液中,各离子浓度由大到小的顺序为
溶液中,各离子浓度由大到小的顺序为___________ 。
(6)通过测定三氯氧磷产品中Cl元素含量,可进一步计算产品的纯度,实验步骤如下:
I.取mg产品于锥形瓶中,加入足量NaOH溶液,待水解完全后滴加稀硝酸至酸性;
Ⅱ.向锥形瓶中加入 溶液至
溶液至 完全沉淀;
完全沉淀;
Ⅲ.向其中加入少量硝基苯,用力摇动,使沉淀表面被有机物覆盖;
Ⅳ.加入指示剂,用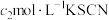 溶液进行滴定,至终点时消耗KSCN溶液
溶液进行滴定,至终点时消耗KSCN溶液 。
。
(已知: 溶于酸,AgSCN是白色沉淀;
溶于酸,AgSCN是白色沉淀;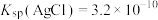 ,
,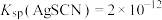 )
)
①步骤Ⅳ中选用的指示剂为___________ 。
A. B.
B. C.淀粉 D.甲基橙
C.淀粉 D.甲基橙
②产品中氯元素的百分含量表达式为:___________ 。
③下列操作会使测得的氯元素含量偏小的是___________ 。
A.配制 标准溶液时仰视容量瓶刻度线
标准溶液时仰视容量瓶刻度线
B.实验过程中未加入硝基苯
C.滴定前滴定管尖嘴处有气泡,滴定后无气泡
D.滴定时锥形瓶未干燥
 )可用作半导体掺杂剂。工业上采用直接氧化法由
)可用作半导体掺杂剂。工业上采用直接氧化法由 制备
制备 ,反应原理为:
,反应原理为: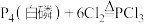 ,
, 。
。已知:
 、
、 的部分性质如下:
的部分性质如下:| 熔点/℃ | 沸点/℃ | 其它 | |
 | -112 | 75.5 |  和 和 互溶,均为无色液体,遇水均剧烈水解 互溶,均为无色液体,遇水均剧烈水解 |
 | 2 | 105.3 |
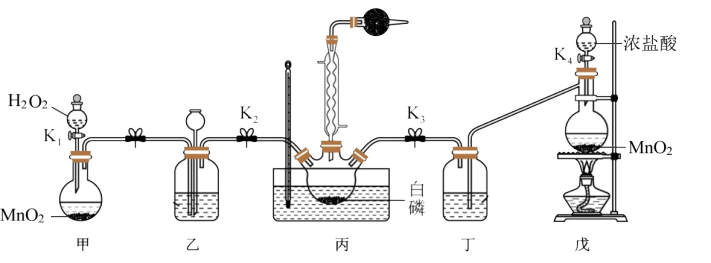
(2)装置乙的主要作用为:①干燥气体,②
(3)装置丙的温度需控制在60-65°℃的原因是
(4)提纯
 (含少量杂质
(含少量杂质 ),可采用的方法是
),可采用的方法是(5)
 遇水生成弱电解质亚磷酸
遇水生成弱电解质亚磷酸 ,已知
,已知 与过量NaOH反应生成
与过量NaOH反应生成 。
。①写出
 的电离方程式:
的电离方程式:②
 溶液中,各离子浓度由大到小的顺序为
溶液中,各离子浓度由大到小的顺序为(6)通过测定三氯氧磷产品中Cl元素含量,可进一步计算产品的纯度,实验步骤如下:
I.取mg产品于锥形瓶中,加入足量NaOH溶液,待水解完全后滴加稀硝酸至酸性;
Ⅱ.向锥形瓶中加入
 溶液至
溶液至 完全沉淀;
完全沉淀;Ⅲ.向其中加入少量硝基苯,用力摇动,使沉淀表面被有机物覆盖;
Ⅳ.加入指示剂,用
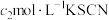 溶液进行滴定,至终点时消耗KSCN溶液
溶液进行滴定,至终点时消耗KSCN溶液 。
。(已知:
 溶于酸,AgSCN是白色沉淀;
溶于酸,AgSCN是白色沉淀;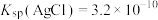 ,
,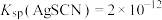 )
)①步骤Ⅳ中选用的指示剂为
A.
 B.
B. C.淀粉 D.甲基橙
C.淀粉 D.甲基橙②产品中氯元素的百分含量表达式为:
③下列操作会使测得的氯元素含量偏小的是
A.配制
 标准溶液时仰视容量瓶刻度线
标准溶液时仰视容量瓶刻度线B.实验过程中未加入硝基苯
C.滴定前滴定管尖嘴处有气泡,滴定后无气泡
D.滴定时锥形瓶未干燥
您最近一年使用:0次



