名校
解题方法
1 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
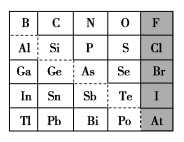
(1)元素 在元素周期表中的位置为第
在元素周期表中的位置为第______ 周期第______ 族。
(2) 的最高化合价为
的最高化合价为______ , 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为______ , 的最高价氧化物为
的最高价氧化物为______ 。
(3)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是______ 元素(填元素符号)。
②酸性:
______ (填“>”“<”或“=”,下同) 。
。
③氢化物的还原性:
______  。
。
④原子半径:
______  。
。
(4)可在图中分界线(虚线)附近寻找______ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料
(5)从下列试剂中选择最佳试剂组合,比较 、
、 的非金属性强弱:
的非金属性强弱:______ 。(可供选择的药品有 固体、稀硫酸、盐酸、饱和
固体、稀硫酸、盐酸、饱和 溶液、饱和
溶液、饱和 溶液、硅酸钠溶液)
溶液、硅酸钠溶液)

(1)元素
 在元素周期表中的位置为第
在元素周期表中的位置为第(2)
 的最高化合价为
的最高化合价为 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为 的最高价氧化物为
的最高价氧化物为(3)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是
②酸性:

 。
。③氢化物的还原性:

 。
。④原子半径:

 。
。(4)可在图中分界线(虚线)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料
(5)从下列试剂中选择最佳试剂组合,比较
 、
、 的非金属性强弱:
的非金属性强弱: 固体、稀硫酸、盐酸、饱和
固体、稀硫酸、盐酸、饱和 溶液、饱和
溶液、饱和 溶液、硅酸钠溶液)
溶液、硅酸钠溶液)
您最近一年使用:0次
2020-09-08更新
|
1584次组卷
|
6卷引用:安徽省芜湖市第二中学2023-2024学年高二上学期入学学情评价化学试题
名校
解题方法
2 . 下面是元素周期表的一部分,参照元素①~⑧在表中的位置。
请用化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)___________________ 。
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)_____________ 。
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:_____________________ 。
(4)由②最高价氧化物与⑤的同周期相邻主族元素的单质反应的化学方程式为:___________________________ 。
(5)②单质与③的最高价氧化物的水化物的浓溶液反应的离子方程式为______________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
请用化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为(元素符号)
(2)②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是(填化学式)
(3)在①、④、⑤、⑧中的某些元素之间可形成既含离子键又含非极性共价键的离子化合物,写出其中一种化合物的电子式:
(4)由②最高价氧化物与⑤的同周期相邻主族元素的单质反应的化学方程式为:
(5)②单质与③的最高价氧化物的水化物的浓溶液反应的离子方程式为
您最近一年使用:0次
2020-08-28更新
|
94次组卷
|
2卷引用:安徽省淮南市第一中学2019-2020学年高一下学期期末考试化学试题
名校
3 . 元素周期表的一部分如图所示。回答下列问题:
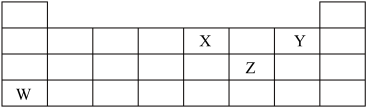
(1)X的原子结构示意图为____ ,其最简单氢化物的电子式为_____ 。
(2)Y 元素位于元素周期表中第_____ 周期_______ 族。
(3)Z、Y 最简单氢化物热稳定性由强到弱的顺序为________ (填化学式)。
(4)W 的最高价氧化物对应水化物的化学式为_____ ,该水化物中含有______ (填“共价键”、“离子键”)。
(5)用电子式表示 WY 的形成过程:__________ 。

(1)X的原子结构示意图为
(2)Y 元素位于元素周期表中第
(3)Z、Y 最简单氢化物热稳定性由强到弱的顺序为
(4)W 的最高价氧化物对应水化物的化学式为
(5)用电子式表示 WY 的形成过程:
您最近一年使用:0次
名校
4 . 下表是元素周期表的一部分,回答有关问题。

(1)写出元素符号:①___ ,⑥___ 。
(2)在这些元素中,最活泼的金属元素的原子结构示意图为___ 。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生反应的离子方程式为___ 。
(4)在②、③、④、⑤这些元素形成的最简单离子中,离子半径由大到小的顺序为___ (填离子符号)。
(5)由元素②、③、⑧形成的一种常见的杀菌消毒剂中存在的化学键有___ 。
(6)由元素⑦和⑧形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:___ 。

(1)写出元素符号:①
(2)在这些元素中,最活泼的金属元素的原子结构示意图为
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质在水溶液中发生反应的离子方程式为
(4)在②、③、④、⑤这些元素形成的最简单离子中,离子半径由大到小的顺序为
(5)由元素②、③、⑧形成的一种常见的杀菌消毒剂中存在的化学键有
(6)由元素⑦和⑧形成的某种化合物可表示为X2Y2(其中各原子均满足8电子稳定结构),写出X2Y2的电子式:
您最近一年使用:0次
2020-07-12更新
|
259次组卷
|
5卷引用:安徽省桐城中学2021-2022学年高二上学期综合测试化学试题
名校
解题方法
5 . 下表为元素周期表的一部分,请回答下列问题:
(1)元素③在元素周期表中的位置是_____________________ 。
(2)元素④和⑤的最高价氧化物对应水化物酸性较强的是____________ (填化学式),元素①和④中,原子半径较大的是__________ (填元素符号)。
(3)元素②的氢氧化物能溶于元素①的氢氧化物所形成的的溶液中,离子方程式为:______________________________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ③ | |||||||
| 3 | ① | ② | ④ | ⑤ | ||||
(1)元素③在元素周期表中的位置是
(2)元素④和⑤的最高价氧化物对应水化物酸性较强的是
(3)元素②的氢氧化物能溶于元素①的氢氧化物所形成的的溶液中,离子方程式为:
您最近一年使用:0次
名校
6 . 下表是元素周期表一部分,列出了九种元素在周期表中的位置:
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是____________ 。
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是________ (填物质化学式)。写出⑥和⑧的最高价氧化物对应的水化物反应的离子方程式 _______________________________ 。
(3)只由④形成的18电子微粒的电子式________________ 。
(4)写出由①和③形成的离子化合物的化学式____________________________ 。
(5)用电子式表示⑦和⑨形成的化合物的形成过程_________________________________ 。
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式_________________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(3)只由④形成的18电子微粒的电子式
(4)写出由①和③形成的离子化合物的化学式
(5)用电子式表示⑦和⑨形成的化合物的形成过程
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式
您最近一年使用:0次
2020-05-26更新
|
84次组卷
|
2卷引用:安徽省黄山市屯溪第一中学2019-2020学年高一下学期期中考试化学试题
名校
7 . 下表是元素周期表的一部分。
回答下列问题:
(1)元素①的名称是____ ,元素⑧的符号是____ 。
(2)在这些元素中,___ (用元素符号或化学式填写,下同)是最活泼的非金属元素,____ 是最不活泼的元素。
(3)这些元素的最高价氧化物对应的水化物中,____ 酸性最强,____ 碱性最强,具有两性的氢氧化物是____ 。
(4)比较⑤与⑥的化学性质,____ 更活泼,试用实验证明此结论(简述操作、现象和结论):________________________ 。
(5)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式是______________________________________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
回答下列问题:
(1)元素①的名称是
(2)在这些元素中,
(3)这些元素的最高价氧化物对应的水化物中,
(4)比较⑤与⑥的化学性质,
(5)⑦的最高价氧化物与⑤的最高价氧化物对应的水化物反应的离子方程式是
您最近一年使用:0次
名校
8 . 下图是元素周期表的一部分,针对表中的①~⑥元素,回答下列问题
(1)最活泼的金属元素是_______________ (填元素符号)
(2)②和⑤两种元素原子半径较大的是_______________ (填元素符号),⑤和⑥两种元素最高价氧化物对应的水合物酸性较强的是_____________ (填元素符号);
(3)写出①的单质在⑥的单质中燃烧的化学方程式_______________________________________ 。
| 主族 周期 | ⅠA | 0族 | ||||||
一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
二 | ② | |||||||
三 | ③ | ④ | ⑤ | ⑥ | ||||
(1)最活泼的金属元素是
(2)②和⑤两种元素原子半径较大的是
(3)写出①的单质在⑥的单质中燃烧的化学方程式
您最近一年使用:0次
2020-05-21更新
|
39次组卷
|
2卷引用:安徽省蚌埠田家炳中学2019-2020学年高一下学期开学学业检测化学试题
13-14高一·全国·课后作业
名校
9 . A、B两种元素,A的原子序数为x,A和B所在周期所含的元素种类分别是a和b。
(1)如果A和B同在ⅠA族,当A在B的上一周期时,B的原子序数为___________ ,当A在B的下一周期时,B的原子序数为___________ 。
(2)如果A和B同在ⅦA族,当A在B的上一周期时,B的原子序数为____________ ,当A在B的下一周期时,B的原子序数为____________ 。
(1)如果A和B同在ⅠA族,当A在B的上一周期时,B的原子序数为
(2)如果A和B同在ⅦA族,当A在B的上一周期时,B的原子序数为
您最近一年使用:0次
2020-05-14更新
|
244次组卷
|
8卷引用:安徽省阜阳三中2017-2018学年高一上学期第二次调研考试化学试题
安徽省阜阳三中2017-2018学年高一上学期第二次调研考试化学试题(已下线)2014年高一化学人教版必修二 1-1-1元素周期表练习卷吉林省长春市德惠市实验中学2018-2019学年高一下学期期初检测化学试题人教版高中化学必修二第一章《物质结构 元素周期律》测试卷苏教版高一化学必修2专题1《微观结构与物质的多样性》测试卷湖北省孝感市云梦县2019-2020高一下学期普通高中联考协作体线上考试化学试题(已下线)4.1.1 原子结构 元素周期表 核素练习(1)——《高中新教材同步备课》(人教版 必修第一册)(已下线)【精品卷】4.1.2 元素周期表课堂例题-人教版2023-2024学年必修第一册
解题方法
10 . 下表是元素周期表的一部分,回答相关的问题。
(1)写出④的元素符号__ 。
(2)在这些元素中,最活泼的金属元素与水反应的离子方程式:__ 。
(3)在这些元素中,最高价氧化物的水化物酸性最强的是__ (填相应化学式,下同),碱性最强的是__ 。
(4)这些元素中(除⑨外),原子半径最小的是__ (填元素符号,下同),原子半径最大的是__ 。
(5)②的单质与③的最高价氧化物的水化物的溶液反应,其产物之一是OX2,(O、X分别表示氧和②的元素符号,即OX2代表该化学式),该反应的离子方程式为(方程式中用具体元素符号表示)__ 。
(6)⑦的低价氧化物通入足量Ba(NO3)2溶液中的离子方程式__ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)写出④的元素符号
(2)在这些元素中,最活泼的金属元素与水反应的离子方程式:
(3)在这些元素中,最高价氧化物的水化物酸性最强的是
(4)这些元素中(除⑨外),原子半径最小的是
(5)②的单质与③的最高价氧化物的水化物的溶液反应,其产物之一是OX2,(O、X分别表示氧和②的元素符号,即OX2代表该化学式),该反应的离子方程式为(方程式中用具体元素符号表示)
(6)⑦的低价氧化物通入足量Ba(NO3)2溶液中的离子方程式
您最近一年使用:0次
2020-05-06更新
|
164次组卷
|
3卷引用:安徽省定远县育才学校2019-2020学年高一下学期4月月考化学试题



