1 . 联合国大会将2019年定为“国际化学元素周期表年” ,显示了元素周期律的重要性。下表列出了7种元素在周期表中的位置:
回答下列问题: 。
(1)⑦的元素符号是___________ ,③的原子结构示意图为___________ 。
(2)上述7种元素中,金属性最强的是___________ ( 填元素符号) ,最高价氧化物对应水化物具有两性的物质是___________ ( 填化学式)。
(3)用“>”、“<”、“=”填空。
(4)③的单质与②的简单氢化物反应的离子方程式为___________ ,
④的单质与③的最高价氧化物对应水化物反应的离子方程式___________ 。
(5)用电子式表示③和⑤形成化合物的过程___________ 。
| 周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | |||||
| 4 | ⑥ | ⑦ | ||||||
(1)⑦的元素符号是
(2)上述7种元素中,金属性最强的是
(3)用“>”、“<”、“=”填空。
| 类别 | 比较 |
| 简单氢化物稳定性 | ① |
| 简单离子半径 | ③ |
| 元素的非金属性 | ⑤ |
④的单质与③的最高价氧化物对应水化物反应的离子方程式
(5)用电子式表示③和⑤形成化合物的过程
您最近一年使用:0次
名校
2 . 铁、铝和铜是人类使用最广泛的金属。回答下列问题:
(1)根据电子排布的特点,Al位于元素周期表的__ (填标号,下同),Fe位于元素周期表的__ 。
a.s区 b.p区 c.d区 d.ds区
(2)63Cu和65Cu互称为__ ,在元素周期表中位于第__ 周期,基态Cu+的电子排布式为__ 。
(3)经研究发现目前铁的最高价为+6价,其+6价化合物Na2FeO4在硫酸存在的条件下,可将Mn2+氧化为MnO ,而自身被还原为Fe3+,该反应的离子方程式为
,而自身被还原为Fe3+,该反应的离子方程式为__ 。
(1)根据电子排布的特点,Al位于元素周期表的
a.s区 b.p区 c.d区 d.ds区
(2)63Cu和65Cu互称为
(3)经研究发现目前铁的最高价为+6价,其+6价化合物Na2FeO4在硫酸存在的条件下,可将Mn2+氧化为MnO
 ,而自身被还原为Fe3+,该反应的离子方程式为
,而自身被还原为Fe3+,该反应的离子方程式为
您最近一年使用:0次
2022-01-09更新
|
232次组卷
|
2卷引用:安徽省滁州市九校2021-2022学年高二下学期3月月考化学试题
2021高一·全国·专题练习
名校
3 . 下表是元素周期表的一部分,请用化学符号回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___________ 。
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是___________ ,最高价氧化物的水化物中酸性最强的是___________ 。
(3)第三周期元素形成的简单离子中半径最小的微粒是___________ ,写出该元素的单质分别与⑥、⑩最高价氧化物的水化物反应的离子方程式___________ 、___________ 。
| 主族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是
(3)第三周期元素形成的简单离子中半径最小的微粒是
您最近一年使用:0次
2021-12-06更新
|
1095次组卷
|
4卷引用:安徽省芜湖市第一中学2022-2023学年高一上学期选科分班考试化学试题
安徽省芜湖市第一中学2022-2023学年高一上学期选科分班考试化学试题(已下线)专题4.2.1 元素性质的周期性变化规律(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)浙江省舟山市舟山中学2021-2022学年高一下学期开学考试化学试题山东省“学情空间”区域教研共同体2022-2023学年高一上学期12月联考(人教版) 化学试题
解题方法
4 . 我国的食品添加剂有多种,如富硒(Se)酵母、二氧化硅、硫黄等,新品种食品添加剂的安全性需通过审查和测试,食品添加剂包括食品营养强化剂、风味改良剂、结构改善剂、防腐剂等,用于食品生产中能更好地满足吃货们的心愿,丰富舌尖上的营养和美味。请回答下列问题:
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为___________ ;普通玻璃的主要成分为二氧化硅,用氢氟酸蚀刻普通玻璃时,发生反应的化学方程式为___________ 。
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示(已知:a为非金属元素)。
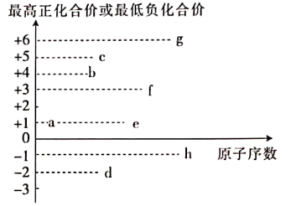
①由a、c、d三种元素形成的离子化合物的化学式为___________ 。
②图中所示元素中金属性最强的是___________ (填元素符号),工业上得到该元素的单质的原理为___________ (填化学方程式)。
③e、f、g元素的简单离子半径由大到小的顺序为___________ (用离子符号回答)。
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为___________ (填化学式)。
⑤a2d2可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,发生反应的离子方程式为___________ 。
(1)二氧化硅是一种新型添加剂,用作抗结剂。硅元素在元素周期表中的位置为
(2)食品添加剂中可能存在的部分短周期元素的最高正化合价或最低负化合价与原子序数的关系如图所示(已知:a为非金属元素)。

①由a、c、d三种元素形成的离子化合物的化学式为
②图中所示元素中金属性最强的是
③e、f、g元素的简单离子半径由大到小的顺序为
④低温下,h的单质与化合物eda的稀溶液的反应中的氧化产物为
⑤a2d2可用于处理碱性工业废水中的bc-,发生氧化还原反应,产物为一种酸根离子和常见的碱性气体,发生反应的离子方程式为
您最近一年使用:0次
2021-11-05更新
|
422次组卷
|
3卷引用:安徽省部分学校2021-2022学年高三上学期10月联考化学试题
安徽省部分学校2021-2022学年高三上学期10月联考化学试题河北省石家庄市保定市2022届高三10月月考化学试题(已下线)解密05 物质结构 元素周期律(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
名校
解题方法
5 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,如图是元素周期表的一部分,回答下列问题:
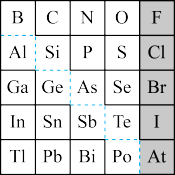
(1)元素Ga在元素周期表中的位置为:___ 。
(2)Sn的最高正价为___ ,Cl的最高价氧化物对应水化物的化学式为___ 。
(3)根据元素周期律,推断
①阴影部分元素形成的氢化物中热稳定性最高的是___ 。(写化学式)
②原子半径比较:N___ Si(填“>”、“<”、“=”或“无法比较”)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断
①阴影部分元素形成的氢化物中热稳定性最高的是
②原子半径比较:N
您最近一年使用:0次
名校
解题方法
6 . 下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①___________ ,⑦___________ 。
(2)画出原子的结构示意图:④___________ ,⑧___________ 。
(3)在①—⑫元素中,金属性最强的元素是___________ ,非金属性最强的元素是___________ ,最不活泼的元素是___________ 。(均填元素符号)
(4)元素⑦与元素⑧相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ 。
a.常温下⑦的单质和⑧的单质状态不同 b.⑧的氢化物比⑦的氢化物稳定 c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是___________ (填序号),跟它同周期原子半径最小的元素是___________ (填序号),它们可以形成 ___________ (填“离子”或“共价”)化合物,用电子式表示其形成过程如下:___________ 。
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,它可与⑧形成一种AB4型化合物,请写出该化合物的电子式:___________ 。
 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)画出原子的结构示意图:④
(3)在①—⑫元素中,金属性最强的元素是
(4)元素⑦与元素⑧相比,非金属性较强的是
a.常温下⑦的单质和⑧的单质状态不同 b.⑧的氢化物比⑦的氢化物稳定 c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,它可与⑧形成一种AB4型化合物,请写出该化合物的电子式:
您最近一年使用:0次
7 . 如表列出了A~R9种元素在周期表中的位置(用化学符号表示):

(1)这9种元素中化学性质最不活泼的是___ 。
(2)A、B、C三种元素按原子半径由大到小的顺序排列为___ 。
(3)写出A和D的最高价氧化物对应水化物之间反应的离子方程式___ 。
(4)G元素跟B元素形成化合物的电子式是___ 。
(5)G元素和H元素两者核电荷数之差是___ 。

(1)这9种元素中化学性质最不活泼的是
(2)A、B、C三种元素按原子半径由大到小的顺序排列为
(3)写出A和D的最高价氧化物对应水化物之间反应的离子方程式
(4)G元素跟B元素形成化合物的电子式是
(5)G元素和H元素两者核电荷数之差是
您最近一年使用:0次
解题方法
8 . 图是元素周期表的一部分,回答下列有关问题:
(1)写出⑫的元素符号:_______ ,其原子序数为_______ 。
(2)在这些元素中,非金属性最强的元素是_______ (用元素符号填答)。
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质反应的化学方程式_______ 。
(4)在④⑤⑦⑧形成的四个简单离子中,离子 半径由大到小的顺序是(用离子符号和“>”填答)_______
(5)设计一种简单实验确认④与⑤中,哪个金属性更强(只要写出实验方案即可),写出实验方案并预测结论:_______ ;
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | VⅡA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(1)写出⑫的元素符号:
(2)在这些元素中,非金属性最强的元素是
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的物质与碱性最强的物质反应的化学方程式
(4)在④⑤⑦⑧形成的四个简单离子中,
(5)设计一种简单实验确认④与⑤中,哪个金属性更强(只要写出实验方案即可),写出实验方案并预测结论:
您最近一年使用:0次
解题方法
9 . 下表列出了A~R 9种元素在周期表中的位置:
请回答下列问题。
(1)写出下列几种元素符号:B___________ ,D___________ ,H___________ ,R___________ 。9种元素中化学性质最不活泼的是___________ 。
(2)A与F形成的一种化合物可作供氧剂,写出该化合物作供氧剂时的反应原理:___________ 。
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是___________ 。
(4)A、B、C三种元素按原子半径由大到小的顺序排列为___________ 。
(5)H元素与A元素形成化合物的化学式是___________ ,高温灼烧该化合物时,火焰呈___________ 色。
| 周期 | 族 | |||||||
| Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
请回答下列问题。
(1)写出下列几种元素符号:B
(2)A与F形成的一种化合物可作供氧剂,写出该化合物作供氧剂时的反应原理:
(3)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是
(4)A、B、C三种元素按原子半径由大到小的顺序排列为
(5)H元素与A元素形成化合物的化学式是
您最近一年使用:0次
10 . 元素周期表是打开物质世界奥秘之门的一把金钥匙,1869年门捷列夫发现了元素周期律并发表元素周期表。下图为元素周期表的一部分回答下列问题。

(1)上述元素中化学性质最稳定的是_______ (填元素符号下同),金属性最强的是_______ 。
(2)b、c的最高价氧化物对应水化物中,酸性更强的是_______ (用化学式表示),d、e形成的简单阴离子中,还原性更强的是_______ (用离子符号表示)。
(3)h元素的原子结构示意图是_______ ,写出h元素最高价氧化物的一种用途_______ 。
(4)d、e、f三种元素原子半径由大到小的顺序是_______ (用化学符号表示)。
(5)写出j的最高价氧化物对应水化物与g的最高价氧化物对应水化物反应的离子方程式_______ 。
(6)12gb单质在足量d单质中燃烧,所得气体通入 的最高价氧化物的水化物溶液中,完全吸收后,所得溶液中主要阴离子的物质的量之比是
的最高价氧化物的水化物溶液中,完全吸收后,所得溶液中主要阴离子的物质的量之比是_______ 。

(1)上述元素中化学性质最稳定的是
(2)b、c的最高价氧化物对应水化物中,酸性更强的是
(3)h元素的原子结构示意图是
(4)d、e、f三种元素原子半径由大到小的顺序是
(5)写出j的最高价氧化物对应水化物与g的最高价氧化物对应水化物反应的离子方程式
(6)12gb单质在足量d单质中燃烧,所得气体通入
 的最高价氧化物的水化物溶液中,完全吸收后,所得溶液中主要阴离子的物质的量之比是
的最高价氧化物的水化物溶液中,完全吸收后,所得溶液中主要阴离子的物质的量之比是
您最近一年使用:0次



