名校
解题方法
1 . 钛酸钙是最典型的钙钛矿型化合物,该类化合物具有特殊的理化性质。
(1)基态 的核外电子排布式为
的核外电子排布式为____________ 。
(2)钛酸钙的晶胞如下图所示。
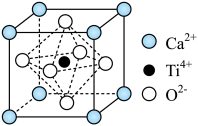
①每个 周围等距且紧邻的
周围等距且紧邻的 有
有______ 个。
②比较 和
和 的离子半径大小并说明理由
的离子半径大小并说明理由____________ 。
(3)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞中距离最近的 和
和 之间的距离为
之间的距离为 ,则钛酸钙晶体密度
,则钛酸钙晶体密度
______  (列出计算式)。
(列出计算式)。
②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是______ (填字母序号)。
a. b.
b.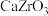 c.
c.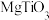
(4)通过离子替代可获得具有优异光电性能的有机钙钛矿型化合物 。其中有机阳离子
。其中有机阳离子 可由甲胺(
可由甲胺( )制得。
)制得。
① 中N的杂化方式为
中N的杂化方式为____________ 。
请从化学键的角度解释由甲胺形成 的过程:
的过程:____________ 。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)钛酸钙的晶胞如下图所示。

①每个
 周围等距且紧邻的
周围等距且紧邻的 有
有②比较
 和
和 的离子半径大小并说明理由
的离子半径大小并说明理由(3)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞中距离最近的
 和
和 之间的距离为
之间的距离为 ,则钛酸钙晶体密度
,则钛酸钙晶体密度
 (列出计算式)。
(列出计算式)。②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是
a.
 b.
b.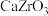 c.
c.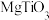
(4)通过离子替代可获得具有优异光电性能的有机钙钛矿型化合物
 。其中有机阳离子
。其中有机阳离子 可由甲胺(
可由甲胺( )制得。
)制得。①
 中N的杂化方式为
中N的杂化方式为请从化学键的角度解释由甲胺形成
 的过程:
的过程:
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
2 . 如图为分子X的结构图,其中A、B、C、D为同一族的元素,B电负性大于D,E与C的价电子数之和与Mg的质子数相同,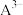 与
与 电子结构相同,工业上利用沸点差异分离出C的单质。下列说法错误的是
电子结构相同,工业上利用沸点差异分离出C的单质。下列说法错误的是

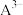 与
与 电子结构相同,工业上利用沸点差异分离出C的单质。下列说法错误的是
电子结构相同,工业上利用沸点差异分离出C的单质。下列说法错误的是
| A.X中A、C的杂化轨道类型相同 | B.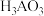 是三元酸 是三元酸 |
| C.原子半径大小:A>E | D.A、B、C、D、E均满足8电子结构 |
您最近一年使用:0次
名校
解题方法
3 . 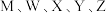 是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
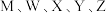 是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外层电子数等于X的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法正确的是
A.原子半径: |
| B.X的氧化物一定属于酸性氧化物 |
| C.在Q的结构中,所有原子最外层均满足8电子稳定结构 |
| D.Y元素组成的最常见单质和M的单质,在加热条件下生成的化合物中只含离子键 |
您最近一年使用:0次
2023-12-05更新
|
1970次组卷
|
11卷引用:吉林省长春市东北师大附中2023-2024学年高三上学期第三次摸底考试化学科试卷
吉林省长春市东北师大附中2023-2024学年高三上学期第三次摸底考试化学科试卷宁夏石嘴山市第三中学2023-2024学年高三上学期第四次月考理科综合试卷宁夏回族自治区石嘴山市第三中学2023-2024学年高三上学期第四次月考理综试题福建省泉州市培元中学2023-2024学年高三上学期12月月考化学试题四川省成都市石室中学2023-2024学年高三上学期期末考试理综试题-高中化学(已下线)选择题11-16(已下线)专题04 物质结构与性质-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)黑龙江省大庆市大庆中学2023-2024学年高三下学期开学化学试题陕西省西安中学2023-2024学年高三下学期模拟预测(五)理综试题-高中化学江西省赣州地区2023-2024学年十大教学能手选拔赛高中化学试题湖南省永州市第一中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
4 . 常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01 )的
)的 和原子半径、原子序数的关系如图所示。下列说法错误的是
和原子半径、原子序数的关系如图所示。下列说法错误的是

 )的
)的 和原子半径、原子序数的关系如图所示。下列说法错误的是
和原子半径、原子序数的关系如图所示。下列说法错误的是
A.电负性: |
| B.W和X形成的化合物XW3中含有离子键和共价键 |
C.简单氢化物的沸点: |
D.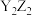 为非极性分子, 为非极性分子, 为极性分子,二者中的Y原子都是 为极性分子,二者中的Y原子都是 杂化 杂化 |
您最近一年使用:0次
5 . X,Y、Z、W、R为原子序数依次增大的前20号主族元素,且分属于四个周期。Y的最外层电子数是电子层数的3倍,Z、W为同周期相邻元素,Y、W可形成如图所示的离子,R原子核外无未成对电子。回答下列问题:
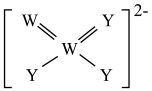
(1)第七周期与Z同族元素的原子序数为___________ 。
(2)Z、W、R简单离子半径由大到小的顺序为___________ (用化学式表示)。
(3)用电子式表示X与R组成的物质的形成过程:___________ 。
(4)Y、W的简单氢化物沸点较高的是___________ (填化学式),判断依据是___________ 。
(5)写出图中离子与稀硫酸反应的离子方程式:___________ 。

(1)第七周期与Z同族元素的原子序数为
(2)Z、W、R简单离子半径由大到小的顺序为
(3)用电子式表示X与R组成的物质的形成过程:
(4)Y、W的简单氢化物沸点较高的是
(5)写出图中离子与稀硫酸反应的离子方程式:
您最近一年使用:0次
6 . 金属M在潮湿的空气中会形成一层致密稳定的3M(XY)2•MZX3,X、Y、Z为短周期主族元素,X的原子序数是Y的8倍,基态X和Z的未成对电子数相同,M是人体必需的元素之一。1molMZX3,含有42mol质子,下列说法正确的是
| A.离子半径:M>X | B.X、Y、Z的电负性大小为:X>Z>Y |
| C.M的最高价氧化物对应水化物为强碱 | D.第一电离能:Z>X |
您最近一年使用:0次
2023-10-25更新
|
717次组卷
|
6卷引用:浙江省普通高中拔尖强基联盟协作体2023–2024学年高三上学期九月化学入学联考化学试题
浙江省普通高中拔尖强基联盟协作体2023–2024学年高三上学期九月化学入学联考化学试题(已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)(已下线)压轴题05 “位-构-性”元素推断(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)(已下线)选择题11-16辽宁省沈阳市东北育才学校高中部2023-2024学年高二上学期第二次月考化学试题浙江省宁波市2023-2024学年高二上学期九校联考化学试题
7 . 几种短周期元素的原子半径及主要化合价见下表,下列相关叙述错误的是
| 元素代号 |  |  |  |  |  |
原子半径 |  |  | 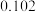 | 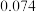 |  |
| 主要化合价 |  |  |  、 、 |  |  、 、 |
A. 、 、 最高价氧化物对应的水化物碱性: 最高价氧化物对应的水化物碱性: |
B.离子半径: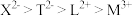 |
C. 单质能与 单质能与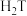 反应,置换出 反应,置换出 |
D. 的最高价氧化物是两性氧化物 的最高价氧化物是两性氧化物 |
您最近一年使用:0次
解题方法
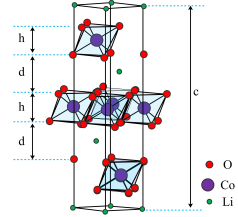
8 . 钴酸锂(LiCoO2)是常见的锂离子电池正极材料,其晶胞结构示意图如图。晶体中O围绕Co形成八面体,八面体共棱形成带负电的层状空间结构,与Li+层交替排列。在充放电过程中,Li+在层间脱出或嵌入。
(1)下列Li原子电子排布图表示的状态中,能量最低的是______ 。
(2)Li+与H-具有相同的电子构型,离子半径r(Li+)小于r(H-)的主要原因是______ 。
(3)观察该晶胞图示,其中Li处于晶胞顶点或晶胞内部,Co处于晶胞内部或晶胞侧棱上,而O的位置不易观察。结合钴酸锂(LiCoO2)化学式,可推断该晶胞中O的个数为______ 。
(4)晶胞底面为菱形,晶胞高度为cnm,Co和O组成八面体层高度为hnm,计算两层间的距离d=______ nm。(列出计算式)
(5)Li+在______ (填“充电”或“放电”)过程中会从八面体层间脱出。该过程会导致晶胞高度c变大,解释原因:______ 。

(1)下列Li原子电子排布图表示的状态中,能量最低的是
A.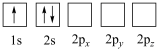 | B.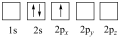 |
C.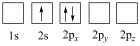 | D. |
(2)Li+与H-具有相同的电子构型,离子半径r(Li+)小于r(H-)的主要原因是
(3)观察该晶胞图示,其中Li处于晶胞顶点或晶胞内部,Co处于晶胞内部或晶胞侧棱上,而O的位置不易观察。结合钴酸锂(LiCoO2)化学式,可推断该晶胞中O的个数为
(4)晶胞底面为菱形,晶胞高度为cnm,Co和O组成八面体层高度为hnm,计算两层间的距离d=
(5)Li+在
您最近一年使用:0次
解题方法
9 . W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为18,四种元素形成的一种化合物的结构如图所示,下列说法错误的是


A.原子半径: | B.简单氢化物的沸点: |
| C.W、X和Y三种元素能形成离子化合物 | D.X的含氧酸一定是强酸 |
您最近一年使用:0次
名校
解题方法
10 . 日光灯中用到的某种荧光粉的主要成分为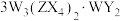 。已知:
。已知: 、
、 、
、 和
和 为原子序数依次增大的前20号元素,
为原子序数依次增大的前20号元素, 为金属元素,基态
为金属元素,基态 原子
原子 轨道上的电子数和
轨道上的电子数和 轨道上的电子数相等,基态
轨道上的电子数相等,基态 、
、 、
、 原子的未成对电子数之比为
原子的未成对电子数之比为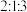 。下列说法正确的是
。下列说法正确的是
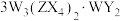 。已知:
。已知: 、
、 、
、 和
和 为原子序数依次增大的前20号元素,
为原子序数依次增大的前20号元素, 为金属元素,基态
为金属元素,基态 原子
原子 轨道上的电子数和
轨道上的电子数和 轨道上的电子数相等,基态
轨道上的电子数相等,基态 、
、 、
、 原子的未成对电子数之比为
原子的未成对电子数之比为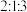 。下列说法正确的是
。下列说法正确的是A.原子半径: | B. 元素最高价化物对应的水化物具有强氧化性 元素最高价化物对应的水化物具有强氧化性 |
C.电负性: | D.能与水反应生成气体的单质只有 的单质 的单质 |
您最近一年使用:0次



