名校
解题方法
1 .  可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关
可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关 的说法正确的是
的说法正确的是
 可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关
可用作高压发电系统的绝缘气体,分子呈正八面体结构,如图所示。有关 的说法正确的是
的说法正确的是
A. 是只含极性键的非极性分子 是只含极性键的非极性分子 | B.键角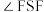 都等于 都等于 |
| C.S与F之间共用电子对偏向S | D.推测 在水中溶解度较大 在水中溶解度较大 |
您最近半年使用:0次
名校
2 . 嫦娥5号月球探测器带回的月壤样品的元素分析结果如图,下列有关含量前六位元素的说法正确的是
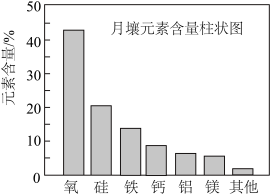
| A.基态Mg原子有6种能量不同的电子 | B.这六种元素中,电负性最大的是O |
| C.Ca原子核外有4种形状的原子轨道 | D.基态原子未成对电子数:Si<Al |
您最近半年使用:0次
3 . 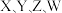 四种短周期元素,
四种短周期元素, 的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是
的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是
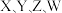 四种短周期元素,
四种短周期元素, 的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是
的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是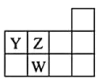
A.单质 与 与 常温下能直接化合 常温下能直接化合 | B.简单氢化物的沸点: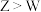 |
C.电负性: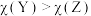 | D. 三种元素组成的化合物是离子化合物 三种元素组成的化合物是离子化合物 |
您最近半年使用:0次
名校
解题方法
4 .  (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度( 350℃)而成为颇具潜力的化学储氢材料之一,它可通过环硼氨烷、
350℃)而成为颇具潜力的化学储氢材料之一,它可通过环硼氨烷、 与
与 进行合成。
进行合成。
1.上述涉及的元素H、B、C、N、O原子半径最大的是___________ ,电负性最大的是___________ 。
2.键角:
___________  (填“
(填“ ”“
”“ ”或“
”或“ ”),原因是
”),原因是___________ 。
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度( 350℃)而成为颇具潜力的化学储氢材料之一,它可通过环硼氨烷、
350℃)而成为颇具潜力的化学储氢材料之一,它可通过环硼氨烷、 与
与 进行合成。
进行合成。1.上述涉及的元素H、B、C、N、O原子半径最大的是
2.键角:

 (填“
(填“ ”“
”“ ”或“
”或“ ”),原因是
”),原因是
您最近半年使用:0次
名校
解题方法
5 . 工业上高纯晶体硅时中间产物为SiHCl3,SiHCl3中电负性由大到小的顺序是___________ ,其中处于同一周期的两元素第一电离能大小关系为___________ 。
您最近半年使用:0次
名校
6 . 下列解释不正确的是
| 选项 | 物质的结构或性质或者实验目的 | 解释 |
| A | 键角: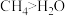 | CH4中C原子与H2O中O原子杂化不同 |
| B | CH4、SiH4、GeH4熔点逐渐升高 | 相对分子质量逐渐增大 |
| C | 一氟乙酸的 大于一溴乙酸 大于一溴乙酸 |  的电负性比 的电负性比 的大 的大 |
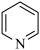
| D | 水中溶解性;苯<吡啶( | 吡啶能与水形成分子间氢键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
7 . 已知: 与
与 在一定条件下可以发生如下反应,
在一定条件下可以发生如下反应,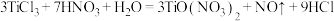 .回答下列问题:
.回答下列问题:
(1)基态钛原子的核外电子排布式为_____________ .
(2)N、H、O三种元素的电负性由大到小的顺序为_____________ .
(3)上述方程式中涉及的元素中属于P区元素的是_____________ (填元素符号).
(4) 的空间结构为
的空间结构为_____________ .
(5)肼 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被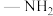 (氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下:
(氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下: .若该反应中有
.若该反应中有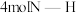 键断裂,则形成的
键断裂,则形成的 键有
键有_____________  .
.
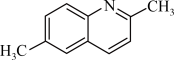
(6)由C、H、N三种元素形成的一种有机物的结构简式如下,则该物质中N原子的杂化方式为_____________ ,C原子的杂化方式为_____________ .
 与
与 在一定条件下可以发生如下反应,
在一定条件下可以发生如下反应,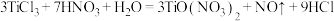 .回答下列问题:
.回答下列问题:(1)基态钛原子的核外电子排布式为
(2)N、H、O三种元素的电负性由大到小的顺序为
(3)上述方程式中涉及的元素中属于P区元素的是
(4)
 的空间结构为
的空间结构为(5)肼
 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被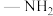 (氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下:
(氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下: .若该反应中有
.若该反应中有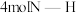 键断裂,则形成的
键断裂,则形成的 键有
键有 .
.(6)由C、H、N三种元素形成的一种有机物的结构简式如下,则该物质中N原子的杂化方式为
您最近半年使用:0次
名校
解题方法
8 . 下列说法中,正确的是
| A.N、P、S的第一电离能依次减小 | B.Li、Na、K的电负性依次增大 |
| C.F、O、Na的原子半径依次减小 | D.甲烷、氨气、水的键角依次增大 |
您最近半年使用:0次
名校
解题方法
9 . 卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示。下列判断不正确的是
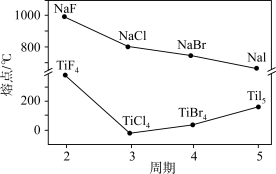
| A.NaX随X-半径增大,离子键减弱 |
| B.四氯化钛中存在共价键和分子间作用力 |
| C.TiF4的熔点反常升高是由于氢键的作用 |
| D.由图可看出F的电负性强于Cl、Br、I |
您最近半年使用:0次
名校
解题方法
10 . 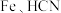 与
与 在一定条件下发生如下反应:
在一定条件下发生如下反应: ,下列说法正确的是
,下列说法正确的是
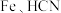 与
与 在一定条件下发生如下反应:
在一定条件下发生如下反应: ,下列说法正确的是
,下列说法正确的是A.此化学方程式中涉及的第二周期元素的电负性大小的顺序为 |
B.配合物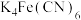 中心离子的配位数是10 中心离子的配位数是10 |
C.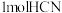 分子中含有 分子中含有 键的数目为 键的数目为 |
D. 中阴离子的空间构型为三角锥形,其中碳原子的价层电子对数为4 中阴离子的空间构型为三角锥形,其中碳原子的价层电子对数为4 |
您最近半年使用:0次

 )
)

