解题方法
1 . 近日,科学家利用铁配合物催化氮气选择性转化成肼。铁配合物结构如图所示(Et为乙基:-CH2CH3)。

回答下列问题:
(1)基态 的价层电子排布式
的价层电子排布式___________ ,微粒半径Fe___________  。(填“大于”、“小于”或“等于”)
。(填“大于”、“小于”或“等于”)
(2) 所含元素中,电负性最大的元素是
所含元素中,电负性最大的元素是___________ 。P原子的杂化类型是___________ 。
(3) 和
和 的相对分子质量相同,但是常温常压下,
的相对分子质量相同,但是常温常压下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是___________ 。
(4) 的VSEPR模型为
的VSEPR模型为___________ 。写出N2的一种等电子体___________ 。
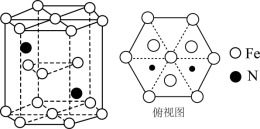
(5)某种磁性氮化铁的晶胞结构如图所示。已知: 为阿伏加德罗常数的值,六棱柱底边的边长为
为阿伏加德罗常数的值,六棱柱底边的边长为 ,高为
,高为 ,该晶体中Fe、N原子个数最简比为
,该晶体中Fe、N原子个数最简比为___________ 。该晶体的密度为___________  (只列计算式)。
(只列计算式)。

回答下列问题:
(1)基态
 的价层电子排布式
的价层电子排布式 。(填“大于”、“小于”或“等于”)
。(填“大于”、“小于”或“等于”)(2)
 所含元素中,电负性最大的元素是
所含元素中,电负性最大的元素是(3)
 和
和 的相对分子质量相同,但是常温常压下,
的相对分子质量相同,但是常温常压下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是(4)
 的VSEPR模型为
的VSEPR模型为(5)某种磁性氮化铁的晶胞结构如图所示。已知:
 为阿伏加德罗常数的值,六棱柱底边的边长为
为阿伏加德罗常数的值,六棱柱底边的边长为 ,高为
,高为 ,该晶体中Fe、N原子个数最简比为
,该晶体中Fe、N原子个数最简比为 (只列计算式)。
(只列计算式)。
您最近一年使用:0次
名校
解题方法
2 . X、Y、Z、W为原子序数依次增大的前四周期元素,X为元素周期表中半径最小的原子,Z是地壳中含量最多的元素,W的原子序数为29,X、Y、Z、W形成的阳离子如图所示,下列说法正确的是
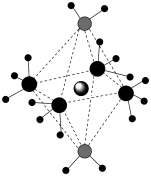
A.原子半径: | B.该阳离子中心离子的配位数为6 |
C.氢化物的沸点: | D.两种配体中的键角: |
您最近一年使用:0次
名校
3 . 下列关于物质结构与性质的说法,不正确的是
A. 中的 中的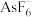 离子的空间结构为正八面体形 离子的空间结构为正八面体形 |
| B.C、H、O三种元素的电负性由小到大的顺序为H<C<O |
C.HClO、 、 、 的中心原子价层电子对数不完全相同 的中心原子价层电子对数不完全相同 |
| D.第四周期元素中,Ga的第一电离能低于Zn |
您最近一年使用:0次
解题方法
4 . 请按要求回答下列问题:
(1)符号“3px”没有给出的信息是___________。
(2)某元素基态原子4s轨道上有1个电子,则该元素基态原子价电子排布不可能是___________。
(3)X元素的原子最外层电子排布式为(n+1)sn(n+1)pn+1,则X的氢化物的化学式是___________。
(4)下列比较正确的是___________ 。
A.酸性:H3PO4<H3AsO4 B.键角:H2O<NH3 C.离子半径:r(Al3+)>r(O2-)
(5)下列实验事实不能用氢键来解释的是___________。
(1)符号“3px”没有给出的信息是___________。
| A.能层 | B.能级 | C.电子云在空间的伸展方向 | D.电子的自旋方向 |
| A.4s1 | B.3p64s1 | C.3d54s1 | D.3d104s1 |
| A.HX | B.H2X | C.XH3 | D.XH4 |
A.酸性:H3PO4<H3AsO4 B.键角:H2O<NH3 C.离子半径:r(Al3+)>r(O2-)
(5)下列实验事实不能用氢键来解释的是___________。
| A.CH4比SiH4稳定 |
| B.乙醇能与水以任意比互溶 |
| C.邻羟基苯甲醛的沸点低于对羟基苯甲醛 |
| D.接近沸点的水蒸气的相对分子质量测量值大于18 |
您最近一年使用:0次
名校
解题方法
5 . 下列说法不正确的是
| A.电负性:N> P>Li |
B.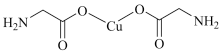 中σ键和 中σ键和 键比例为7:1 键比例为7:1 |
C.N2与 互为等电子体, 互为等电子体, 中含有的 中含有的 键数目为 键数目为 |
D.C 中的所有原子均共面 中的所有原子均共面 |
您最近一年使用:0次
2023-04-08更新
|
244次组卷
|
3卷引用:陕西省西安市西北工业大学附属中学2023-2024学年高二上学期期末质量检化学试题
6 . 按要求填空。
(1)已知Ge与C同族, 中心原子价层电子对互斥模型为
中心原子价层电子对互斥模型为_______ 。
(2)等电子体是具有相同的价电子数和原子数的分子或离子,它们通常具有相似的空间结构。CO的结构式为_______ , 的空间结构为
的空间结构为_______ 。
(3)根据对角线规则,铍(Be)的性质_______ (填化学式)相似,能与氢氧化钠溶液反应。写出氢氧化铍与氢氧化钠溶液反应的化学方程式_______ 。
(4)某有机物结构简式为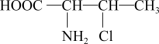 ,该分子中含有
,该分子中含有_______ 个手性碳原子。
(5)在BF3分子中,硼原子的杂化轨道类型为_______ ,F-B-F的键角是_______ , 为
为_______ 分子(填“极性”或“非极性”)。
(1)已知Ge与C同族,
 中心原子价层电子对互斥模型为
中心原子价层电子对互斥模型为(2)等电子体是具有相同的价电子数和原子数的分子或离子,它们通常具有相似的空间结构。CO的结构式为
 的空间结构为
的空间结构为(3)根据对角线规则,铍(Be)的性质
(4)某有机物结构简式为
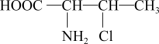 ,该分子中含有
,该分子中含有(5)在BF3分子中,硼原子的杂化轨道类型为
 为
为
您最近一年使用:0次
解题方法
7 . SiCl4可发生水解反应,机理如下:

中间体SiCl4(H2O)中Si采取的杂化类型为

中间体SiCl4(H2O)中Si采取的杂化类型为
| A.dsp2 | B.sp3d | C.sp3d2 | D.sp3 |
您最近一年使用:0次
8 . 下列分子的中心原子是 杂化的是
杂化的是
 杂化的是
杂化的是A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
9 . 下表是元素周期表的一部分。表中所列的字母分别代表一种元素。
回答下列问题:
(1)D的简单气态氢化物分子的立体构型为___________ 。
(2)第一电离能H___________ X(填“>”、“<”或“=”)。
(3)DA3的沸点比D2E的沸点高,其原因是___________ 。
(4)YE 的立体构型为
的立体构型为___________ ,YE 的键角比YE
的键角比YE 的键角小的原因是
的键角小的原因是___________ 。
| A | R | ||||||||||||||||
| B | D | E | M | T | |||||||||||||
| G | H | X | J | Y | L | ||||||||||||
| N |
(1)D的简单气态氢化物分子的立体构型为
(2)第一电离能H
(3)DA3的沸点比D2E的沸点高,其原因是
(4)YE
 的立体构型为
的立体构型为 的键角比YE
的键角比YE 的键角小的原因是
的键角小的原因是
您最近一年使用:0次
2022-05-05更新
|
101次组卷
|
2卷引用:陕西省西安中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
10 . 硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)基态S原子价层电子的电子排布图(轨道表达式)为_______ ,其电子占据最高能级的电子云轮廓图为_______ 形。
(2)根据价层电子对互斥理论, 、
、 、
、 的气态分子中,中心原子价层电子对数不同其他分子的是
的气态分子中,中心原子价层电子对数不同其他分子的是_______ 。
(3)气态三氧化硫以单分子形式存在,其分子的立体构型为_______ 形;固体三氧化硫中存在如下图所示的三聚分子,该分子中S原子的杂化轨道类型为_______ 。
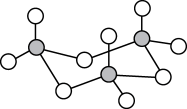
(4)已知亚硫酸根的键角小于硫酸根的键角,请用相关理论解释原因:_______ 。
(5)已知含量酸的酸性与结构中非羟基氧的数目有关,强酸一般有两个非羟基氧(如硫酸: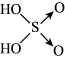 ),中强酸一般有一个非羟基氧(如磷酸:
),中强酸一般有一个非羟基氧(如磷酸: )。已知亚磷酸(H3PO3)是一种二元中强酸。
)。已知亚磷酸(H3PO3)是一种二元中强酸。
①请写出亚磷酸的结构式_______ 。
② 与过量的
与过量的 溶液反应的离子方程式为
溶液反应的离子方程式为_______ 。
| H2S | SO2 | SO3 | H2SO4 | |
| 熔点/℃ | -85.5 | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)基态S原子价层电子的电子排布图(轨道表达式)为
(2)根据价层电子对互斥理论,
 、
、 、
、 的气态分子中,中心原子价层电子对数不同其他分子的是
的气态分子中,中心原子价层电子对数不同其他分子的是(3)气态三氧化硫以单分子形式存在,其分子的立体构型为

(4)已知亚硫酸根的键角小于硫酸根的键角,请用相关理论解释原因:
(5)已知含量酸的酸性与结构中非羟基氧的数目有关,强酸一般有两个非羟基氧(如硫酸:
 ),中强酸一般有一个非羟基氧(如磷酸:
),中强酸一般有一个非羟基氧(如磷酸: )。已知亚磷酸(H3PO3)是一种二元中强酸。
)。已知亚磷酸(H3PO3)是一种二元中强酸。①请写出亚磷酸的结构式
②
 与过量的
与过量的 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次



