1 .  、
、 都是重要的有机反应中间体,下列说法正确的是
都是重要的有机反应中间体,下列说法正确的是
 、
、 都是重要的有机反应中间体,下列说法正确的是
都是重要的有机反应中间体,下列说法正确的是A. 的球棍模型为 的球棍模型为 | B. 中C-H为 中C-H为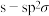 |
C. 中键角为109°28′ 中键角为109°28′ | D. 与 与 形成的化合物中含有离子键 形成的化合物中含有离子键 |
您最近一年使用:0次
名校
解题方法
2 . ⅥA族元素在生产、生活中有着重要的应用。
(1)臭氧分子是___________ (填“极性”或“非极性”)分子。
(2) 溶液中滴加氨水,
溶液中滴加氨水, 最终转化为
最终转化为 。
。 中含有
中含有___________ mol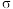 键,
键, 转化为
转化为 的原因为
的原因为___________ 。
(3)①As、Se、Br的第一电离能由小到大的顺序:___________ ,原因:___________ ;电负性由小到大的顺序:___________ ;
②热的浓硒酸可以溶解单质金,产生红黄色的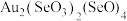 (Au为+3价),这种红黄色物质中Se元素的杂化方式为
(Au为+3价),这种红黄色物质中Se元素的杂化方式为___________ 。
(4)①基态Te原子电子排布式为___________ ;
②碲酸 中除了Te元素外只有羟基基团,
中除了Te元素外只有羟基基团, 的空间构型:
的空间构型:___________ ;
③第三代太阳能电池就是铜镓硒等化合物薄膜太阳能电池,其中一种结构如图所示:
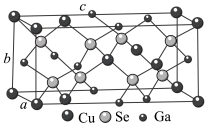
已知晶胞参数为anm、bnm、cnm。则晶体的密度为___________  。
。
(1)臭氧分子是
(2)
 溶液中滴加氨水,
溶液中滴加氨水, 最终转化为
最终转化为 。
。 中含有
中含有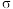 键,
键, 转化为
转化为 的原因为
的原因为(3)①As、Se、Br的第一电离能由小到大的顺序:
②热的浓硒酸可以溶解单质金,产生红黄色的
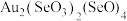 (Au为+3价),这种红黄色物质中Se元素的杂化方式为
(Au为+3价),这种红黄色物质中Se元素的杂化方式为(4)①基态Te原子电子排布式为
②碲酸
 中除了Te元素外只有羟基基团,
中除了Te元素外只有羟基基团, 的空间构型:
的空间构型:③第三代太阳能电池就是铜镓硒等化合物薄膜太阳能电池,其中一种结构如图所示:

已知晶胞参数为anm、bnm、cnm。则晶体的密度为
 。
。
您最近一年使用:0次
名校
解题方法
3 . 现有A、B、C、D、E、F、G、H八种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
A:核外电子数和电子层数相等,也是宇宙中最丰富的元素
B:形成化合物种类最多的元素
C:基态原子的核外p能级电子数比s能级电子数少1
D:基态原子的核外p轨道中有两个未成对电子
E:气态基态原子的第一至第四电离能分别是:I1=738 kJ/mol,I2=1451 kJ/mol,I3=7733 kJ/mol,I4=10540 kJ/mol
F:同周期元素的简单离子中半径最小
G:主族序数与周期数的差为4
H:前四周期主族元素中电负性最小
(1)C2A4的电子式为_______ 。
(2)B元素的原子核外共有_______ 种不同空间运动状态的电子,电子所处最高能级轨道的形状为_______ 。
(3)G2D分子的VSEPR模型名称为_______ 。
(4)某同学推断E元素基态原子的轨道表示式为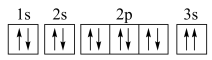 。该同学所画的轨道表示式违背了
。该同学所画的轨道表示式违背了_______ ,解释E元素原子的第一电离能大于F元素原子的第一电离能的原因:_______ 。
(5)B2A4分子中含有的σ键、π键数目之比为_______ 。
(6)与F元素成“对角线规则”关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与H元素的最高价氧化物的水化物反应的离子方程式:_______ 。
(7)与H元素同周期的基态原子中,未成对电子数与H原子相同的元素有_______ 种。
A:核外电子数和电子层数相等,也是宇宙中最丰富的元素
B:形成化合物种类最多的元素
C:基态原子的核外p能级电子数比s能级电子数少1
D:基态原子的核外p轨道中有两个未成对电子
E:气态基态原子的第一至第四电离能分别是:I1=738 kJ/mol,I2=1451 kJ/mol,I3=7733 kJ/mol,I4=10540 kJ/mol
F:同周期元素的简单离子中半径最小
G:主族序数与周期数的差为4
H:前四周期主族元素中电负性最小
(1)C2A4的电子式为
(2)B元素的原子核外共有
(3)G2D分子的VSEPR模型名称为
(4)某同学推断E元素基态原子的轨道表示式为
 。该同学所画的轨道表示式违背了
。该同学所画的轨道表示式违背了(5)B2A4分子中含有的σ键、π键数目之比为
(6)与F元素成“对角线规则”关系的某短周期元素T的最高价氧化物的水化物具有两性,写出该两性物质与H元素的最高价氧化物的水化物反应的离子方程式:
(7)与H元素同周期的基态原子中,未成对电子数与H原子相同的元素有
您最近一年使用:0次
22-23高二上·浙江杭州·期中
名校
解题方法
4 . 下列有关描述正确的是
| A.O3为非极性分子 |
| B.NCl3的空间结构为平面三角形 |
C. 的VSEPR模型、空间结构均为平面三角形 的VSEPR模型、空间结构均为平面三角形 |
D. 的VSEPR模型、空间结构相同 的VSEPR模型、空间结构相同 |
您最近一年使用:0次
解题方法
5 . 某小组同学探究实验室配制银氨溶液并检验醛基的方法。
资料:i.AgOH是白色难溶于水的物质,常温下极不稳定,分解生成棕色微溶于水的 。
。
ii.向硝酸银溶液中加入氨水,转化为 的
的 占参加反应的
占参加反应的 总量的百分比最大不超过10%。
总量的百分比最大不超过10%。
Ⅰ.在实验室配制银氨溶液的过程中,小组同学发现,所用试剂的配制方式和存放时间不同,实验现象不同。(注:以下试剂若无特殊说明,均为新制)
(1)NH3分子空间构型为_______ 。
(2)结合资料ii,写出实验1中加入少量氨水时发生的主要反应的离子方程式_______ 。
(3)已知,实验2中白色沉淀加硝酸产生能使澄清石灰水变浑浊的无色气体,实验2中白色沉淀的主要成分是_______ 。
(4)对比实验1和3,分析实验3中“溶液始终澄清”的原因是_______ 。
Ⅱ.用实验1配制出的银氨溶液检验醛基。
资料:可从电极反应角度分析物质氧化性和还原性的变化。
(5)银氨溶液与CH3CHO的反应中,电极反应式:
还原反应:Ag++e-=Ag;氧化反应:_______ (碱性条件下)。
在此基础上设计并实施了以下实验。
(6)实验5产生银镜比实验4快的可能原因是_______ 。按照实验5的方法,将乙醛换成丙酮,水浴加热后也能产生银镜。
综合上述实验,实验4是检验醛基的最合理方法。
资料:i.AgOH是白色难溶于水的物质,常温下极不稳定,分解生成棕色微溶于水的
 。
。ii.向硝酸银溶液中加入氨水,转化为
 的
的 占参加反应的
占参加反应的 总量的百分比最大不超过10%。
总量的百分比最大不超过10%。Ⅰ.在实验室配制银氨溶液的过程中,小组同学发现,所用试剂的配制方式和存放时间不同,实验现象不同。(注:以下试剂若无特殊说明,均为新制)
| 序号 | 实验操作 | 实验现象 |
| 1 | 向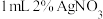 溶液中逐滴加入2%氨水 溶液中逐滴加入2%氨水 | 先产生棕色沉淀,后溶液变澄清 |
| 2 | 向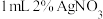 溶液中逐滴加入在空气中存放一段时间的2%氨水 溶液中逐滴加入在空气中存放一段时间的2%氨水 | 先产生白色沉淀,后溶液变澄清 |
| 3 | 向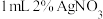 ( ( 酸化)溶液中逐滴加入2%氨水至过量 酸化)溶液中逐滴加入2%氨水至过量 | 溶液始终澄清 |
(2)结合资料ii,写出实验1中加入少量氨水时发生的主要反应的离子方程式
(3)已知,实验2中白色沉淀加硝酸产生能使澄清石灰水变浑浊的无色气体,实验2中白色沉淀的主要成分是
(4)对比实验1和3,分析实验3中“溶液始终澄清”的原因是
Ⅱ.用实验1配制出的银氨溶液检验醛基。
资料:可从电极反应角度分析物质氧化性和还原性的变化。
(5)银氨溶液与CH3CHO的反应中,电极反应式:
还原反应:Ag++e-=Ag;氧化反应:
在此基础上设计并实施了以下实验。
| 序号 | 实验操作 | 实验现象 |
| 4 | 向银氨溶液中加入3滴 ,水浴加热 ,水浴加热 | 产生银镜 |
| 5 | 向银氨溶液中加入1滴10% NaOH溶液后,滴入3滴 | 产生银镜比实验4快 |
综合上述实验,实验4是检验醛基的最合理方法。
您最近一年使用:0次
解题方法
6 . 2022年9月9日,国家航天局、国家原子能机构联合在北京发布“嫦娥五号”最新科学成果:中国科学家首次在月球上发现新矿物,并命名为“嫦娥石”。“嫦娥石”是一种新的磷酸盐矿物,属于陨磷钠镁钙石(Merrillite)族,颗粒约2~30微米,伴生矿物有钛铁矿等。回答下列问题:
(1)基态钛原子价电子排布式为_______ 。
(2)Fe的配合物有多种。 、
、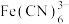 、
、 的配体中所含原子C、N、O、F电负性由大到小的顺序是
的配体中所含原子C、N、O、F电负性由大到小的顺序是_______ (写元素符号,下同);第一电离能由大到小的顺序为_______ 。
(3)磷酸为磷的最高价含氧酸,其空间结构如图:
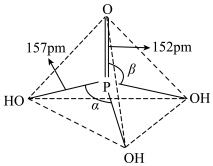
①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是_______ 。
② 的立体构型为
的立体构型为_______ ,中心原子的杂化类型是_______ 。
(4)反型钙钛矿电池无须使用具有光催化活性的 (通过氮掺杂生成
(通过氮掺杂生成 ,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
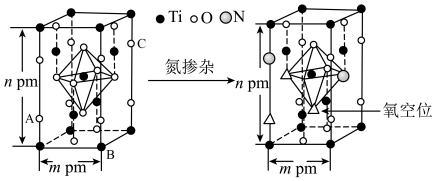
 晶体中
晶体中
_______ ;已知原子A、B的分数坐标分别为 和
和 ,则原子C的坐标为
,则原子C的坐标为_______ ,设阿伏加德罗常数的值为 ,
, 的密度为
的密度为_______ g·cm 。
。
(1)基态钛原子价电子排布式为
(2)Fe的配合物有多种。
 、
、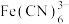 、
、 的配体中所含原子C、N、O、F电负性由大到小的顺序是
的配体中所含原子C、N、O、F电负性由大到小的顺序是(3)磷酸为磷的最高价含氧酸,其空间结构如图:

①纯净的磷酸黏度极大,随温度升高黏度迅速下降,原因是
②
 的立体构型为
的立体构型为(4)反型钙钛矿电池无须使用具有光催化活性的
 (通过氮掺杂生成
(通过氮掺杂生成 ,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
,反应如图)以及掺杂的有机空穴传输层,光照下的输出稳定性更好,更具发展潜力。
 晶体中
晶体中
 和
和 ,则原子C的坐标为
,则原子C的坐标为 ,
, 的密度为
的密度为 。
。
您最近一年使用:0次
2023-01-02更新
|
387次组卷
|
3卷引用:吉林省部分学校2022-2023学年高三上学期12月联考化学试题
名校
解题方法
7 . 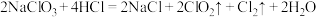 可用于制备含氯消毒剂。二氧化氯(
可用于制备含氯消毒剂。二氧化氯( )是一种黄绿色气体,易溶于水,在水中的溶解度约为
)是一种黄绿色气体,易溶于水,在水中的溶解度约为 的5倍,其水溶液在较高温度与光照下会生成
的5倍,其水溶液在较高温度与光照下会生成 与
与 。
。 是一种极易爆炸的强氧化性气体。下列关于
是一种极易爆炸的强氧化性气体。下列关于 、
、 和
和 的说法正确的是
的说法正确的是
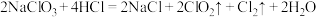 可用于制备含氯消毒剂。二氧化氯(
可用于制备含氯消毒剂。二氧化氯( )是一种黄绿色气体,易溶于水,在水中的溶解度约为
)是一种黄绿色气体,易溶于水,在水中的溶解度约为 的5倍,其水溶液在较高温度与光照下会生成
的5倍,其水溶液在较高温度与光照下会生成 与
与 。
。 是一种极易爆炸的强氧化性气体。下列关于
是一种极易爆炸的强氧化性气体。下列关于 、
、 和
和 的说法正确的是
的说法正确的是A. 为非极性分子 为非极性分子 | B. 中含有非极性键 中含有非极性键 |
C. 的空间结构为三角锥形 的空间结构为三角锥形 | D. 与 与 的键角相等 的键角相等 |
您最近一年使用:0次
2022-12-31更新
|
512次组卷
|
2卷引用:广东省梅州市名校2022-2023学年高三上学期期末考试化学试题
2022·浙江·模拟预测
解题方法
8 . 硼化物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态B原子核外电子有_______ 种不同的空间运动状态。
(2) 主要用作有机合成中的催化剂,也用于制作火箭的高能燃料。
主要用作有机合成中的催化剂,也用于制作火箭的高能燃料。 的空间构型为
的空间构型为_______ 。形成 时,基态B原子价层电子先进行激发,再进行杂化,激发时B原子的价层电子轨道表示式可能为
时,基态B原子价层电子先进行激发,再进行杂化,激发时B原子的价层电子轨道表示式可能为_______ 。(填序号)。
A.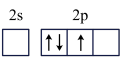 B.
B.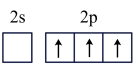 C.
C.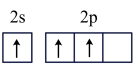 D.
D.
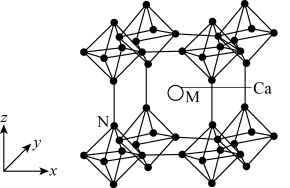
(3)Ca与B组成的金属硼化物结构如图所示,硼原子通过B—B键互相连接成三维骨架形成 正八面体,该结构具有立方晶系的对称性。
正八面体,该结构具有立方晶系的对称性。
①该晶体的化学式为_______ ,晶体中Ca原子的配位数为_______ 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如M点原子的分数坐标为 ,已知
,已知 八面体中B—B键的键长为rpm,晶胞参数为apm,则N点原子的分数坐标为
八面体中B—B键的键长为rpm,晶胞参数为apm,则N点原子的分数坐标为_______ ,Ca与B原子间的距离d为_______ pm(列出表达式即可)。
(1)基态B原子核外电子有
(2)
 主要用作有机合成中的催化剂,也用于制作火箭的高能燃料。
主要用作有机合成中的催化剂,也用于制作火箭的高能燃料。 的空间构型为
的空间构型为 时,基态B原子价层电子先进行激发,再进行杂化,激发时B原子的价层电子轨道表示式可能为
时,基态B原子价层电子先进行激发,再进行杂化,激发时B原子的价层电子轨道表示式可能为A.
 B.
B. C.
C. D.
D.
(3)Ca与B组成的金属硼化物结构如图所示,硼原子通过B—B键互相连接成三维骨架形成
 正八面体,该结构具有立方晶系的对称性。
正八面体,该结构具有立方晶系的对称性。①该晶体的化学式为
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如M点原子的分数坐标为
 ,已知
,已知 八面体中B—B键的键长为rpm,晶胞参数为apm,则N点原子的分数坐标为
八面体中B—B键的键长为rpm,晶胞参数为apm,则N点原子的分数坐标为
您最近一年使用:0次
名校
解题方法
9 . 一种提纯白磷样品(含惰性杂质)的工艺流程如图所示。
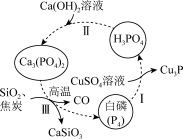
下列说法不正确 的是

下列说法
A. 的空间结构为正四面体形 的空间结构为正四面体形 |
| B.流程中所涉及元素的基态原子未成对电子数最多的是P |
| C.过程I、II、III中发生的均为氧化还原反应 |
| D.过程I中,氧化产物与还原产物的物质的量之比为6:5 |
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
10 . 根据所学知识回答问题
(1)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是___________ 。Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为___________ ,微粒之间存在的作用力是___________ 。比较下列锗卤化物的熔点和沸点,分析其变化规律及原因___________ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是___________ 。在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为___________ ,提供孤电子对的成键原子是___________ 。氨的沸点___________ (填“高于”或“低于”)膦(PH3),原因是___________ ;氨是___________ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为___________ 。
(3) AsCl3分子的立体构型为___________ ,其中As的杂化轨道类型为___________ 。
(1)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。[Ni(NH3)6]SO4中阴离子的立体构型是
(3) AsCl3分子的立体构型为
您最近一年使用:0次



