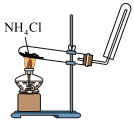
1 . 下列实验装置或操作不能达到实验目的的是
|
|
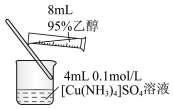
A.检验 是否沉淀完全 是否沉淀完全 | B.析出晶体[Cu(NH3)4]SO4·H2O |
|
|
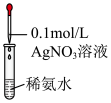
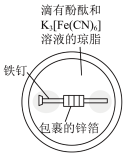
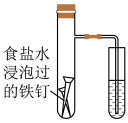
| C.配制银氨溶液 | D.牺牲阳极法保护铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 下列实验设计不能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A |  在水溶液中存在平衡 在水溶液中存在平衡 | 向1mL  的 的 溶液中加入1mL浓KI溶液,振荡试管,观察颜色变化 溶液中加入1mL浓KI溶液,振荡试管,观察颜色变化 |
| B | 比较AgCl和AgI的 | 向2mL 0.1 的NaCl溶液中滴加两滴等浓度的 的NaCl溶液中滴加两滴等浓度的 溶液,再滴加4滴等浓度KI溶液,观察现象 溶液,再滴加4滴等浓度KI溶液,观察现象 |
| C | 检验某卤代烃中的是否含有氯元素 | 取卤代烃少许与NaOH乙醇溶液共热后,加入稀硝酸酸化,再加入 溶液,观察是否有白色沉淀生成 溶液,观察是否有白色沉淀生成 |
| D | 比较配位键 和 和 的稳定性 的稳定性 | 向 溶液中加入少量NaCl固体,振荡,观察溶液颜色变化 溶液中加入少量NaCl固体,振荡,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
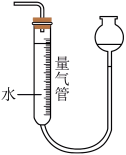
3 . 下列装置可以实现对应实验目的的是
|
|
| A.验证吸氧腐蚀 | B.分离乙醇和 |
|
|
C.制备 | D.测量 体积 体积 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . B、C、N、O、F、Fe是地壳中常见的元素。回答下列问题
(1)基态碳、氮、氧原子的未成对电子数之比是___________ ;电负性由大到小的顺序是___________ 。
(2)三氟化硼( )是一种无色气体。
)是一种无色气体。 水解生成
水解生成 和另一种一元无氧酸(甲),甲的化学式是
和另一种一元无氧酸(甲),甲的化学式是___________ 。
(3)三氟化硼( )分子中心原子的杂化轨道类型是
)分子中心原子的杂化轨道类型是___________ ;分子空间构型是___________ 。
(4)图1是一种太阳能电池工作原理的示意图。其中电解质溶液为 和
和 的混合溶液。
的混合溶液。 中,中心离子为
中,中心离子为___________ 。
②电池工作时,下列描述正确的是___________ 。
A.电极a为正极 B. 向电极a移动
向电极a移动
C.电子由电极a经导线流向电极b D.电极b上发生氧化反应
③正极上发生的电极反应为___________ 。
(5)氮化铁晶体,其晶胞结构如图2所示:___________ 个
A.2 B.4 C.6 D.8
②该氮化铁晶体的化学式为___________
A.FeN B.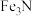 C.
C. D.
D.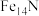
(1)基态碳、氮、氧原子的未成对电子数之比是
(2)三氟化硼(
 )是一种无色气体。
)是一种无色气体。 水解生成
水解生成 和另一种一元无氧酸(甲),甲的化学式是
和另一种一元无氧酸(甲),甲的化学式是(3)三氟化硼(
 )分子中心原子的杂化轨道类型是
)分子中心原子的杂化轨道类型是(4)图1是一种太阳能电池工作原理的示意图。其中电解质溶液为
 和
和 的混合溶液。
的混合溶液。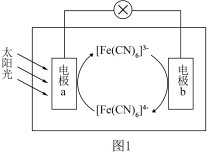
 中,中心离子为
中,中心离子为②电池工作时,下列描述正确的是
A.电极a为正极 B.
 向电极a移动
向电极a移动C.电子由电极a经导线流向电极b D.电极b上发生氧化反应
③正极上发生的电极反应为
(5)氮化铁晶体,其晶胞结构如图2所示:

A.2 B.4 C.6 D.8
②该氮化铁晶体的化学式为
A.FeN B.
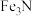 C.
C. D.
D.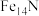
您最近一年使用:0次
名校
解题方法
5 . 下列离子方程式正确的是
A.向 溶液中滴加过量的氨水: 溶液中滴加过量的氨水: |
B.向乙二醇溶液中加入足量酸性高锰酸钾溶液: |
C.向饱和 溶液中通入过量 溶液中通入过量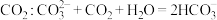 |
D.将少量 通入 通入 溶液中: 溶液中: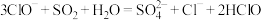 |
您最近一年使用:0次
6 . 配合物在许多方面有着广泛的用途,目前我国科学家利用配合物在能源转化与储存方面有着杰出的贡献,请根据题意回答下列问题:
(1)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知Ti3+的配位数为6,TiCl3·4H2O的化学式用配合物的形式表示为___ 。
(2)有下列实验:___ 。深蓝色晶体的化学式为___ 。
②写出蓝色沉淀溶解成深蓝色溶液的离子方程式___ 。
③[Cu(NH3)4]2+中H−N−H键角比NH3分子中H−N−H键角___ (填“大”或“小”)。[Cu(NH3)4]SO4中存在的化学键类型有___ (填标号)。
A.离子键 B.共价键 C.氢键 D.配位键
④物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是___ (填标号)。
A.[Cr(OH)4] − B.[Cu(CN)4]3− C.[ZnCl4]2− D.[Fe(CN)6]4−
画出[Cu(CN)4]2−的结构:___ (用“→”或“—”将配位键表示出来)。
(1)将 1 mol TiCl3·4H2O 溶于水,加入足量 AgNO3 溶液,得到 1 mol AgCl 沉淀,已知Ti3+的配位数为6,TiCl3·4H2O的化学式用配合物的形式表示为
(2)有下列实验:

②写出蓝色沉淀溶解成深蓝色溶液的离子方程式
③[Cu(NH3)4]2+中H−N−H键角比NH3分子中H−N−H键角
A.离子键 B.共价键 C.氢键 D.配位键
④物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是
A.[Cr(OH)4] − B.[Cu(CN)4]3− C.[ZnCl4]2− D.[Fe(CN)6]4−
画出[Cu(CN)4]2−的结构:
您最近一年使用:0次
7 . 舞蹈诗剧《只此青绿》感动国人,石青等矿石可做颜料。回答下列问题:
(1)石青,化学式为 ,基态
,基态 核外电子的空间运动状态有
核外电子的空间运动状态有___________ 种。
(2)配合物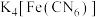 ,
,___________ 是中心离子,___________ 是配位原子(填元素或离子符号),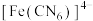 中σ键和π键的数目之比为
中σ键和π键的数目之比为___________ 。
(3)Cu2+可与H2O、Cl-、NH3等配体形成配位数为4的配离子,如 (蓝色)、
(蓝色)、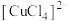 (黄色)、
(黄色)、 。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验:

①溶液I呈绿色原因为___________ ,若想要得到蓝色溶液,可采取的方法是___________ 。
②向溶液I中继续加入浓盐酸得到黄绿色溶液Ⅱ,测定平衡体系中: 浓度为
浓度为 、
、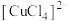 浓度为
浓度为 、
、 浓度为
浓度为 ,写出该过程对应的离子方程式
,写出该过程对应的离子方程式___________ ,该过程中 的转化率为
的转化率为___________ (用a、b、c中的字母表示)。
③向溶液Ⅱ中通入NH3至过量观察到的现象是___________ 。
④已知[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为___________ ,(填“正四面体”或“平面四边形”),写出该离子的结构简式___________ 。
(1)石青,化学式为
 ,基态
,基态 核外电子的空间运动状态有
核外电子的空间运动状态有(2)配合物
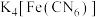 ,
,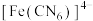 中σ键和π键的数目之比为
中σ键和π键的数目之比为(3)Cu2+可与H2O、Cl-、NH3等配体形成配位数为4的配离子,如
 (蓝色)、
(蓝色)、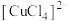 (黄色)、
(黄色)、 。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验:
①溶液I呈绿色原因为
②向溶液I中继续加入浓盐酸得到黄绿色溶液Ⅱ,测定平衡体系中:
 浓度为
浓度为 、
、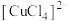 浓度为
浓度为 、
、 浓度为
浓度为 ,写出该过程对应的离子方程式
,写出该过程对应的离子方程式 的转化率为
的转化率为③向溶液Ⅱ中通入NH3至过量观察到的现象是
④已知[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
您最近一年使用:0次
8 . 铜氨溶液含有 ,具有溶解纤维素的性能,在溶解纤维素后所得溶液中再加酸时纤维素又可以沉淀析出,利用这种性质来制造人造丝。用硫酸铜溶液和氨水反应可以制得铜氨溶液。
,具有溶解纤维素的性能,在溶解纤维素后所得溶液中再加酸时纤维素又可以沉淀析出,利用这种性质来制造人造丝。用硫酸铜溶液和氨水反应可以制得铜氨溶液。
(1) 溶液呈蓝色是因为含有水合铜离子
溶液呈蓝色是因为含有水合铜离子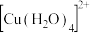 ,结构示意图如图所示:基态
,结构示意图如图所示:基态 原子核外电子排布式为
原子核外电子排布式为_______ 。
向 溶液中加入少量氨水,得到浅蓝色的碱式硫酸铜的沉淀;若继续加入氨水,沉淀溶解,得到深蓝色的含
溶液中加入少量氨水,得到浅蓝色的碱式硫酸铜的沉淀;若继续加入氨水,沉淀溶解,得到深蓝色的含 的铜氨溶液。
的铜氨溶液。
①比较键角:NH3_______ NH (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
②该实验中, 与
与 结合能力
结合能力_______ (填“大于”“小于”或“等于”) 与
与 结合能力,解释原因:
结合能力,解释原因:_______ 。
③经实验发现:金属铜与氨水和过氧化氢的混合溶液反应也可得到 。金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是
。金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是_______ ,反应的离子方应程式为_______ 。
(3)某种铜的氯化物晶胞形状为立方体,结构如图所示。
已知该晶胞的密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 。则该晶胞的边长为
。则该晶胞的边长为_______  (列出计算式)。
(列出计算式)。
 ,具有溶解纤维素的性能,在溶解纤维素后所得溶液中再加酸时纤维素又可以沉淀析出,利用这种性质来制造人造丝。用硫酸铜溶液和氨水反应可以制得铜氨溶液。
,具有溶解纤维素的性能,在溶解纤维素后所得溶液中再加酸时纤维素又可以沉淀析出,利用这种性质来制造人造丝。用硫酸铜溶液和氨水反应可以制得铜氨溶液。(1)
 溶液呈蓝色是因为含有水合铜离子
溶液呈蓝色是因为含有水合铜离子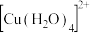 ,结构示意图如图所示:基态
,结构示意图如图所示:基态 原子核外电子排布式为
原子核外电子排布式为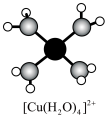
向
 溶液中加入少量氨水,得到浅蓝色的碱式硫酸铜的沉淀;若继续加入氨水,沉淀溶解,得到深蓝色的含
溶液中加入少量氨水,得到浅蓝色的碱式硫酸铜的沉淀;若继续加入氨水,沉淀溶解,得到深蓝色的含 的铜氨溶液。
的铜氨溶液。①比较键角:NH3
 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。②该实验中,
 与
与 结合能力
结合能力 与
与 结合能力,解释原因:
结合能力,解释原因:③经实验发现:金属铜与氨水和过氧化氢的混合溶液反应也可得到
 。金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是
。金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是(3)某种铜的氯化物晶胞形状为立方体,结构如图所示。
已知该晶胞的密度为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 。则该晶胞的边长为
。则该晶胞的边长为 (列出计算式)。
(列出计算式)。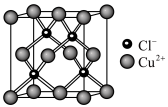
您最近一年使用:0次
2024·辽宁鞍山·二模
解题方法
9 . 某实验小组在探究 性质时,做了如下实验:
性质时,做了如下实验:
实验Ⅰ:向NaCl溶液中加入 溶液,溶液呈绿色。
溶液,溶液呈绿色。
实验Ⅱ:向 溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
实验Ⅲ:向 溶液中加入适量氨水,溶液变为深蓝色。
溶液中加入适量氨水,溶液变为深蓝色。
实验Ⅳ:向实验Ⅲ的深蓝色溶液中加入 溶液,产生蓝色沉淀。
溶液,产生蓝色沉淀。
资料显示: 为黄色,
为黄色, 为绿色不溶物。
为绿色不溶物。
下列说法错误的是
 性质时,做了如下实验:
性质时,做了如下实验:实验Ⅰ:向NaCl溶液中加入
 溶液,溶液呈绿色。
溶液,溶液呈绿色。实验Ⅱ:向
 溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。实验Ⅲ:向
 溶液中加入适量氨水,溶液变为深蓝色。
溶液中加入适量氨水,溶液变为深蓝色。实验Ⅳ:向实验Ⅲ的深蓝色溶液中加入
 溶液,产生蓝色沉淀。
溶液,产生蓝色沉淀。资料显示:
 为黄色,
为黄色, 为绿色不溶物。
为绿色不溶物。下列说法错误的是
A.实验Ⅰ: 在NaCl溶液中部分转化为 在NaCl溶液中部分转化为 |
B.实验Ⅱ:Mg消耗了溶液中的 从而产生了 从而产生了 |
C.实验Ⅲ:有 生成 生成 |
D.实验Ⅳ:获得的蓝色沉淀为 |
您最近一年使用:0次
10 . 某实验小组采用如下实验探究该依地酸铁钠(强化补铁剂)中铁元素的化合价。(已知:依地酸根是常见的配体,邻二氮菲可与 形成橙红色配合物)下列说法正确的是
形成橙红色配合物)下列说法正确的是
 形成橙红色配合物)下列说法正确的是
形成橙红色配合物)下列说法正确的是
| A.从现象②和③推测,依地酸铁钠中不含Fe(Ⅲ) |
| B.从现象②和⑤推测,依地酸铁钠中含Fe(Ⅱ) |
C.从现象①、②和③推测, 与 与 形成配合物的稳定性强于依地酸铁钠 形成配合物的稳定性强于依地酸铁钠 |
D.从现象①、④和⑤推测, 与邻二氮菲形成配合物的稳定性强于依地酸根 与邻二氮菲形成配合物的稳定性强于依地酸根 |
您最近一年使用:0次