1 . 向盛有硫酸铜溶液的试管里加入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象的说法中,正确的是
A.1 mol  含有的σ键数目为 含有的σ键数目为 |
B.沉淀溶解后,将生成深蓝色的配离子 |
C.在 中, 中, 给出孤电子对,NH3提供空轨道 给出孤电子对,NH3提供空轨道 |
D.向反应后的溶液中加入乙醇,溶液没有发生任何变化,因为 不与乙醇发生反应 不与乙醇发生反应 |
您最近一年使用:0次
名校
解题方法
2 . 科技强国,我国科学家在诸多领域取得新突破。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂 、
、 及清洗剂
及清洗剂 。
。
①基态F原子核外电子有_____ 种空间运动状态,下列为氟原子激发态的电子排布式的是_____ (填标号)。
A. B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为__________ 。
③氟硼酸铵( )中B的杂化方式为
)中B的杂化方式为__________ , 的空间构型为
的空间构型为__________ 。
(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是__________ (填元素符号),Mn原子的配位数为__________ ,CH3CN中 键与
键与 键数目之比为
键数目之比为__________ 。
(3)超导材料 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为__________ (列出计算式即可) 。
。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂
 、
、 及清洗剂
及清洗剂 。
。①基态F原子核外电子有
A.
 B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为
③氟硼酸铵(
 )中B的杂化方式为
)中B的杂化方式为 的空间构型为
的空间构型为(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是
 键与
键与 键数目之比为
键数目之比为(3)超导材料
 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为 。
。
您最近一年使用:0次
2024-04-11更新
|
295次组卷
|
5卷引用:2024届内蒙古锡林郭勒盟高三第三次模拟考试理综试卷-高中化学
2024届内蒙古锡林郭勒盟高三第三次模拟考试理综试卷-高中化学(已下线)化学(上海卷03)-2024年高考押题预测卷2024届青海省部分学校高三下学期模拟考试理综试题-高中化学2024届宁夏回族自治区石嘴山市平罗中学高三下学期模拟预测理综试题-高中化学(已下线)T16-结构与性质
3 . 用试管可以完成很多有趣的化学实验。下列说法不正确的是

A.①中出现的蓝色沉淀为 | B.②中生成了配位化合物 |
| C.③中出现的沉淀与①中不同 | D.⑤中发生了氧化还原反应 |
您最近一年使用:0次
2024-02-24更新
|
553次组卷
|
5卷引用:内蒙古师范大学锦山实验中学2023-2024学年高二下学期一调考试化学试题
4 . 下列物质不属于配合物的是
A. | B. | C. | D.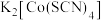 |
您最近一年使用:0次
名校
5 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.   中含有的 中含有的 键数目为 键数目为 |
B. 中 中 杂化的原子数目为 杂化的原子数目为 |
| C.30g分子式为CH2O的有机物含有的共价键数目为4NA |
D. 与足量AgNO3溶液反应最多生成3 mol AgCl沉淀 与足量AgNO3溶液反应最多生成3 mol AgCl沉淀 |
您最近一年使用:0次
解题方法
6 . 完成下列小题
(1)胆矾的结构可表示如下:

则胆矾晶体中含有_____ (填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键 E.氢键
(2)向硫酸铜溶液里逐滴加入氨水至生成的蓝色沉淀溶解,得到深蓝色的透明溶液,蓝色沉淀溶解的离子方程式为_____ ,该配离子中的配体跟水分子相比,_____ 较容易跟铜离子形成配位键,原因是_____ 。
(3)配合物 中,配位原子是
中,配位原子是_____ ,该配合物的结构式为_____ (标出配位键)该配合物中, 键与Π键的个数比为
键与Π键的个数比为_____ 。
(1)胆矾的结构可表示如下:

则胆矾晶体中含有
A.配位键 B.离子键 C.极性共价键 D.非极性共价键 E.氢键
(2)向硫酸铜溶液里逐滴加入氨水至生成的蓝色沉淀溶解,得到深蓝色的透明溶液,蓝色沉淀溶解的离子方程式为
(3)配合物
 中,配位原子是
中,配位原子是 键与Π键的个数比为
键与Π键的个数比为
您最近一年使用:0次
解题方法
7 . Fe、Cu、Cr都是第四周期过渡元素,回答下列问题。
(1)FeCl3是一种常用的净水剂,则Cl元素的原子核外有___________ 种不同能级的电子,基态Fe3+的电子排布式为___________ 。
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+,其中K4[Fe(CN)6]与Fe3+反应可得到一种蓝色沉淀KFe[Fe(CN)6],该物质晶胞的 结构如图所示(K+未画出),则一个晶胞中的K+个数为
结构如图所示(K+未画出),则一个晶胞中的K+个数为___________ 。

(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图,则该配离子中含有的化学键类型有___________ (填字母)。

a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有___________ 个σ键,C原子的杂化方式为___________ 。
(4)铜的晶胞为面心立方最密堆积,边长为 pm。则铜原子直径约为
pm。则铜原子直径约为___________ pm。
(1)FeCl3是一种常用的净水剂,则Cl元素的原子核外有
(2)实验室中可用KSCN或K4[Fe(CN)6]来检验Fe3+,其中K4[Fe(CN)6]与Fe3+反应可得到一种蓝色沉淀KFe[Fe(CN)6],该物质晶胞的
 结构如图所示(K+未画出),则一个晶胞中的K+个数为
结构如图所示(K+未画出),则一个晶胞中的K+个数为
(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图,则该配离子中含有的化学键类型有

a.配位键 b.极性键 c.离子键 d.非极性键
一个乙二胺分子中共有
(4)铜的晶胞为面心立方最密堆积,边长为
 pm。则铜原子直径约为
pm。则铜原子直径约为
您最近一年使用:0次
8 . 氢能源发展的关键环节是新型储氢材料,铁与组成的合金是目前已发现的储氢密度最高的储氢材料之一,回答下列问题:
(1)下列铁的外围电子排布图中,再失去一个电子需要能量最大的是_______ (填标号)。
A. B.
B.
C. D.
D.
基态Fe原子核电子排布式为_______ ;
(2)甘氨酸亚铁络合物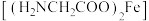 是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。
是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。
①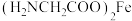 中含有第二周期元素的第一电离能由大到小的顺序为
中含有第二周期元素的第一电离能由大到小的顺序为_______ (用元素符号表示)。碳原子的杂化类型为_______ 。
② 分子中存在
分子中存在_______ 个 键和
键和_______ 个 键。
键。 分子是
分子是_______ 分子(填“极性”或“非极性”)。
③甘氨酸 的沸点比相同相对分子质量的烷烃大很多,原因是
的沸点比相同相对分子质量的烷烃大很多,原因是_______ ;
(3)硫酸亚铁( )可用于制造甘氨酸亚铁,
)可用于制造甘氨酸亚铁, 的空间构型为
的空间构型为_______ ,二聚体氯化铁分子结构对称,试写出二聚体氯化铁分子的结构_______ ;
(4)已知 的熔点为
的熔点为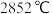 ,
, 的熔点为
的熔点为 ,
, 的熔点高于
的熔点高于 的原因是
的原因是_______ ;
(5)铁与镁组成的其中一种储氢合金的晶胞结构如图所示(晶胞的边长为dnm)。

①晶胞中铁原子的配位数为_______ ,
②图中a处原子的坐标参数为_______ ,合金的密度为_______  。
。
(1)下列铁的外围电子排布图中,再失去一个电子需要能量最大的是
A.
 B.
B.
C.
 D.
D.
基态Fe原子核电子排布式为
(2)甘氨酸亚铁络合物
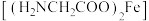 是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。
是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。①
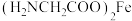 中含有第二周期元素的第一电离能由大到小的顺序为
中含有第二周期元素的第一电离能由大到小的顺序为②
 分子中存在
分子中存在 键和
键和 键。
键。 分子是
分子是③甘氨酸
 的沸点比相同相对分子质量的烷烃大很多,原因是
的沸点比相同相对分子质量的烷烃大很多,原因是(3)硫酸亚铁(
 )可用于制造甘氨酸亚铁,
)可用于制造甘氨酸亚铁, 的空间构型为
的空间构型为(4)已知
 的熔点为
的熔点为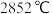 ,
, 的熔点为
的熔点为 ,
, 的熔点高于
的熔点高于 的原因是
的原因是(5)铁与镁组成的其中一种储氢合金的晶胞结构如图所示(晶胞的边长为dnm)。

①晶胞中铁原子的配位数为
②图中a处原子的坐标参数为
 。
。
您最近一年使用:0次
名校
解题方法
9 . 分子中含有两个或两个以上中心原子(离子)的配合物称为多核配合物,如图为Co(Ⅱ)双核配合物的内界,下列说法正确的是


A.图示结构中的氯元素为 ,则其含有极性键、非极性键和离子键 ,则其含有极性键、非极性键和离子键 |
B.配合物中的 原子的杂化方式是 原子的杂化方式是 、 、 |
C.每个中心离子的配位数为4,孤对电子全部由 原子提供 原子提供 |
| D.图示结构中所有微粒共平面 |
您最近一年使用:0次
2022-04-23更新
|
139次组卷
|
5卷引用:内蒙古霍林郭勒市第一中学2021-2022学年高二下学期第一次月考化学试题
内蒙古霍林郭勒市第一中学2021-2022学年高二下学期第一次月考化学试题湖南省天壹名校联盟2021-2022学年高二下学期3月大联考化学(B)试题浙江省台州市九校联盟2021-2022学年高二下学期期中考试化学试题(已下线)【2022】【高二下】【长河】【期中考】【高中化学】【徐外兰收集】山西省怀仁市第一中学校2022-2023学年高二下学期期末考试理综化学试题
名校
10 . 书写以下要求的表达式:
(1)过氧化钠的电子式_______ ;
(2)Ga原子核外电子排布式_______ ;
(3) 的原子结构示意图
的原子结构示意图_______ ;
(4)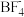 中心原子B的杂化方式为
中心原子B的杂化方式为_______ ;
(5) 分子空间构型为
分子空间构型为_______ ;
(6)准确书写向硫酸铜水溶液中滴加氨水至起初产生的沉淀溶解的原理(用离子反应方程式回答)
①_______ ;
②_______ ;
(1)过氧化钠的电子式
(2)Ga原子核外电子排布式
(3)
 的原子结构示意图
的原子结构示意图(4)
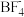 中心原子B的杂化方式为
中心原子B的杂化方式为(5)
 分子空间构型为
分子空间构型为(6)准确书写向硫酸铜水溶液中滴加氨水至起初产生的沉淀溶解的原理(用离子反应方程式回答)
①
②
您最近一年使用:0次



