解题方法
1 . 胆矾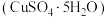 可写为
可写为 ,其结构示意图如图所示:
,其结构示意图如图所示:
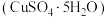 可写为
可写为 ,其结构示意图如图所示:
,其结构示意图如图所示: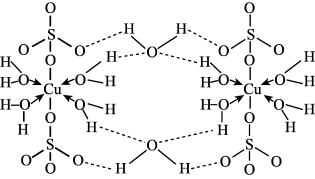
A.胆矾晶体中存在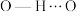 氢键 氢键 | B.胆矾晶体中 的配位数是4 的配位数是4 |
C.基态 的价层电子排布式为 的价层电子排布式为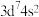 | D.五水硫酸铜晶体是一种含水混合物 |
您最近一年使用:0次
解题方法
2 . 根据下列实验操作及现象,所得结论错误的是
选项 | 实验操作及现象 | 结论\ |
A. | 向溶有 的 的 溶液中滴加 溶液中滴加 溶液,产生白色沉淀 溶液,产生白色沉淀 |  具有强氧化性 具有强氧化性 |
B. |  ,用 ,用 计测得 计测得 某一元酸(HR)溶液的 某一元酸(HR)溶液的 | HR为弱电解质 |
C. | 向 溶液中加入乙醇,析出深蓝色晶体 溶液中加入乙醇,析出深蓝色晶体 |  在水-乙醇混合溶剂中的溶解度较小 在水-乙醇混合溶剂中的溶解度较小 |
D. | 将 与 与 用导线相连,插入稀硫酸酸化的 用导线相连,插入稀硫酸酸化的 溶液,一段时间后,从 溶液,一段时间后,从 电极区取出少量溶液,滴入2滴 电极区取出少量溶液,滴入2滴 溶液,无明显现象 溶液,无明显现象 | Zn可以保护 不被腐蚀 不被腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-17更新
|
519次组卷
|
2卷引用:云南省罗平第一中学2024年高三二模考试化学试题
名校
解题方法
3 . 氮元素是重要的非金属元素,可形成多种铵盐、氮化物、叠氮化物及配合物等。
(1)基态氮原子价电子的轨道表示式(价电子排布图)为___________ ;第二周期元素原子中第一电离能大于氮原子的有___________ 种, 中阴离子的空间构型为
中阴离子的空间构型为___________ 。
(2)C、N、O、S四种元素中,电负性最大的是___________ 。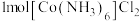 中含有σ键的数目为
中含有σ键的数目为___________ ;已知 比
比 的沸点低得多,试解释原因
的沸点低得多,试解释原因___________ 。
(3)含有多个配位原子的配体与同一中心离子(或原子)通过整合配位成环而形成的配合物为螯合物。一种 配合物的结构如图所示,1mol该螯合物中通过螯合作用形成的配位键有
配合物的结构如图所示,1mol该螯合物中通过螯合作用形成的配位键有___________ mol。 作简单立方堆积,两个立方体共用的面中心存在一个
作简单立方堆积,两个立方体共用的面中心存在一个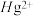 ,
, 位于立方体的体心,相邻的
位于立方体的体心,相邻的 的距离均为apm,阿伏加德罗常数的值为
的距离均为apm,阿伏加德罗常数的值为 ,该物质的化学式为
,该物质的化学式为___________ ,该晶体的密度为___________  。
。 可以与
可以与 、
、 等形成配合物。与
等形成配合物。与 互为等电子体且为非极性分子的化学式为
互为等电子体且为非极性分子的化学式为___________ 。在一定条件下铁形成的晶体的基本结构单元如图1和图2所示,则图1和图2的结构中铁原子的配位数之比为___________ ,两种晶体中空间利用率较高的是___________ 。(填“图1”或“图2”)
(1)基态氮原子价电子的轨道表示式(价电子排布图)为
 中阴离子的空间构型为
中阴离子的空间构型为(2)C、N、O、S四种元素中,电负性最大的是
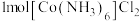 中含有σ键的数目为
中含有σ键的数目为 比
比 的沸点低得多,试解释原因
的沸点低得多,试解释原因(3)含有多个配位原子的配体与同一中心离子(或原子)通过整合配位成环而形成的配合物为螯合物。一种
 配合物的结构如图所示,1mol该螯合物中通过螯合作用形成的配位键有
配合物的结构如图所示,1mol该螯合物中通过螯合作用形成的配位键有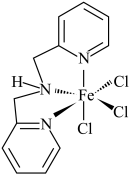
 作简单立方堆积,两个立方体共用的面中心存在一个
作简单立方堆积,两个立方体共用的面中心存在一个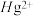 ,
, 位于立方体的体心,相邻的
位于立方体的体心,相邻的 的距离均为apm,阿伏加德罗常数的值为
的距离均为apm,阿伏加德罗常数的值为 ,该物质的化学式为
,该物质的化学式为 。
。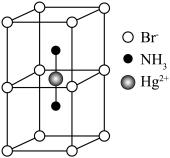
 可以与
可以与 、
、 等形成配合物。与
等形成配合物。与 互为等电子体且为非极性分子的化学式为
互为等电子体且为非极性分子的化学式为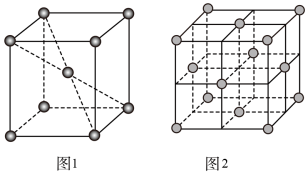
您最近一年使用:0次
4 . 近年来,人们发现 不仅在颜料、防腐工业等方面具有广泛的用途,而且
不仅在颜料、防腐工业等方面具有广泛的用途,而且 的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含
的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含 、
、 和
和 等)为原料制取
等)为原料制取 的工艺流程如下:
的工艺流程如下:
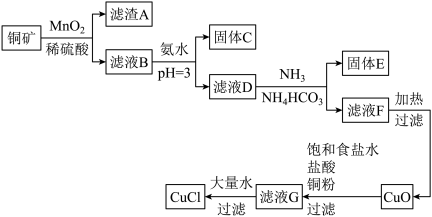
已知:i.水溶液中不存在碳酸铜,碳酸铜遇水立即水解为碱式碳酸铜和氢氧化铜。
ii.室温时, 的溶度积常数
的溶度积常数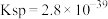 。
。
(1)铜矿中未被 氧化的物质有
氧化的物质有___________ 。
(2)滤液D中铁离子的浓度约为___________ 。
(3)向滤液D中先通氨气的目的是___________。
(4)固体E主要是 ,生成
,生成 的离子方程式是
的离子方程式是___________ 。
(5)滤液F加热生成 、
、 和
和 ,反应的化学方程式是
,反应的化学方程式是___________ 。
(6)若要制取99.5g ,理论上至少需要质量分数为25%的
,理论上至少需要质量分数为25%的 的铜矿粉的质量为
的铜矿粉的质量为___________ g。
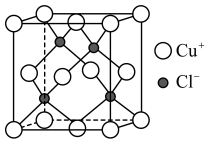
(7)查阅资料: 立方晶胞结构如下图所示,其晶胞参数为apm,
立方晶胞结构如下图所示,其晶胞参数为apm, 以配位键与
以配位键与 相结合,其中
相结合,其中 的配位数为
的配位数为___________ , 晶体密度为
晶体密度为___________  。
。
 不仅在颜料、防腐工业等方面具有广泛的用途,而且
不仅在颜料、防腐工业等方面具有广泛的用途,而且 的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含
的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含 、
、 和
和 等)为原料制取
等)为原料制取 的工艺流程如下:
的工艺流程如下:
已知:i.水溶液中不存在碳酸铜,碳酸铜遇水立即水解为碱式碳酸铜和氢氧化铜。
ii.室温时,
 的溶度积常数
的溶度积常数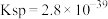 。
。(1)铜矿中未被
 氧化的物质有
氧化的物质有(2)滤液D中铁离子的浓度约为
(3)向滤液D中先通氨气的目的是___________。
A.中和溶液中的 | B.调节溶液 值,生成 值,生成 沉淀 沉淀 |
C.有利于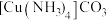 的生成 的生成 | D.增加 的溶解度 的溶解度 |
(4)固体E主要是
 ,生成
,生成 的离子方程式是
的离子方程式是(5)滤液F加热生成
 、
、 和
和 ,反应的化学方程式是
,反应的化学方程式是(6)若要制取99.5g
 ,理论上至少需要质量分数为25%的
,理论上至少需要质量分数为25%的 的铜矿粉的质量为
的铜矿粉的质量为(7)查阅资料:
 立方晶胞结构如下图所示,其晶胞参数为apm,
立方晶胞结构如下图所示,其晶胞参数为apm, 以配位键与
以配位键与 相结合,其中
相结合,其中 的配位数为
的配位数为 晶体密度为
晶体密度为 。
。
您最近一年使用:0次
5 . 热致变色是某些物质随温度变化而改变颜色的特性。某实验小组欲制备 并探究其溶液的颜色变化及热致变色现象。回答下列问题:
并探究其溶液的颜色变化及热致变色现象。回答下列问题:
(一)制备氯化铬晶体( )
)
主要步骤如下:
i.将铬酸钠(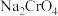 )、水、甲醇加入到如图所示装置中,升温至120℃,缓慢滴加盐酸进行反应,加完盐酸后于100℃进行熟化
)、水、甲醇加入到如图所示装置中,升温至120℃,缓慢滴加盐酸进行反应,加完盐酸后于100℃进行熟化 ,期间产生
,期间产生 气体,铬酸钠全部被还原。
气体,铬酸钠全部被还原。
ii.熟化后溶液用 中和至
中和至 为6.5~7.5,得到沉淀,过滤、洗涤。
为6.5~7.5,得到沉淀,过滤、洗涤。
iii.滤渣用足量盐酸溶解,经系列操作得到 。
。
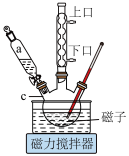
(1)仪器c的名称是_______ ;仪器b的冷凝水从_______ 进水(填“上口”或“下口”)。
(2)写出步骤i中反应的化学方程式:_______ 。
(3)步骤ⅲ中的系列操作为_______ ﹑_______ 、过滤、洗涤、干燥。
(二)探究氯化铬溶液的颜色变化及热致变色现象
(4)过渡元素的化合物往往呈现特殊颜色与d能级的电子数有关,铬的原子序数为24,基态铬原子的价层电子排布式为_______ ﹔文献报道 固体以配位化合物的形式存在,Cr(Ⅲ)的配位数为6.用
固体以配位化合物的形式存在,Cr(Ⅲ)的配位数为6.用 现配浓度为
现配浓度为 的溶液,溶液呈绿色,取
的溶液,溶液呈绿色,取 溶液滴加足量
溶液滴加足量 溶液,析出
溶液,析出 ,说明该绿色溶液中Cr(Ⅲ)的存在形式是下列中的
,说明该绿色溶液中Cr(Ⅲ)的存在形式是下列中的_______ (填标号)。
A.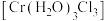 B.
B. C.
C. D.
D.
(5)上述现配的绿色溶液放置18小时后溶液呈墨绿色,放置7天以上后变为蓝色。取 该蓝色溶液滴加足量
该蓝色溶液滴加足量 溶液,析出
溶液,析出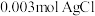 。另取少量蓝色溶液加热,颜色很快变为墨绿色再变至绿色,变化过程中Cr(Ⅲ)的配位数保持不变,该热致变色过程总反应的离子方程式为
。另取少量蓝色溶液加热,颜色很快变为墨绿色再变至绿色,变化过程中Cr(Ⅲ)的配位数保持不变,该热致变色过程总反应的离子方程式为_______ ﹔其正反应的
_______ 0(填“>”“<”或“=”)。
(6)经过探究,可推测该 晶体用配位化合物表示的化学式为
晶体用配位化合物表示的化学式为_______ 。
 并探究其溶液的颜色变化及热致变色现象。回答下列问题:
并探究其溶液的颜色变化及热致变色现象。回答下列问题:(一)制备氯化铬晶体(
 )
)主要步骤如下:
i.将铬酸钠(
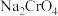 )、水、甲醇加入到如图所示装置中,升温至120℃,缓慢滴加盐酸进行反应,加完盐酸后于100℃进行熟化
)、水、甲醇加入到如图所示装置中,升温至120℃,缓慢滴加盐酸进行反应,加完盐酸后于100℃进行熟化 ,期间产生
,期间产生 气体,铬酸钠全部被还原。
气体,铬酸钠全部被还原。ii.熟化后溶液用
 中和至
中和至 为6.5~7.5,得到沉淀,过滤、洗涤。
为6.5~7.5,得到沉淀,过滤、洗涤。iii.滤渣用足量盐酸溶解,经系列操作得到
 。
。
(1)仪器c的名称是
(2)写出步骤i中反应的化学方程式:
(3)步骤ⅲ中的系列操作为
(二)探究氯化铬溶液的颜色变化及热致变色现象
(4)过渡元素的化合物往往呈现特殊颜色与d能级的电子数有关,铬的原子序数为24,基态铬原子的价层电子排布式为
 固体以配位化合物的形式存在,Cr(Ⅲ)的配位数为6.用
固体以配位化合物的形式存在,Cr(Ⅲ)的配位数为6.用 现配浓度为
现配浓度为 的溶液,溶液呈绿色,取
的溶液,溶液呈绿色,取 溶液滴加足量
溶液滴加足量 溶液,析出
溶液,析出 ,说明该绿色溶液中Cr(Ⅲ)的存在形式是下列中的
,说明该绿色溶液中Cr(Ⅲ)的存在形式是下列中的A.
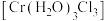 B.
B. C.
C. D.
D.
(5)上述现配的绿色溶液放置18小时后溶液呈墨绿色,放置7天以上后变为蓝色。取
 该蓝色溶液滴加足量
该蓝色溶液滴加足量 溶液,析出
溶液,析出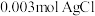 。另取少量蓝色溶液加热,颜色很快变为墨绿色再变至绿色,变化过程中Cr(Ⅲ)的配位数保持不变,该热致变色过程总反应的离子方程式为
。另取少量蓝色溶液加热,颜色很快变为墨绿色再变至绿色,变化过程中Cr(Ⅲ)的配位数保持不变,该热致变色过程总反应的离子方程式为
(6)经过探究,可推测该
 晶体用配位化合物表示的化学式为
晶体用配位化合物表示的化学式为
您最近一年使用:0次
名校
解题方法
6 . 298K时,向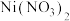 、
、 、
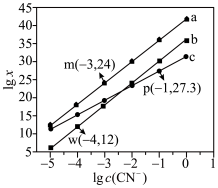
、 的混合液中滴加KCN溶液,混合液中lgx与
的混合液中滴加KCN溶液,混合液中lgx与 的关系如图所示,
的关系如图所示, 或
或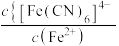 或
或 。下列叙述正确的是
。下列叙述正确的是
已知:①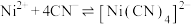
 ;
;
②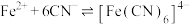
 ;
;
③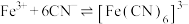
 ,且
,且 。
。
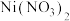 、
、 、
、 的混合液中滴加KCN溶液,混合液中lgx与
的混合液中滴加KCN溶液,混合液中lgx与 的关系如图所示,
的关系如图所示, 或
或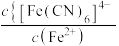 或
或 。下列叙述正确的是
。下列叙述正确的是
已知:①
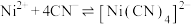
 ;
;②
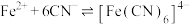
 ;
;③
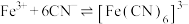
 ,且
,且 。
。A.直线c代表 与 与 的关系 的关系 |
B.根据图像可计算平衡常数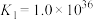 |
C.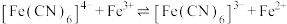 的平衡常数 的平衡常数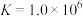 |
D.向含相同浓度的 和 和 的溶液中滴加KCN溶液,先生成 的溶液中滴加KCN溶液,先生成 |
您最近一年使用:0次
2024-02-25更新
|
272次组卷
|
4卷引用:云南省楚雄彝族自治州2023-2024学年高三上学期1月期末考试理综化学试题
名校
解题方法
7 . 下列装置与对应操作正确的是
 |  | 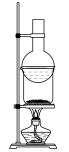 |  |
A.析出 晶体 晶体 | B.分离苯酚和水的混合物 | C.碘晶体(含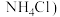 | D.测定 溶液的浓度 溶液的浓度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-10更新
|
429次组卷
|
3卷引用:云南省昆明市第三中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
8 . 邻二氮菲的结构简式为 ,简写为phen,遇
,简写为phen,遇 溶液生成橙红色配合物
溶液生成橙红色配合物 ,其中
,其中 的配位数为6。下列说法
的配位数为6。下列说法不正确 的是
 ,简写为phen,遇
,简写为phen,遇 溶液生成橙红色配合物
溶液生成橙红色配合物 ,其中
,其中 的配位数为6。下列说法
的配位数为6。下列说法| A.phen中,不含手性碳原子 |
B. 中,phen的一个N参与配位 中,phen的一个N参与配位 |
C. 中, 中, 提供空轨道,N提供孤对电子 提供空轨道,N提供孤对电子 |
D. 中,既存在极性键也存在非极性键 中,既存在极性键也存在非极性键 |
您最近一年使用:0次
2023-11-02更新
|
290次组卷
|
4卷引用:云南省大理白族自治州民族中学2023-2024学年高三上学期1月月考理综试卷
9 . 我国科学家开发了一种新型手性Ru(Ⅱ)—Pt(Ⅱ)双核配合物( )作为G—quadruplexDNA稳定剂和端粒酶抑制剂。手性Ru(Ⅱ)—Pt(Ⅱ)双核配合物的化学结构∆/A—RuPt和相关的单一核配合物(Pt和
)作为G—quadruplexDNA稳定剂和端粒酶抑制剂。手性Ru(Ⅱ)—Pt(Ⅱ)双核配合物的化学结构∆/A—RuPt和相关的单一核配合物(Pt和 )的结构如图所示。已知:在等价轨道上的电子排布采取全充满和半充满时,能量会较低,体系有更大的稳定性。下列说法正确的是
)的结构如图所示。已知:在等价轨道上的电子排布采取全充满和半充满时,能量会较低,体系有更大的稳定性。下列说法正确的是
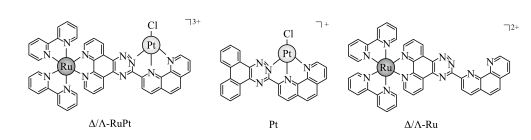
已知:Ru(Ⅱ)表示+2价Ru,Pt(Ⅱ)的配位数为4。
 )作为G—quadruplexDNA稳定剂和端粒酶抑制剂。手性Ru(Ⅱ)—Pt(Ⅱ)双核配合物的化学结构∆/A—RuPt和相关的单一核配合物(Pt和
)作为G—quadruplexDNA稳定剂和端粒酶抑制剂。手性Ru(Ⅱ)—Pt(Ⅱ)双核配合物的化学结构∆/A—RuPt和相关的单一核配合物(Pt和 )的结构如图所示。已知:在等价轨道上的电子排布采取全充满和半充满时,能量会较低,体系有更大的稳定性。下列说法正确的是
)的结构如图所示。已知:在等价轨道上的电子排布采取全充满和半充满时,能量会较低,体系有更大的稳定性。下列说法正确的是
已知:Ru(Ⅱ)表示+2价Ru,Pt(Ⅱ)的配位数为4。
A.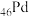 与 与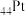 位于同一周期,基态Pd的价层电子排布式为 位于同一周期,基态Pd的价层电子排布式为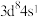 |
| B.单一核配合物Pt中的配位原子只有N原子 |
C. 中Ru原子与Pt原子的配位数相同 中Ru原子与Pt原子的配位数相同 |
D.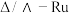 中Ru提供空轨道形成配位键 中Ru提供空轨道形成配位键 |
您最近一年使用:0次
2023-07-10更新
|
72次组卷
|
4卷引用:云南省楚雄彝族自治州2022-2023学年高二下学期期末考试化学试题
名校
解题方法
10 . 下列实验能达到目的的是
| 选项 | 目的 | 实验 |
| A | 实验室制备溴苯 | 将苯和溴的混合液加入装有FeBr3的圆底烧瓶中反应,反应后的混合液经碱溶液洗涤、结晶得到纯溴苯 |
| B | 配制0.20 mol ·L-1的NaOH溶液 | 称取2.0 g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至250 mL容量瓶定容 |
| C | 探究浓度对反应速率的影响 | 向2支盛有5 mL不同浓度Na2SO3溶液的试管中同时加入2 mL 5% H2O2溶液,观察实验现象 |
| D | 实验室制备[Cu(NH3)4]SO4·H2O | 向盛有CuSO4溶液的试管里滴加几滴氨水,产生蓝色沉淀,继续滴加氨水并振荡试管,沉淀溶解并得到深蓝色的透明溶液,加入乙醇后,析出深蓝色的晶体,过滤、洗涤、干燥 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



