名校
解题方法
1 . 科技强国,我国科学家在诸多领域取得新突破。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂 、
、 及清洗剂
及清洗剂 。
。
①基态F原子核外电子有_____ 种空间运动状态,下列为氟原子激发态的电子排布式的是_____ (填标号)。
A. B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为__________ 。
③氟硼酸铵( )中B的杂化方式为
)中B的杂化方式为__________ , 的空间构型为
的空间构型为__________ 。
(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是__________ (填元素符号),Mn原子的配位数为__________ ,CH3CN中 键与
键与 键数目之比为
键数目之比为__________ 。
(3)超导材料 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为__________ (列出计算式即可) 。
。
(1)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂
 、
、 及清洗剂
及清洗剂 。
。①基态F原子核外电子有
A.
 B.
B. C.
C. D.
D.
②C、N、O、F四种元素的第一电离能由大到小的顺序为
③氟硼酸铵(
 )中B的杂化方式为
)中B的杂化方式为 的空间构型为
的空间构型为(2)复兴号高铁车体材质用到了Mn、Co等元素。Mn的一种配合物的化学式为[Mn(CO)5(CH3CN)],CH3CN与Mn原子配位时,提供孤电子对的是
 键与
键与 键数目之比为
键数目之比为(3)超导材料
 具有
具有 型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为
型结构(如图),晶胞参数(晶胞边长)为a pm,该氮化钛晶体的密度为 。
。
您最近一年使用:0次
2024-04-11更新
|
313次组卷
|
6卷引用:2024届宁夏回族自治区石嘴山市平罗中学高三下学期模拟预测理综试题-高中化学
2024届宁夏回族自治区石嘴山市平罗中学高三下学期模拟预测理综试题-高中化学2024届内蒙古锡林郭勒盟高三第三次模拟考试理综试卷-高中化学(已下线)化学(上海卷03)-2024年高考押题预测卷2024届青海省部分学校高三下学期模拟考试理综试题-高中化学(已下线)T16-结构与性质四川省雅安市2023-2024学年高三下学期4月月考理综试题-高中化学
名校
解题方法
2 . 下列关于实验现象的解释或所得结论错误的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
 | 向某补血口服液中滴加几滴酸性KMnO4溶液 | 加入K3[Fe(CN)6]溶液出现蓝色沉淀 | 该补血口服液中含有Fe2+ |
 | 用蒸馏水溶解CuCl2固体,并继续加水稀释 | 溶液由绿色逐渐变为蓝色 | [CuCl4]2-+4H2O [Cu(H2O)4]2++4Cl-正向移动 [Cu(H2O)4]2++4Cl-正向移动 |
 | 将25℃0.1mol·L-1Na2SO3溶液加热到40℃,用传感器监测溶液pH变化 | 溶液的pH逐渐减小 | 温度升高,Na2SO3水解平衡正向移动 |
 | 比较次氯酸和醋酸的酸性强弱 | 室温下,用pH计测定同浓度的NaClO溶液和CH3COONa溶液pH | pH:NaClO>CH3COONa |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . Co元素的某些化合物在电池、光电材料、催化剂等方面有广泛应用。回答下列问题:
(1)一种具有光催化作用的配合物A结构简式如图所示:
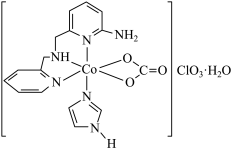
①基态Co原子价电子排布图为___________ 。
②外界 的空间构型为
的空间构型为___________ ,钴元素价态为___________ 。
③配合物A配位数为___________ ,中心离子的杂化方式为___________ (填标号)。
A.sp3 B.dsp2 C.d2sp3 D.sp3d
④咪唑( )具有类似苯环的结构,①号N比②号N更易与钴形成配位键的原因是
)具有类似苯环的结构,①号N比②号N更易与钴形成配位键的原因是_________ 。
(2)Co的一种化合物为六方晶系晶体,晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数体标。

已知晶胞含对称中心,其中1号氧原子的分数坐标为(0.6667,0.6667,0.6077),则2号氧原子的分数坐标为___________ ;NA为阿伏加德罗常数的值,该晶体的密度为___________ g/cm3(用计算式表示)。
(1)一种具有光催化作用的配合物A结构简式如图所示:

①基态Co原子价电子排布图为
②外界
 的空间构型为
的空间构型为③配合物A配位数为
A.sp3 B.dsp2 C.d2sp3 D.sp3d
④咪唑(
 )具有类似苯环的结构,①号N比②号N更易与钴形成配位键的原因是
)具有类似苯环的结构,①号N比②号N更易与钴形成配位键的原因是(2)Co的一种化合物为六方晶系晶体,晶胞结构如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数体标。

已知晶胞含对称中心,其中1号氧原子的分数坐标为(0.6667,0.6667,0.6077),则2号氧原子的分数坐标为
您最近一年使用:0次
2024-01-29更新
|
494次组卷
|
2卷引用:2023届宁夏回族自治区石嘴山市第三中学高三下学期第三次模拟考试理综试题
4 . 铁、钴、镍并称铁系元素,性质具有相似性。
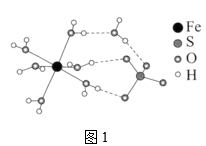
(1)FeSO4•7H2O结构如图1所示:该配合物中配离子的化学式为________ ,该晶体内部H2O与Fe2+、SO 和H2O的作用分别为
和H2O的作用分别为________ 和________ 。
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO________ FeO(填“<”或“>”),判断依据是________ 。
(3)某氮化铁的晶胞结构如图2所示:
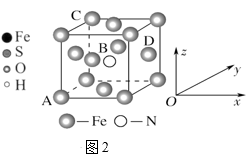
①原子坐标参数表示晶胞内部各原子的相对位置。如图所示晶胞中,原子坐标参数A为(0,0,0);B为( ,
, ,
, );C为(0,1,1)。则D原子的坐标参数为
);C为(0,1,1)。则D原子的坐标参数为________ 。
②若该晶体的密度是ρg•cm-3,则晶胞中两个最近的Fe的核间距为________ cm。(用含ρ的代数式表示,不必化简)
(1)FeSO4•7H2O结构如图1所示:该配合物中配离子的化学式为
 和H2O的作用分别为
和H2O的作用分别为
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO
(3)某氮化铁的晶胞结构如图2所示:

①原子坐标参数表示晶胞内部各原子的相对位置。如图所示晶胞中,原子坐标参数A为(0,0,0);B为(
 ,
, ,
, );C为(0,1,1)。则D原子的坐标参数为
);C为(0,1,1)。则D原子的坐标参数为②若该晶体的密度是ρg•cm-3,则晶胞中两个最近的Fe的核间距为
您最近一年使用:0次
5 . 化学式为K4[Fe(CN)6]的配合物常用作为抗结剂少量添加在食盐中,而KCN却是一种极具毒性的盐类,下列说法错误的是
| A.K4[Fe(CN)6]配合物在水中溶解并能完全解离出K+、Fe2+和CN- |
| B.K4[Fe(CN)6]配合物的配体是CN-,配位数是6,其晶体中有离子键、共价键和配位键 |
| C.[Fe(CN)6]4-配离子的中心离子Fe2+提供6个空轨道,配体CN-提供孤电子对 |
| D.KCN的剧毒性是由CN-引起 |
您最近一年使用:0次
6 . 某杂志报道了一种用磁场远程开启化学反应的方法,一种含铁化合物纳米粒子在其中发挥了重要作用。
(1)基态C原子的价层电子轨道表达式为_____ ;其核外电子占据的最高能级的电子云轮廓图形为_____ 。
(2)写出与NO 互为等电子体的一种分子和一种离子:
互为等电子体的一种分子和一种离子:_____ 。
(3)[Fe(CN)6]4-与硝酸反应的离子方程式为:[Fe(CN)6]4-+4H++NO =CO2↑+[Fe(CN)5(NO)]2-(红色)+NH
=CO2↑+[Fe(CN)5(NO)]2-(红色)+NH 。
。
①红色离子中所含非金属元素的第一电离能由大到小的顺序为_____ 。
②CN-与亚铁离子之间的作用力为_____ ;NO 、NH
、NH 中氮原子的杂化方式分别为
中氮原子的杂化方式分别为_____ 、_____ ,键角∠ONO_____ (填“>”或“<”)∠HNH。
(1)基态C原子的价层电子轨道表达式为
(2)写出与NO
 互为等电子体的一种分子和一种离子:
互为等电子体的一种分子和一种离子:(3)[Fe(CN)6]4-与硝酸反应的离子方程式为:[Fe(CN)6]4-+4H++NO
 =CO2↑+[Fe(CN)5(NO)]2-(红色)+NH
=CO2↑+[Fe(CN)5(NO)]2-(红色)+NH 。
。①红色离子中所含非金属元素的第一电离能由大到小的顺序为
②CN-与亚铁离子之间的作用力为
 、NH
、NH 中氮原子的杂化方式分别为
中氮原子的杂化方式分别为
您最近一年使用:0次
名校
7 . 向盛有少量CuCl2溶液的试管中滴入少量NaOH溶液,再滴入适量浓氨水,下列叙述不正确的是
| A.Cu(OH)2溶于浓氨水的离子方程式是Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH- |
| B.开始生成蓝色沉淀,加入过量氢氧化钠时,形成深蓝色溶液 |
| C.开始生成Cu(OH)2,之后生成更稳定的配合物 |
| D.开始生成蓝色沉淀,加入氨水后,沉淀溶解形成深蓝色溶液 |
您最近一年使用:0次
名校
8 . 向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解得到深蓝色透明溶液,若加入乙醇将析出深蓝色晶体。下列说法正确的是
A.反应后溶液中不存在任何沉淀,所以反应前后 的浓度保持不变 的浓度保持不变 |
B.在 离子中, 离子中, 提供空轨道, 提供空轨道, 提供孤对电子 提供孤对电子 |
C.1 mol  离子中含有 离子中含有 键 键 |
D.加入极性较小的溶剂乙醇后,将析出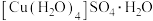 晶体 晶体 |
您最近一年使用:0次
2023-04-16更新
|
163次组卷
|
2卷引用:宁夏吴忠市吴忠中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
9 . 某化学小组设计如下实验制备铜的配合物。
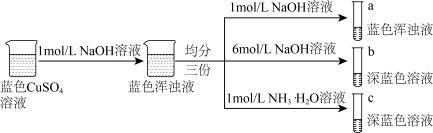
已知: 和
和 均为深蓝色
均为深蓝色
下列说法不正确的是

已知:
 和
和 均为深蓝色
均为深蓝色下列说法不正确的是
A.硫酸铜溶液呈蓝色的原因是 的颜色所致 的颜色所致 |
B. 与铜离子络合,形成配合物后H-N-H键角会变大 与铜离子络合,形成配合物后H-N-H键角会变大 |
C.由实验可知, 的配位能力比 的配位能力比 强 强 |
D.从b溶液得到的 晶体中,只存在配位键和极性共价键 晶体中,只存在配位键和极性共价键 |
您最近一年使用:0次
2023-04-14更新
|
107次组卷
|
2卷引用:宁夏银川一中2022-2023学年高二下学期期中考试化学试题
名校
10 . 按要求填空
(1)在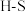 和H-Cl两种共价键中,键的极性较强的是
和H-Cl两种共价键中,键的极性较强的是___________ ,键长较长的是___________ 。
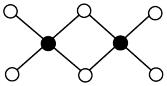
(2)氯化铝通常以双聚物存在,其结构如图所示。 该分子中含
该分子中含___________ 个配位键,该分子___________ (填“是”或“不是”)平面型分子。
(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色[Cu(NH3)4]SO4•H2O沉淀。
①写出上述实验前两步反应的离子方程式___________ ,___________ 。
②与NH3分子互为等电子体的一种阳离子是___________ 。
③在晶体[Cu(NH3)4]SO4•H2O中,中心原子是sp3杂化的原子有___________ (写元素符号),配离子(内界)中存在的化学键有___________ 。
a、离子键b、共价键c、配位键d、氢键e、范德华力
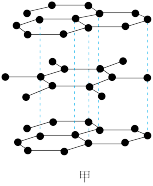
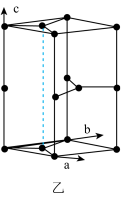
(4)图甲所示石墨晶体按ABAB方式堆积而成,图乙为石墨的六方晶胞。每个晶胞中的碳原子个数为___________ 。

(1)在
 和H-Cl两种共价键中,键的极性较强的是
和H-Cl两种共价键中,键的极性较强的是(2)氯化铝通常以双聚物存在,其结构如图所示。
 该分子中含
该分子中含(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色[Cu(NH3)4]SO4•H2O沉淀。
①写出上述实验前两步反应的离子方程式
②与NH3分子互为等电子体的一种阳离子是
③在晶体[Cu(NH3)4]SO4•H2O中,中心原子是sp3杂化的原子有
a、离子键b、共价键c、配位键d、氢键e、范德华力
(4)图甲所示石墨晶体按ABAB方式堆积而成,图乙为石墨的六方晶胞。每个晶胞中的碳原子个数为


您最近一年使用:0次



