名校
解题方法
1 . 乙二胺四乙酸(简称EDTA,可用 表示)在化学分析中常用于配位滴定。水溶液中,EDTA常以
表示)在化学分析中常用于配位滴定。水溶液中,EDTA常以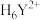 、
、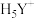 、
、 、
、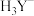 、
、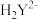 、
、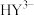 和
和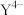 等7种形式存在。常温下,EDTA溶液中上述7种微粒的分布分数[如
等7种形式存在。常温下,EDTA溶液中上述7种微粒的分布分数[如 ]与溶液pH的关系如左图,图表示EDTA与某金属离子
]与溶液pH的关系如左图,图表示EDTA与某金属离子 形成的螯合物的结构。下列说法错误的是
形成的螯合物的结构。下列说法错误的是
 表示)在化学分析中常用于配位滴定。水溶液中,EDTA常以
表示)在化学分析中常用于配位滴定。水溶液中,EDTA常以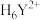 、
、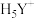 、
、 、
、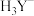 、
、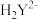 、
、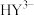 和
和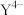 等7种形式存在。常温下,EDTA溶液中上述7种微粒的分布分数[如
等7种形式存在。常温下,EDTA溶液中上述7种微粒的分布分数[如 ]与溶液pH的关系如左图,图表示EDTA与某金属离子
]与溶液pH的关系如左图,图表示EDTA与某金属离子 形成的螯合物的结构。下列说法错误的是
形成的螯合物的结构。下列说法错误的是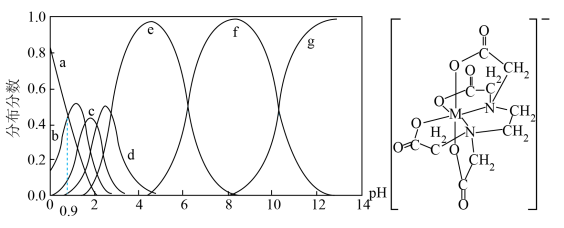
A.曲线d代表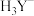 |
B. 时有 时有 |
| C.pH减小会降低EDTA与金属离子的配位能力 |
D. |
您最近一年使用:0次
昨日更新
|
113次组卷
|
3卷引用:江苏省部分学校2024届高三下学期高考模拟化学试题
2 . 砷化镓是一种高性能半导体材料,被广泛应用于光电子器件等领域。砷化镓立方晶胞(晶胞参数为 )如图1。下列说法正确的是
)如图1。下列说法正确的是
 )如图1。下列说法正确的是
)如图1。下列说法正确的是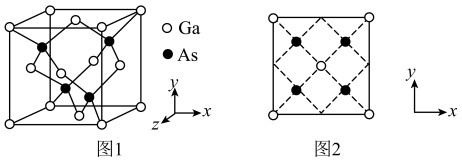
A. 的配位数为2 的配位数为2 | B.该晶胞沿z轴方向的平面投影如图2 |
| C.晶体中配位键占共价键总数的25% | D.晶胞中砷原子与镓原子间的最短距离为 |
您最近一年使用:0次
7日内更新
|
446次组卷
|
4卷引用:江苏省南京师范大学附属中学2024届高三下学期5月模拟化学试题
名校
解题方法
3 . 钌(Ru)的配合物在光电、催化、生物等领域备受关注,在[RuBr2(NH3)4]+中,Ru的化合价和配位数分别是
| A.+3和6 | B.+2和4 |
| C.+3和4 | D.+2和6 |
您最近一年使用:0次
名校
4 . 下列实验设计能达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 探究反应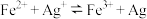 存在限度 存在限度 | 将0.1mol·L-1AgNO3溶液与0.21mol·L-1 溶液等体积混合后,取出两份混合液分别滴加KSCN溶液和 溶液等体积混合后,取出两份混合液分别滴加KSCN溶液和 溶液 溶液 |
| B | 探究浓度对反应速率的影响 | 向两支盛有5mL不同浓度KMnO4溶液的试管中分别加入同浓度同体积的足量草酸溶液,观察实验现象 |
| C | 检验某卤代烃中的是否含有氯元素 | 取卤代烃少许与NaOH乙醇溶液共热后,加入稀硝酸酸化,再加入AgNO3溶液,观察是否有白色沉淀生成 |
| D | 制备 晶体 晶体 | 向4mL0.1mol·L-1CuSO4溶液中滴加1mol·L-1氨水至沉淀溶解,再加入8mL95%乙醇,过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 烟气脱硝技术是烟气治理的发展方向和研究热点。
(1)用NH3选择性脱除氮氧化物,有如下反应:6NO(g)+4NH3(g)=5N2(g)+6H2O(g)
已知化学键的键能数据如下表:
则该反应的ΔH=___________ kJ/mol。
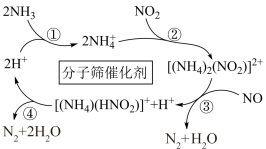
(2)利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如图所示。___________ 。
(3)以CuO-CeO2为活性物质、γ-Al2O3为载体的催化剂,可用于烟气中NOx的脱除。将吸附有Cu2+、Ce3+的Al(OH)3胶体煅烧可制得CuO-CeO2/γ-Al2O3催化剂。异丙醇铝Al[OCH(CH3)2]3加入到75℃水中,充分搅拌可生成Al(OH)3胶体。
①生成Al(OH)3胶体的化学方程式为___________ 。
②Al(OH)3胶体中,两分子Al(OH)3以配位键聚合成含四元环的二聚分子。该二聚分子的结构式为___________ (用“→”标出其中的配位键)
(4)以连二硫酸根(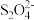 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:___________ 。
②NO吸收转化后的主要产物为 ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为___________ mL。
(1)用NH3选择性脱除氮氧化物,有如下反应:6NO(g)+4NH3(g)=5N2(g)+6H2O(g)
已知化学键的键能数据如下表:
| 化学键 | NO中的氮氧键 | N-H | N≡N | O-H |
| 键能(kJ/mol) | a | b | c | d |
(2)利用某分子筛作催化剂,NH3可脱除废气中的NO和NO2,生成两种无毒物质,其反应历程如图所示。
(3)以CuO-CeO2为活性物质、γ-Al2O3为载体的催化剂,可用于烟气中NOx的脱除。将吸附有Cu2+、Ce3+的Al(OH)3胶体煅烧可制得CuO-CeO2/γ-Al2O3催化剂。异丙醇铝Al[OCH(CH3)2]3加入到75℃水中,充分搅拌可生成Al(OH)3胶体。
①生成Al(OH)3胶体的化学方程式为
②Al(OH)3胶体中,两分子Al(OH)3以配位键聚合成含四元环的二聚分子。该二聚分子的结构式为
(4)以连二硫酸根(
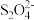 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示: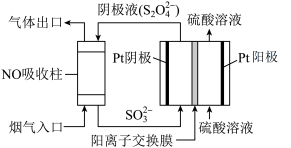
②NO吸收转化后的主要产物为
 ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标准状况下的体积为
您最近一年使用:0次
6 . 一种利用废铜渣(主要成分CuO,及少量 、
、 等杂质)制备超细铜粉的流程如下:
等杂质)制备超细铜粉的流程如下:
 、
、 等杂质)制备超细铜粉的流程如下:
等杂质)制备超细铜粉的流程如下:
A.“酸浸”所得滤渣的主要成分为 |
B.“沉铁”后所得滤液中含 |
| C.“沉铜”发生的反应为复分解反应 |
D.“转化”过程中Cu由 价降为0价 价降为0价 |
您最近一年使用:0次
7 . 填写下列空白:
(1)下列不属于配合物的是_______(填字母)。
(2)在配合离子[Fe(SCN)]2+中,提供空轨道接受孤电子对的微粒是_______ ,画出配合离子[Cu(NH3)4]2+中的配位键_______ 。
(1)下列不属于配合物的是_______(填字母)。
| A.[Cu(H2O)4]SO4·H2O | B.[Ag(NH3)2]OH |
| C.KAl(SO4)2·12H2O | D.Na[Al(OH)4] |
您最近一年使用:0次
8 . 第四周期过渡元素形成的化合物具有重要作用。黄铜( )用
)用 溶液浸泡后生成单质硫,所得
溶液浸泡后生成单质硫,所得 溶液可用于制取纳米
溶液可用于制取纳米 ,
, 能与酸发生反应。
能与酸发生反应。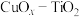 可用于低温下催化氧化HCHO:
可用于低温下催化氧化HCHO: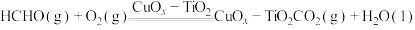 。
。 具有强氧化性,可与盐酸反应生成氯气。由
具有强氧化性,可与盐酸反应生成氯气。由 、
、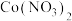 、
、 和
和 反应制备的配合物
反应制备的配合物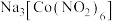 可应用于
可应用于 的鉴定。
的鉴定。
下列化学反应表示正确的是
 )用
)用 溶液浸泡后生成单质硫,所得
溶液浸泡后生成单质硫,所得 溶液可用于制取纳米
溶液可用于制取纳米 ,
, 能与酸发生反应。
能与酸发生反应。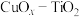 可用于低温下催化氧化HCHO:
可用于低温下催化氧化HCHO: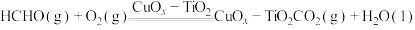 。
。 具有强氧化性,可与盐酸反应生成氯气。由
具有强氧化性,可与盐酸反应生成氯气。由 、
、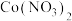 、
、 和
和 反应制备的配合物
反应制备的配合物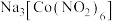 可应用于
可应用于 的鉴定。
的鉴定。下列化学反应表示正确的是
A. 与稀硫酸反应: 与稀硫酸反应: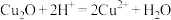 |
B. 溶液和 溶液和 反应: 反应: |
C. 与足量盐酸反应: 与足量盐酸反应: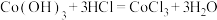 |
D.制备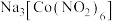 的反应: 的反应: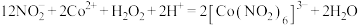 |
您最近一年使用:0次
9 . 碲广泛应用于冶金工业。以碲铜废料(主要含 )为原料回收碲单质的一种工艺流程如下:
)为原料回收碲单质的一种工艺流程如下:
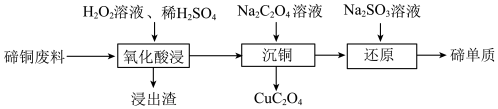
已知: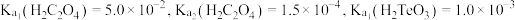 ,
,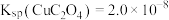 。
。
(1)“氧化酸浸”得到 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)“沉铜”时 过多会导致
过多会导致 与
与 生成环状结构的配离子
生成环状结构的配离子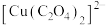 ,该配离子的结构式为
,该配离子的结构式为___________ (不考虑立体异构)
(3) 可溶于
可溶于 ,反应
,反应 的平衡常数为
的平衡常数为___________ 。[已知:反应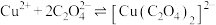 的平衡常数
的平衡常数 ]
]
(4)“还原”在 条件下进行,
条件下进行, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(5)“还原”时, 的实际投入量大于理论量,其可能的原因为
的实际投入量大于理论量,其可能的原因为___________ 。
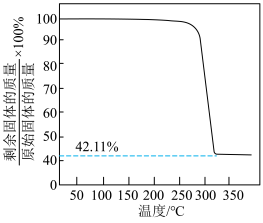
(6)将一定质量的 置于
置于 气中热解,测得剩余固体的质量与原始固体的质量的比值随温度变化的曲线如图所示。
气中热解,测得剩余固体的质量与原始固体的质量的比值随温度变化的曲线如图所示。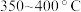 下剩余固体的化学式为
下剩余固体的化学式为___________ 。
 )为原料回收碲单质的一种工艺流程如下:
)为原料回收碲单质的一种工艺流程如下:
已知:
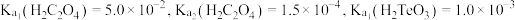 ,
,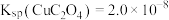 。
。(1)“氧化酸浸”得到
 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(2)“沉铜”时
 过多会导致
过多会导致 与
与 生成环状结构的配离子
生成环状结构的配离子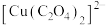 ,该配离子的结构式为
,该配离子的结构式为(3)
 可溶于
可溶于 ,反应
,反应 的平衡常数为
的平衡常数为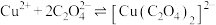 的平衡常数
的平衡常数 ]
](4)“还原”在
 条件下进行,
条件下进行, 发生反应的离子方程式为
发生反应的离子方程式为(5)“还原”时,
 的实际投入量大于理论量,其可能的原因为
的实际投入量大于理论量,其可能的原因为(6)将一定质量的
 置于
置于 气中热解,测得剩余固体的质量与原始固体的质量的比值随温度变化的曲线如图所示。
气中热解,测得剩余固体的质量与原始固体的质量的比值随温度变化的曲线如图所示。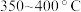 下剩余固体的化学式为
下剩余固体的化学式为
您最近一年使用:0次
名校
10 . 电极活性物质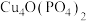 的制备,可通过下列反应制备:
的制备,可通过下列反应制备: 。
。
(1)上述反应涉及的元素中不属于元素周期表p区元素的是___________ ,写出基态 的电子排布式
的电子排布式___________ 。
(2)P、S元素第一电离能大小关系为P___________ S(填“>”、“<”或“=”),原因是___________ 。
(3)O的原子核外有___________ 种不同能量的电子,其氢化物沸点高于同族元素H2S的原因是___________ 。
(4)CuSO4溶液中逐滴加入氨水,先产生蓝色沉淀,后又溶解得到深蓝色溶液 ,加入乙醇后有深蓝色沉淀析出,关于该深蓝色物质的说法错误的是
,加入乙醇后有深蓝色沉淀析出,关于该深蓝色物质的说法错误的是___________ 。
A.该物质正离子的中心是Cu原子 B.该配合物的配体数等于配位数
C.外界离子的中心原子的杂化方式为sp3 D.乙醇的作用是将配合物转化为
写出沉淀溶解生成深蓝色溶液的离子方程式___________ 。
(5)①在硫酸铜溶液中加入过量KCN,生成配合物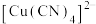 ,则1 mol该配合物含π键的数目为
,则1 mol该配合物含π键的数目为___________ 。
②画出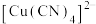 的结构:
的结构:___________ (用“→”或“—”将配位键表示出来)。
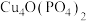 的制备,可通过下列反应制备:
的制备,可通过下列反应制备: 。
。(1)上述反应涉及的元素中不属于元素周期表p区元素的是
 的电子排布式
的电子排布式(2)P、S元素第一电离能大小关系为P
(3)O的原子核外有
(4)CuSO4溶液中逐滴加入氨水,先产生蓝色沉淀,后又溶解得到深蓝色溶液
 ,加入乙醇后有深蓝色沉淀析出,关于该深蓝色物质的说法错误的是
,加入乙醇后有深蓝色沉淀析出,关于该深蓝色物质的说法错误的是A.该物质正离子的中心是Cu原子 B.该配合物的配体数等于配位数
C.外界离子的中心原子的杂化方式为sp3 D.乙醇的作用是将配合物转化为

写出沉淀溶解生成深蓝色溶液的离子方程式
(5)①在硫酸铜溶液中加入过量KCN,生成配合物
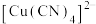 ,则1 mol该配合物含π键的数目为
,则1 mol该配合物含π键的数目为②画出
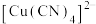 的结构:
的结构:
您最近一年使用:0次



