名校
解题方法
1 . Pt(NH3)2Cl2存在两种异构体,抗癌药物顺铂可由以下途径得到,下列说法错误 的是
 (顺铂)
(顺铂)
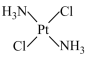 (反铂)
(反铂)
| A.Pt(NH3)2Cl2中Pt采用的杂化方式为sp3 |
| B.过程②说明Cl对位上的Cl更容易被NH3取代 |
| C.该变化过程说明NH3的配位能力大于Cl- |
| D.相同条件下,反铂在苯中的溶解度大于顺铂 |
您最近一年使用:0次
解题方法
2 . 下列实验探究方案能达到探究目的的是
选项 | 探究方案 | |
A | 向 溶液中加入少量 溶液中加入少量 固体,振荡,溶液由蓝色变为黄绿色 固体,振荡,溶液由蓝色变为黄绿色 |  中的配位键稳定性大于 中的配位键稳定性大于 中的配位键 中的配位键 |
B | 向 溶液中滴加淀粉溶液,再通入 溶液中滴加淀粉溶液,再通入 气体,观察现象 气体,观察现象 | 比较 与 与 氧化性的强弱 氧化性的强弱 |
C | 向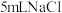 和 和 的混合溶液中,滴加12滴 的混合溶液中,滴加12滴 溶液,观察沉淀颜色 溶液,观察沉淀颜色 | 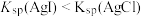 |
D | 向2支分别盛有 不同浓度 不同浓度 溶液的试管中,同时加入 溶液的试管中,同时加入 溶液 溶液 | 探究反应物㳖度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 .  为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 固体中含 固体中含 个阴离子 个阴离子 |
B. 分子式为 分子式为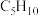 的烃可能含 的烃可能含 个 个 键 键 |
C.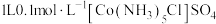 溶液中含 溶液中含 个 个 |
D.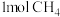 与 与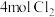 混合光照反应可生成 混合光照反应可生成 个 个 |
您最近一年使用:0次
4 . 由辉铜矿(含 ,少量
,少量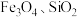 )合成
)合成 的流程如下。
的流程如下。 时,
时, ,
,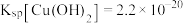 ,离子浓度
,离子浓度 时可认为离子完全沉淀。下列说法正确的是
时可认为离子完全沉淀。下列说法正确的是
 ,少量
,少量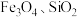 )合成
)合成 的流程如下。
的流程如下。
 时,
时, ,
,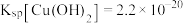 ,离子浓度
,离子浓度 时可认为离子完全沉淀。下列说法正确的是
时可认为离子完全沉淀。下列说法正确的是A.煅烧时只有 两种元素被氧化 两种元素被氧化 |
B.酸浸后,滤液的主要成分为 和 和 |
C.调 为 为 时,可实现铜、铁的分离 时,可实现铜、铁的分离 |
D. 乙醇的作用为增大 乙醇的作用为增大 的溶解度 的溶解度 |
您最近一年使用:0次
名校
解题方法
5 . 蓝铜矿的主要成分为2CuCO3·Ca(OH)2,将它与焦炭一起加热可以生成Cu、CO2和H2O。下列说法正确的是
| A.Cu是第四周期第ⅦB族元素 |
| B.0.1mol[Cu(H2O)4]2+中所含配位键的物质的量为0.8mol |
| C.电负性:O>C>H |
| D.将0.1L0.1mol/L[Cu(NH3)4](OH)2加入足量的MgCl2溶液中,理论上可得到0.2molMg(OH)2 |
您最近一年使用:0次
解题方法
6 . 根据下列实验操作及现象,所得结论错误的是
选项 | 实验操作及现象 | 结论\ |
A. | 向溶有 的 的 溶液中滴加 溶液中滴加 溶液,产生白色沉淀 溶液,产生白色沉淀 |  具有强氧化性 具有强氧化性 |
B. |  ,用 ,用 计测得 计测得 某一元酸(HR)溶液的 某一元酸(HR)溶液的 | HR为弱电解质 |
C. | 向 溶液中加入乙醇,析出深蓝色晶体 溶液中加入乙醇,析出深蓝色晶体 |  在水-乙醇混合溶剂中的溶解度较小 在水-乙醇混合溶剂中的溶解度较小 |
D. | 将 与 与 用导线相连,插入稀硫酸酸化的 用导线相连,插入稀硫酸酸化的 溶液,一段时间后,从 溶液,一段时间后,从 电极区取出少量溶液,滴入2滴 电极区取出少量溶液,滴入2滴 溶液,无明显现象 溶液,无明显现象 | Zn可以保护 不被腐蚀 不被腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-17更新
|
519次组卷
|
2卷引用:河北省重点高中2023-2024学年高三下学期第三次模拟化学试题
解题方法
7 . 下列实验方案能达到实验目的的是
选项 | 实验方案 | 实验目的 |
A | 在饱和 | 制备 |
B | 在 | 证明异丙醇的极性比水的弱 |
C | 在酸性 | 探究醛基的还原性 |
D | 测定同浓度的 | 探究 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 已知A、B、C、D、E、F、G都是元素周期表中前四周期的元素,它们的原子序数依次增大。A是宇宙中含量最丰富的元素,B、D原子的 层有2个未成对电子。
层有2个未成对电子。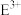 离子
离子 层
层 轨道电子为半满状态,
轨道电子为半满状态, 比
比 原子序数大1且位于同一族,
原子序数大1且位于同一族, 的最外层只有1个电子。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
的最外层只有1个电子。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)B、C、D的第一电离能由小到大的顺序为_____ 。
(2)A、B、D三种元素可以形成组成为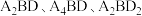 的分子,其中B原子采取
的分子,其中B原子采取 杂化的是
杂化的是_____ (填结构简式)
(3) 可形成分子式均为
可形成分子式均为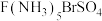 的两种配合物,其中一种化学式为
的两种配合物,其中一种化学式为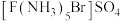 往其溶液中加
往其溶液中加 溶液时,现象是
溶液时,现象是_____ ;往另一种配合物的溶液中加入 溶液时,无明显现象,若加入
溶液时,无明显现象,若加入 溶液时产生淡黄色沉淀,则第二种配合物的化学式为
溶液时产生淡黄色沉淀,则第二种配合物的化学式为_____ 。
(4)B元素在自然界有多种同素异形体,硬度最大晶体中每个晶胞中平均含有_____ 个 原子。若晶胞的棱长为
原子。若晶胞的棱长为 ,则它的密度为
,则它的密度为_____  (
( 表示阿伏加德罗常数)
表示阿伏加德罗常数)
(5)G的一种氧化物M的晶胞结构如图所示(浅灰球代表氧原子),则M的化学式为_____ ,该晶体中氧原子的配位数为_____ 。
 层有2个未成对电子。
层有2个未成对电子。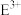 离子
离子 层
层 轨道电子为半满状态,
轨道电子为半满状态, 比
比 原子序数大1且位于同一族,
原子序数大1且位于同一族, 的最外层只有1个电子。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
的最外层只有1个电子。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)(1)B、C、D的第一电离能由小到大的顺序为
(2)A、B、D三种元素可以形成组成为
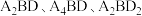 的分子,其中B原子采取
的分子,其中B原子采取 杂化的是
杂化的是(3)
 可形成分子式均为
可形成分子式均为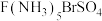 的两种配合物,其中一种化学式为
的两种配合物,其中一种化学式为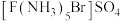 往其溶液中加
往其溶液中加 溶液时,现象是
溶液时,现象是 溶液时,无明显现象,若加入
溶液时,无明显现象,若加入 溶液时产生淡黄色沉淀,则第二种配合物的化学式为
溶液时产生淡黄色沉淀,则第二种配合物的化学式为(4)B元素在自然界有多种同素异形体,硬度最大晶体中每个晶胞中平均含有
 原子。若晶胞的棱长为
原子。若晶胞的棱长为 ,则它的密度为
,则它的密度为 (
( 表示阿伏加德罗常数)
表示阿伏加德罗常数)(5)G的一种氧化物M的晶胞结构如图所示(浅灰球代表氧原子),则M的化学式为

您最近一年使用:0次
9 . 向AgBr饱和溶液(有足量AgBr固体)中滴加Na2S2O3溶液,发生反应Ag++
 [Ag(
[Ag( )]-和[Ag(
)]-和[Ag( )]-+
)]-+
 [Ag(
[Ag( )2]3-, lg[c(M)/(mol/L)、lgc(N)与lg[c(
)2]3-, lg[c(M)/(mol/L)、lgc(N)与lg[c( )/mol/L)的关系如下图所示(其中M代表Ag+或Br-;N代表
)/mol/L)的关系如下图所示(其中M代表Ag+或Br-;N代表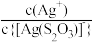 或
或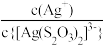 ):
):

 [Ag(
[Ag( )]-和[Ag(
)]-和[Ag( )]-+
)]-+
 [Ag(
[Ag( )2]3-, lg[c(M)/(mol/L)、lgc(N)与lg[c(
)2]3-, lg[c(M)/(mol/L)、lgc(N)与lg[c( )/mol/L)的关系如下图所示(其中M代表Ag+或Br-;N代表
)/mol/L)的关系如下图所示(其中M代表Ag+或Br-;N代表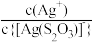 或
或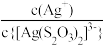 ):
):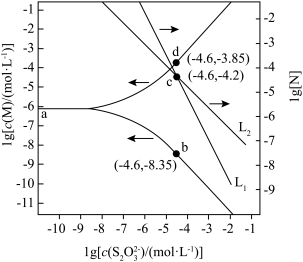
A.直线L1表示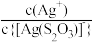 随 随 浓度变化的关系 浓度变化的关系 |
| B.AgBr的溶度积常数Ksp=c(Ag+)c(Br-)=10-12.2 |
C.反应AgBr+2  [Ag( [Ag( )2]3-+Br-的平衡常数K的值为101.2 )2]3-+Br-的平衡常数K的值为101.2 |
D.c( )= 0.001 mol/L时,溶液中c(Br-)>c{[Ag( )= 0.001 mol/L时,溶液中c(Br-)>c{[Ag( )2]3-}>c{[Ag(S2O3)]-} )2]3-}>c{[Ag(S2O3)]-} |
您最近一年使用:0次
2024-04-13更新
|
460次组卷
|
5卷引用:河北省石家庄市2024届高三下学期4月第二次质检化学试题
河北省石家庄市2024届高三下学期4月第二次质检化学试题河北省名校联盟2024届高三下学期4月第二次联考化学试题 (已下线)选择题11-142024届黑龙江省哈尔滨市第九中学高三下学期第四次模拟考试化学试卷(已下线)选择题11-15
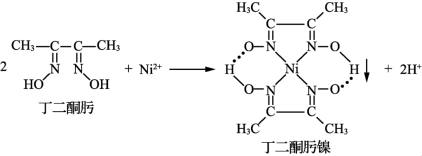
10 . 配位化合物广泛应用于日常生活、工业生产及科研中。例如Ni2+与丁二酮肟生成鲜红色的丁二酮肟镍沉淀,该反应可用于检验Ni2+。
(1)丁二酮肟镍是否属于螯合物___________ (填“是”或“否”),其配位数为___________ ,含有化学键的类型有___________ 。
a.氢键 b.配位键 c.极性键 d.非极性键
(2)绝大部分过渡金属都能与CO分子形成稳定的羰基配合物,金属羰基配合物中每个CO提供一对电子与金属原子形成配位键,且配位键的形成可使金属价层电子满足18电子规律,即中心原子的价电子数+配体提供的总电子数=18,则Fe(CO)x中Fe的配位数x的数值为___________ 。
(3)Cr3+配位能力很强,极易形成配位数为6的八面体结构,例如CrCl3∙6H2O就有3种水合异构体,其中一种结构取1mol与足量的AgNO3溶液反应,生成2mol白色沉淀,则该配合物的化学式为___________ 。
(4)[Ni(NH3)4]2+具有对称的空间构型,[Ni(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,中心离子Ni2+的杂化方式可能为___________ 。
a.sp3 b.dsp2 c.sp2 d.sp
(5)物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是___________。
(1)丁二酮肟镍是否属于螯合物
a.氢键 b.配位键 c.极性键 d.非极性键
(2)绝大部分过渡金属都能与CO分子形成稳定的羰基配合物,金属羰基配合物中每个CO提供一对电子与金属原子形成配位键,且配位键的形成可使金属价层电子满足18电子规律,即中心原子的价电子数+配体提供的总电子数=18,则Fe(CO)x中Fe的配位数x的数值为
(3)Cr3+配位能力很强,极易形成配位数为6的八面体结构,例如CrCl3∙6H2O就有3种水合异构体,其中一种结构取1mol与足量的AgNO3溶液反应,生成2mol白色沉淀,则该配合物的化学式为
(4)[Ni(NH3)4]2+具有对称的空间构型,[Ni(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,中心离子Ni2+的杂化方式可能为
a.sp3 b.dsp2 c.sp2 d.sp
(5)物质在外磁场的作用下会发生磁化现象,在磁场中物质的磁性可分为顺磁性、反磁性和铁磁性,中心离子或原子上含有未成对电子的物质具有顺磁性,下列配离子中具有顺磁性的是___________。
| A.[Cr(OH)4]- | B.[Cu(CN)4]3− | C.[ZnCl4]2− | D.[Fe(CN)6]4− |
您最近一年使用:0次

 溶液中加入
溶液中加入 粉末
粉末 胶体
胶体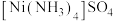 溶液中加入异丙醇
溶液中加入异丙醇 溶液中滴加苯乙醛
溶液中滴加苯乙醛 、NaY溶液的pH
、NaY溶液的pH 、HY的酸性强弱
、HY的酸性强弱

