名校
解题方法
1 . 铝和氟的化合物在制造、化工等领域都有广泛应用。回答下列问题:
(1)基态铝原子的核外电子排布式为___________ ,占据最高能级的电子云轮廓图形状为___________ 。
(2)通常情况下, 可由六氟铝酸铵
可由六氟铝酸铵 受热分解制得,请写出该反应的化学方程式:
受热分解制得,请写出该反应的化学方程式:___________ 。
(3) 具有较高的熔点(1040℃),属于
具有较高的熔点(1040℃),属于___________ (填晶体类型)晶体; 在178℃时升华,写出
在178℃时升华,写出 、
、 晶体类型不同的原因
晶体类型不同的原因___________ (从原子结构与元素性质的角度作答)。
(4) 在水溶液中实际上是以
在水溶液中实际上是以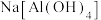 的形式存在。其中
的形式存在。其中 为配离子,Al原子的杂化方式为
为配离子,Al原子的杂化方式为___________ ,该阴离子中存在的化学键有___________ (填字母)。
A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(5)萤石( )晶体的晶胞如图所示,已知立方体边长为
)晶体的晶胞如图所示,已知立方体边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为___________  (列出计算式)。
(列出计算式)。
(1)基态铝原子的核外电子排布式为
(2)通常情况下,
 可由六氟铝酸铵
可由六氟铝酸铵 受热分解制得,请写出该反应的化学方程式:
受热分解制得,请写出该反应的化学方程式:(3)
 具有较高的熔点(1040℃),属于
具有较高的熔点(1040℃),属于 在178℃时升华,写出
在178℃时升华,写出 、
、 晶体类型不同的原因
晶体类型不同的原因(4)
 在水溶液中实际上是以
在水溶液中实际上是以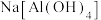 的形式存在。其中
的形式存在。其中 为配离子,Al原子的杂化方式为
为配离子,Al原子的杂化方式为A.离子键 B.极性键 C.非极性键 D.金属键 E.配位键 F.氢键
(5)萤石(
 )晶体的晶胞如图所示,已知立方体边长为
)晶体的晶胞如图所示,已知立方体边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则
,则 晶体的密度为
晶体的密度为 (列出计算式)。
(列出计算式)。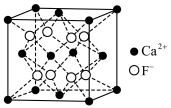
您最近一年使用:0次
2024-03-05更新
|
552次组卷
|
3卷引用:新疆阿克苏市实验中学2022-2023学年高二下学期第三次月考化学试题
名校
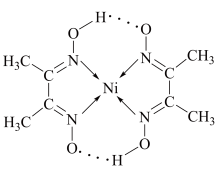
2 . 丁二酮肟常用于检验 。在稀氨水中,丁二酮肟与
。在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示。下列说法不正确的是
反应生成鲜红色沉淀,其结构如图所示。下列说法不正确的是
 。在稀氨水中,丁二酮肟与
。在稀氨水中,丁二酮肟与 反应生成鲜红色沉淀,其结构如图所示。下列说法不正确的是
反应生成鲜红色沉淀,其结构如图所示。下列说法不正确的是
A. 的配位数为4 的配位数为4 |
| B.该物质中碳原子采用sp2、sp3杂化 |
| C.该结构中仅存在极性键、配位键和氢键 |
| D.丁二酮肟中,第一电离能为N>O>C |
您最近一年使用:0次
名校
解题方法
3 . 碳铂(结构简式如图)是一种广谱抗癌药物。下列关于碳铂的说法错误的是


| A.中心原子的配位数为4 | B. 和 和 杂化的碳原子数之比为 杂化的碳原子数之比为 |
C.分子中σ键与π键的数目之比为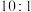 | D.分子中含有极性键、非极性键和配位键 |
您最近一年使用:0次
2024-02-10更新
|
212次组卷
|
7卷引用:新疆乌鲁木齐市第六十八中学2023-2024学年高三上学期1月月考化学试题
新疆乌鲁木齐市第六十八中学2023-2024学年高三上学期1月月考化学试题山东省枣庄市2021-2022学年高三高考适应性练习(一)化学试题(已下线)微专题50 分子的立体结构的判断-备战2023年高考化学一轮复习考点微专题山东省淄博实验中学2022-2023学年高二下学期3月月考化学试题陕西省咸阳市实验中学2023-2024学年高二上学期段性检测(一)化学试题湖南省张家界市慈利县第一中学2022-2023学年高三上学期第四次月考化学试卷(已下线)3.4.1 配合物与超分子(基础)
4 . 向由0.1molCoCl3·6H2O配成的溶液中加入足量AgNO3溶液,产生0.2mol沉淀。配合物CoCl3·6H2O的配位数为6,下列说法错误的是
A.该配合物的中心离子是 |
B.该配合物的配体是H2O和 |
C.每1mol配离子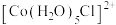 中含有6NA个共价键 中含有6NA个共价键 |
| D.该配合物中存在的化学键有:共价键、配位键、离子键 |
您最近一年使用:0次
5 . 向盛有 溶液的试管中滴加氨水,先形成绿色沉淀,继续滴加氨水,沉淀溶解得到
溶液的试管中滴加氨水,先形成绿色沉淀,继续滴加氨水,沉淀溶解得到 蓝色溶液。下列说法错误的是
蓝色溶液。下列说法错误的是
 溶液的试管中滴加氨水,先形成绿色沉淀,继续滴加氨水,沉淀溶解得到
溶液的试管中滴加氨水,先形成绿色沉淀,继续滴加氨水,沉淀溶解得到 蓝色溶液。下列说法错误的是
蓝色溶液。下列说法错误的是A.在 中, 中, 给出孤对电子, 给出孤对电子, 接受电子对 接受电子对 |
B.因为形成 ,所以反应后 ,所以反应后 的浓度减小 的浓度减小 |
C.在 中,中心原子的配位数为6,N为配位原子 中,中心原子的配位数为6,N为配位原子 |
D.在 中,阴离子的空间结构为正四面体形 中,阴离子的空间结构为正四面体形 |
您最近一年使用:0次
解题方法
6 . 下列说法中不正确的是
| A.ABn型分子中,若中心原子没有孤对电子,则ABn为空间对称结构,属于非极性分子 |
| B.NH3、H2O、CH4分子中的N、O、C原子均是采取sp3杂化的 |
| C.NH3、H2O、CH4分子的几何构型均为三角锥形 |
| D.配合物[Cu(H2O)4]SO4中,中心离子是Cu2+,配体是H2O,配位数是4 |
您最近一年使用:0次
2023-05-10更新
|
192次组卷
|
2卷引用:新疆维吾尔自治区塔城地区2022-2023学年高二下学期5月期中化学试题
名校
7 .  是重要的化工原料,可用于某些配合物的制备,如
是重要的化工原料,可用于某些配合物的制备,如 溶于氨水形成
溶于氨水形成 。液氨可以微弱的电离产生
。液氨可以微弱的电离产生 和
和 ,
, 中的一个H原子若被
中的一个H原子若被 取代可形成
取代可形成 (联氨),若被
(联氨),若被 取代可形成
取代可形成 (羟胺)。
(羟胺)。 经过转化可形成
经过转化可形成 、
、 、
、 、
、 (无色)
(无色) 等。
等。 与
与 反应有气体生成,同时放出大量热。下列说法正确的是
反应有气体生成,同时放出大量热。下列说法正确的是
 是重要的化工原料,可用于某些配合物的制备,如
是重要的化工原料,可用于某些配合物的制备,如 溶于氨水形成
溶于氨水形成 。液氨可以微弱的电离产生
。液氨可以微弱的电离产生 和
和 ,
, 中的一个H原子若被
中的一个H原子若被 取代可形成
取代可形成 (联氨),若被
(联氨),若被 取代可形成
取代可形成 (羟胺)。
(羟胺)。 经过转化可形成
经过转化可形成 、
、 、
、 、
、 (无色)
(无色) 等。
等。 与
与 反应有气体生成,同时放出大量热。下列说法正确的是
反应有气体生成,同时放出大量热。下列说法正确的是A.第一电离能: | B. 的键角比 的键角比 大 大 |
C. 难溶于水 难溶于水 | D. 中 中 键的数目为 键的数目为 |
您最近一年使用:0次
2023-05-05更新
|
315次组卷
|
3卷引用:新疆且末县第一中学2022-2023学年高二下学期6月期末考试化学试题
名校
8 . 已知NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4。下列说法正确的是
| A.中心离子的配位数为5 |
| B.配体为NO中,配位原子为O |
| C.该配合物中Fe的化合价为+2价,价层电子排布式为3d54s1,易被氧化为Fe3+ |
| D.H2O的VSEPR模型为四面体形,空间结构为V形 |
您最近一年使用:0次
名校
9 . 氮及其化合物在生产生活中具有广泛应用。氮气经过一系列的变化可以合成氨、氮的氧化物、硝酸等重要的化工原料;NO能被 溶液吸收生成配合物
溶液吸收生成配合物 ,减少环境污染。下列说法正确的是
,减少环境污染。下列说法正确的是
 溶液吸收生成配合物
溶液吸收生成配合物 ,减少环境污染。下列说法正确的是
,减少环境污染。下列说法正确的是| A.Fe2+提供孤电子对用于形成配位键 |
| B.该配合物中阴离子空间结构为三角锥形 |
C.配离子为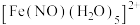 ,中心离子的配位数为6 ,中心离子的配位数为6 |
| D.该配合物中所含非金属元素均位于元素周期表的p区 |
您最近一年使用:0次
2023-02-06更新
|
756次组卷
|
11卷引用:新疆且末县第一中学2022-2023学年高二下学期6月期末考试化学试题
新疆且末县第一中学2022-2023学年高二下学期6月期末考试化学试题湖南省长沙市雅礼中学2022-2023学年高三下学期月考卷(六)化学试题 湖南省衡阳市第一中学2022-2023学年高三第七次月考化学试题湖南省株洲市第二中学2023届高三第七次月考化学试题广东省惠州市第一中学2022-2023学年高二下学期3月月考化学试题黑龙江省齐齐哈尔市第八中学校2022-2023学年高二下学期4月月考化学试题(已下线)回归教材重难点12 原子、分子和晶体结构再归纳-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)广东省珠海市金砖四校2022-2023学年高二下学期期中考试化学试题黑龙江省牡丹江市第二高级中学2023-2024学年高三上学期8月月考化学试题江苏省无锡市匡园双语学校2023-2024学年高二上学期期末考试化学试卷浙江省杭州市富阳区场口中学2023-2024学年高二下学期3月月考化学试题
解题方法
10 . 根据元素周期表中完整周期元素的性质,完成下列空格。
(1)在第三周期中,第一电离能最小的元素符号是_______ ,其原子的结构示意图为_______ ,第一电离能最大的元素符号是_______ ,其价电子排布式为_______ 。
(2)在元素周期表中,电负性最大的元素名称是_______ ,其价电子排布图为_______ 。
(3)第四周期元素中未成对电子数最多的元素符号是_______ ,其原子的简化电子排布式为_______ ,有_______ 个未成对电子。
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是_______ 。
(5)碳和氢形成的最简单碳正离子CH ,其中心原子碳原子的杂化类型为
,其中心原子碳原子的杂化类型为_______ ,该阳离子的空间构型为_______ 。
(6)向盛有CuSO4溶液的试管中滴加少量氨水,现象是_______ ,离子反应方程式为_______ ;继续滴加氨水至过量得到深蓝色溶液。经测定深蓝色是由于存在[Cu(NH3)4]SO4。其阳离子的结构式为_______ ,中心原子的配位数为_______ 。
(1)在第三周期中,第一电离能最小的元素符号是
(2)在元素周期表中,电负性最大的元素名称是
(3)第四周期元素中未成对电子数最多的元素符号是
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是
(5)碳和氢形成的最简单碳正离子CH
 ,其中心原子碳原子的杂化类型为
,其中心原子碳原子的杂化类型为(6)向盛有CuSO4溶液的试管中滴加少量氨水,现象是
您最近一年使用:0次



