1 . 下列关于超分子和配合物的叙述错误的是
A.配合物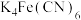 配离子的中心离子配位数是6 配离子的中心离子配位数是6 |
B.配合物 中存在离子键、共价键、配位键,若加入足量 中存在离子键、共价键、配位键,若加入足量 溶液,所有 溶液,所有 均被完全沉淀 均被完全沉淀 |
C.超分子“杯酚”具有分子识别的特性,利用此特性可分离 和 和 |
| D.人体细胞和细胞器的双分子膜体现了超分子的自组装特征 |
您最近一年使用:0次
2 . 为测定 中
中 配位数
配位数 ,将浓度均为
,将浓度均为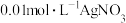 和
和 溶液按不同体积比混合,其用量和溶液浑浊度的关系如图,已知:
溶液按不同体积比混合,其用量和溶液浑浊度的关系如图,已知: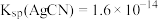 。
。
 中
中 配位数
配位数 ,将浓度均为
,将浓度均为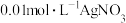 和
和 溶液按不同体积比混合,其用量和溶液浑浊度的关系如图,已知:
溶液按不同体积比混合,其用量和溶液浑浊度的关系如图,已知: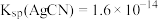 。
。
A.b点对应的 |
B. 中 中 配位数 配位数 |
C.当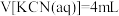 时, 时, |
D.当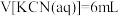 时, 时,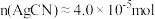 |
您最近一年使用:0次
3 . 向 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应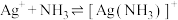 和
和 与
与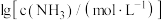 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表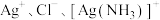 或
或 )。
)。
 饱和溶液(有足量
饱和溶液(有足量 固体)中滴加氨水,发生反应
固体)中滴加氨水,发生反应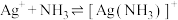 和
和 与
与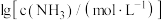 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表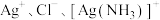 或
或 )。
)。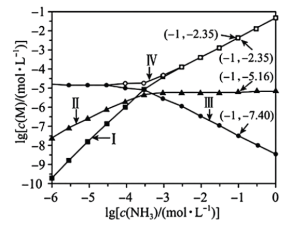
A.曲线Ⅰ表示 随 随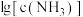 变化的曲线 变化的曲线 |
B. 的溶度积常数 的溶度积常数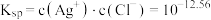 |
C.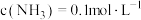 时,该饱和 时,该饱和 的溶解度为 的溶解度为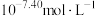 |
D.反应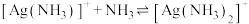 的平衡常数K的值为 的平衡常数K的值为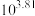 |
您最近一年使用:0次
解题方法
4 . 硫酸四氨合铜晶体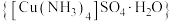 常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备
常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备 的流程如图。
的流程如图。 的空间结构为平面四边形。下列说法正确的是
的空间结构为平面四边形。下列说法正确的是
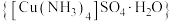 常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备
常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。实验室制备 的流程如图。
的流程如图。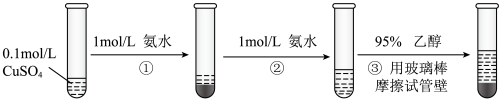
 的空间结构为平面四边形。下列说法正确的是
的空间结构为平面四边形。下列说法正确的是A. 晶体中存在的化学键有共价键、配位键、离子键和氢键 晶体中存在的化学键有共价键、配位键、离子键和氢键 |
| B.过程③加入95%乙醇的作用是增大溶剂极性,减小硫酸四氨合铜的溶解度 |
C.根据上述实验现象可知,与 结合能力由弱到强的顺序为 结合能力由弱到强的顺序为 |
D.若 中两个 中两个 被两个 被两个 取代,只有一种结构 取代,只有一种结构 |
您最近一年使用:0次
2024-05-14更新
|
184次组卷
|
3卷引用:湖北省十堰市2023-2024学年高三下学期4月调研考试化学试题
2024高三·全国·专题练习
5 . 在硫酸铜溶液中加入过量浓氨水,可形成[Cu(NH3)4(H2O)2]2+。下列有关说法错误的是
| A.配离子中两种配体的中心原子杂化方式和VSEPR模型均相同 |
| B.基态原子第一电离能:N>O>S |
| C.键角:BF3>H2O>NH3 |
| D.1mol[Cu(NH3)4(H2O)2]2+中含22molσ键 |
您最近一年使用:0次
2024·陕西安康·模拟预测
解题方法
6 . 向一定浓度硝酸银溶液中加入 溶液,产生
溶液,产生 沉淀,若加入过量
沉淀,若加入过量 溶液,沉淀会逐渐溶解,同时溶液中产生
溶液,沉淀会逐渐溶解,同时溶液中产生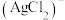 。溶液中含
。溶液中含 离子[
离子[ 和
和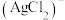 ]和
]和 的浓度关系如图所示[已知
的浓度关系如图所示[已知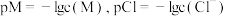 ],下列说法错误的是
],下列说法错误的是
 溶液,产生
溶液,产生 沉淀,若加入过量
沉淀,若加入过量 溶液,沉淀会逐渐溶解,同时溶液中产生
溶液,沉淀会逐渐溶解,同时溶液中产生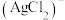 。溶液中含
。溶液中含 离子[
离子[ 和
和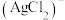 ]和
]和 的浓度关系如图所示[已知
的浓度关系如图所示[已知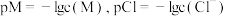 ],下列说法错误的是
],下列说法错误的是
A.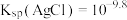 |
B.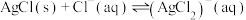 的 的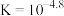 |
C.随着 溶液的加入, 溶液的加入,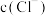 先升高后降低 先升高后降低 |
D. 点时溶液中存在: 点时溶液中存在: |
您最近一年使用:0次
7 . 向AgBr饱和溶液(有足量AgBr固体)中滴加Na2S2O3溶液,发生反应Ag++
 [Ag(
[Ag( )]-和[Ag(
)]-和[Ag( )]-+
)]-+
 [Ag(
[Ag( )2]3-, lg[c(M)/(mol/L)、lgc(N)与lg[c(
)2]3-, lg[c(M)/(mol/L)、lgc(N)与lg[c( )/mol/L)的关系如下图所示(其中M代表Ag+或Br-;N代表
)/mol/L)的关系如下图所示(其中M代表Ag+或Br-;N代表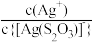 或
或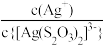 ):
):

 [Ag(
[Ag( )]-和[Ag(
)]-和[Ag( )]-+
)]-+
 [Ag(
[Ag( )2]3-, lg[c(M)/(mol/L)、lgc(N)与lg[c(
)2]3-, lg[c(M)/(mol/L)、lgc(N)与lg[c( )/mol/L)的关系如下图所示(其中M代表Ag+或Br-;N代表
)/mol/L)的关系如下图所示(其中M代表Ag+或Br-;N代表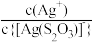 或
或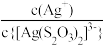 ):
):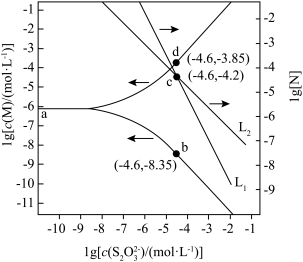
A.直线L1表示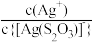 随 随 浓度变化的关系 浓度变化的关系 |
| B.AgBr的溶度积常数Ksp=c(Ag+)c(Br-)=10-12.2 |
C.反应AgBr+2  [Ag( [Ag( )2]3-+Br-的平衡常数K的值为101.2 )2]3-+Br-的平衡常数K的值为101.2 |
D.c( )= 0.001 mol/L时,溶液中c(Br-)>c{[Ag( )= 0.001 mol/L时,溶液中c(Br-)>c{[Ag( )2]3-}>c{[Ag(S2O3)]-} )2]3-}>c{[Ag(S2O3)]-} |
您最近一年使用:0次
2024-04-13更新
|
460次组卷
|
5卷引用:选择题11-15
(已下线)选择题11-15河北省石家庄市2024届高三下学期4月第二次质检化学试题2024届黑龙江省哈尔滨市第九中学高三下学期第四次模拟考试化学试卷河北省名校联盟2024届高三下学期4月第二次联考化学试题 (已下线)选择题11-14
8 . I.Ti、Na、Mg、C、N、O、Fe等元素单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)已知C、CO的燃烧热分别为393.5kJ/mol和283.0kJ/mol,写出碳不完全燃烧生成CO的热化学方程式___________ 。
(2)Na、Mg、C、N、O的第一电离能由大到小的顺序为___________ 。
(3)基态 原子最高能层的原子轨道形状为
原子最高能层的原子轨道形状为___________ ,其价电子轨道表示式为___________ 。
(4)钢铁发生吸氧腐蚀时正极的电极反应式为:___________ 。为防止钢铁输水管的腐蚀,可用导线将其与镁块连接,这种防护方法为___________ 。(电化学保护法中的一种)
(5)用琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是___________ 。
II.制备硫酸四氨合铜晶体
①取20mL配制好的硫酸铜溶液于试管中,向其中滴加1mol/L氨水,有蓝色沉淀生成。
②继续慢慢加入氨水并振荡试管,沉淀逐渐消失,生成深蓝色溶液。
(6) 中,形成配位键提供孤电子对的原子是
中,形成配位键提供孤电子对的原子是___________ (填元素符号),1mol该微粒中,含有σ键的数目为___________  (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(7)步骤②中蓝色沉淀溶解的离子方程式为___________ 。
(8)步骤③中加入无水乙醇的目的是___________ 。
(1)已知C、CO的燃烧热分别为393.5kJ/mol和283.0kJ/mol,写出碳不完全燃烧生成CO的热化学方程式
(2)Na、Mg、C、N、O的第一电离能由大到小的顺序为
(3)基态
 原子最高能层的原子轨道形状为
原子最高能层的原子轨道形状为(4)钢铁发生吸氧腐蚀时正极的电极反应式为:
(5)用琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是II.制备硫酸四氨合铜晶体
①取20mL配制好的硫酸铜溶液于试管中,向其中滴加1mol/L氨水,有蓝色沉淀生成。
②继续慢慢加入氨水并振荡试管,沉淀逐渐消失,生成深蓝色溶液。
③再向试管中加入15mL无水乙醇,混合后静置30分钟,有深蓝色晶体析出
(6)
 中,形成配位键提供孤电子对的原子是
中,形成配位键提供孤电子对的原子是 (设
(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(7)步骤②中蓝色沉淀溶解的离子方程式为
(8)步骤③中加入无水乙醇的目的是
您最近一年使用:0次
解题方法
9 . I.污水处理分析时,常用双硫腙(H2Dz,二元弱酸)把金属离子络合成电中性的物质,再用CCl4萃取络合物,从而把金属离子从水溶液中完全分离出来。如用双硫腙(H2Dz)~CCl4,分离污水中的Cu2+时,先发生络合反应:Cu2++2H2Dz Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
(1)污水显蓝色是因为四水合铜离子,其空间结构为___________ 。
(2)写出双硫腙和Fe3+络合的离子方程式:___________ 。萃取过程中要控制适宜的酸度。如果溶液的pH过大,其后果是___________ 。
Ⅱ.下图是用双硫腙(H2Dz)~CC14络合萃取某些金属离子的酸度曲线。它反映了萃取某些金属离子时适宜的pH范围。E%表示某种金属离子以络合物形式被萃取分离的百分率。
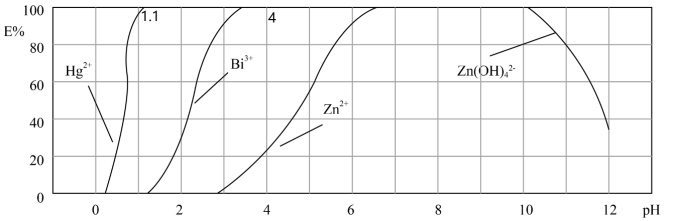
某工业废水中含有Hg2+、Bi3+、Zn2+,用双硫腙(H2Dz)~CC14络合萃取法处理废水。请根据上图回答问题:
(3)欲完全将废水中的Hg2+分离出来,须控制溶液pH为___________ 。
(4)当调节pH=2时,铋(Bi)的存在形式有:___________ ,其物质的量之比为___________ 。
(5)萃取到CCl4中的Zn(HDz)2分液后,加入足量的NaOH溶液,充分振荡后,锌又转到水溶液中。写出反应的离子方程式:___________ 。
 Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。(1)污水显蓝色是因为四水合铜离子,其空间结构为
(2)写出双硫腙和Fe3+络合的离子方程式:
Ⅱ.下图是用双硫腙(H2Dz)~CC14络合萃取某些金属离子的酸度曲线。它反映了萃取某些金属离子时适宜的pH范围。E%表示某种金属离子以络合物形式被萃取分离的百分率。

某工业废水中含有Hg2+、Bi3+、Zn2+,用双硫腙(H2Dz)~CC14络合萃取法处理废水。请根据上图回答问题:
(3)欲完全将废水中的Hg2+分离出来,须控制溶液pH为
(4)当调节pH=2时,铋(Bi)的存在形式有:
(5)萃取到CCl4中的Zn(HDz)2分液后,加入足量的NaOH溶液,充分振荡后,锌又转到水溶液中。写出反应的离子方程式:
您最近一年使用:0次
10 . 某兴趣小组探究镁跟碱性银氨溶液反应。实验步骤及现象如下。
Ⅰ.将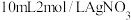 溶液和10mL6mol/L的氨水在锥形瓶中混合,测得pH=12。
溶液和10mL6mol/L的氨水在锥形瓶中混合,测得pH=12。
Ⅱ.加入1g去掉氧化层的镁条,十几秒后有许多气泡生成,用集气瓶排水集气,气体体积先增大后减小然后不变。同时锥形瓶中有灰白色沉淀生成。
Ⅲ.取出镁条过滤洗涤得到灰白色固体。
Ⅳ.取少量灰白色固体于试管中加入稀 ,沉淀全部溶解,并有无色的气体生成,且在试管口部气体变成红棕色,将其溶解后的溶液加入稀盐酸,产生大量白色沉淀。
,沉淀全部溶解,并有无色的气体生成,且在试管口部气体变成红棕色,将其溶解后的溶液加入稀盐酸,产生大量白色沉淀。
回答下列问题:
(1)步骤Ⅱ产生不溶于水的气体是________ ,易溶于水的气体是________ ,该气体使湿润的红色石蕊试纸变蓝色,生成该气体的反应的离子方程式为:________ 。
(2)步骤Ⅳ的现象证明灰白色固体一定含有________ 。证明灰白色固体中有 ,需要的试剂有稀盐酸和
,需要的试剂有稀盐酸和________ 。
(3)向水中加入1g去掉氧化层的镁条,几乎看不见气泡产生。镁跟碱性银氨溶液反应能迅速产生气泡的原因:________ 。
(4)向pH相同的氢氧化钠溶液中加入1g去掉氧化层的镁条,看不见气泡产生,其原因是:________ 。
Ⅰ.将
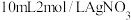 溶液和10mL6mol/L的氨水在锥形瓶中混合,测得pH=12。
溶液和10mL6mol/L的氨水在锥形瓶中混合,测得pH=12。Ⅱ.加入1g去掉氧化层的镁条,十几秒后有许多气泡生成,用集气瓶排水集气,气体体积先增大后减小然后不变。同时锥形瓶中有灰白色沉淀生成。
Ⅲ.取出镁条过滤洗涤得到灰白色固体。
Ⅳ.取少量灰白色固体于试管中加入稀
 ,沉淀全部溶解,并有无色的气体生成,且在试管口部气体变成红棕色,将其溶解后的溶液加入稀盐酸,产生大量白色沉淀。
,沉淀全部溶解,并有无色的气体生成,且在试管口部气体变成红棕色,将其溶解后的溶液加入稀盐酸,产生大量白色沉淀。回答下列问题:
(1)步骤Ⅱ产生不溶于水的气体是
(2)步骤Ⅳ的现象证明灰白色固体一定含有
 ,需要的试剂有稀盐酸和
,需要的试剂有稀盐酸和(3)向水中加入1g去掉氧化层的镁条,几乎看不见气泡产生。镁跟碱性银氨溶液反应能迅速产生气泡的原因:
(4)向pH相同的氢氧化钠溶液中加入1g去掉氧化层的镁条,看不见气泡产生,其原因是:
您最近一年使用:0次
2024-04-04更新
|
218次组卷
|
2卷引用:2024届湖北省十一校高三下学期第二次联考化学试卷



