1 . 某含铜催化剂的阴离于的结构如图所示。 是原子序数依次增大的短周期元素,乙是电负性最大的元素。下列说法错误的是
是原子序数依次增大的短周期元素,乙是电负性最大的元素。下列说法错误的是
 是原子序数依次增大的短周期元素,乙是电负性最大的元素。下列说法错误的是
是原子序数依次增大的短周期元素,乙是电负性最大的元素。下列说法错误的是
A.第一电离能: | B.该阴离于中铜元素的化合价为 |
| C.Z元素的单质可以与水发生置换反应 | D.仅由W和Y不可以构成离子化合物 |
您最近一年使用:0次
2 . 由下列实验事实得出的结论中错误的是
| 选项 | 实验目的 | 实验事实 | 结论 |
| A | 验证牺牲阳极的阴极保护法 | 将锌片与铁片用导线相连,插入酸化的3%NaCl溶液,一段时间后在铁电极区滴入2滴K3[Fe(CN)6]溶液,出现蓝色沉淀 | 铁不一定被腐蚀 |
| B | 麦芽糖水解产物的检验 | 麦芽糖与稀硫酸共热后,加NaOH溶液调至碱性再加入新制Cu(OH)2并加热,有砖红色沉淀生成 | 麦芽糖水解生成葡萄糖 |
| C | 探究Mg和水反应 | 取一小段镁条,用砂纸除去表面氧化膜,放入试管中,加入2mL水,并滴入2滴酚酞溶液,无明显现象;再加热试管至液体沸腾,溶液变红 | Mg可以与热水反应 |
| D | 制备一水合硫酸四氨合铜 | 向[Cu(NH3)4]SO4溶液中加入无水乙醇,并用玻璃棒摩擦试管壁,有深蓝色晶体析出 | 乙醇极性小,降低了[Cu(NH3)4]SO4的溶解度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 中国科学院化学所通过向 溶液引入ppm量级Cu离子,改善了光电阳极上氨催化反应的性能。其可能的反应历程如下图所示。下列说法错误的是
溶液引入ppm量级Cu离子,改善了光电阳极上氨催化反应的性能。其可能的反应历程如下图所示。下列说法错误的是
 溶液引入ppm量级Cu离子,改善了光电阳极上氨催化反应的性能。其可能的反应历程如下图所示。下列说法错误的是
溶液引入ppm量级Cu离子,改善了光电阳极上氨催化反应的性能。其可能的反应历程如下图所示。下列说法错误的是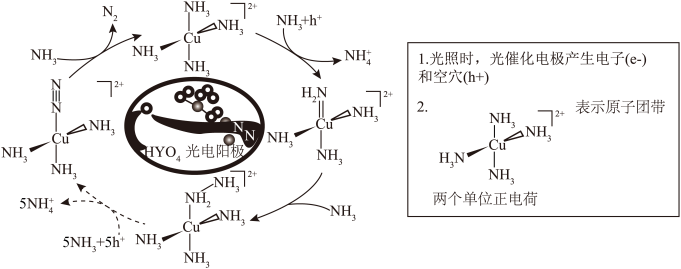
A.氨催化反应的光电阳极反应方程式为: |
B.配离子 比 比 更稳定 更稳定 |
C.反应历程中有 键、 键、 键的断裂和形成 键的断裂和形成 |
D. 中 中 的键角大于 的键角大于 中 中 的键角 的键角 |
您最近一年使用:0次
7日内更新
|
90次组卷
|
2卷引用:安徽省芜湖市2024届高三毕业班下学期5月教学质量统测化学试卷
4 . 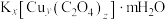 是一种重要的化工原料,其制备及各微粒的测定原理如下:
是一种重要的化工原料,其制备及各微粒的测定原理如下:
 .实验方法:称取
.实验方法:称取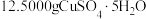 和
和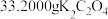 分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。
分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。
 .重量法测定配合物中结晶水含量
.重量法测定配合物中结晶水含量
将 配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。
配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。
 .配合物中
.配合物中 及
及 含量
含量
将 中的剩余固体先用1mol/L的
中的剩余固体先用1mol/L的 将其溶解配成250ml溶液,取25ml用酸性
将其溶解配成250ml溶液,取25ml用酸性 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,消耗
,消耗 0.0048mol;滴定后的溶液中铜以
0.0048mol;滴定后的溶液中铜以 形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量
形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量
回答下列问题:
(1)该配合物的配体及配位原子分别是___________ 、___________ 。
(2)本实验减压过滤所需的主要仪器有抽气泵、吸滤瓶及___________ 、___________ 。
(3)根据题干信息分析步骤 使用的洗涤剂为
使用的洗涤剂为___________ 。
(4)酸性滴定的离子反应方程式为___________ 。
(5)已知: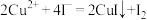 向滴定后的溶液加入足量的KI溶液,用0.6
向滴定后的溶液加入足量的KI溶液,用0.6
 溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为
溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为___________ ;若消耗 溶液的体积为10.00mL。
溶液的体积为10.00mL。 ,步骤
,步骤 中配合物铜的物质的量
中配合物铜的物质的量___________ mol。
(6)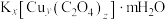 的化学式为:
的化学式为:___________ 。
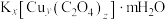 是一种重要的化工原料,其制备及各微粒的测定原理如下:
是一种重要的化工原料,其制备及各微粒的测定原理如下: .实验方法:称取
.实验方法:称取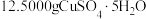 和
和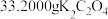 分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。
分别溶于水中,在85~90℃下混合浓缩,然后冷却到10℃,并将所得的沉淀减压过滤,迅速加以洗涤,烘干,晶体产率为60%。 .重量法测定配合物中结晶水含量
.重量法测定配合物中结晶水含量将
 配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。
配合物称重18.9000g于150℃下恒温2h,取出称量,反复几次,恒温称重,直到重量不再变化,称得重量为16.7400g。 .配合物中
.配合物中 及
及 含量
含量将
 中的剩余固体先用1mol/L的
中的剩余固体先用1mol/L的 将其溶解配成250ml溶液,取25ml用酸性
将其溶解配成250ml溶液,取25ml用酸性 标准溶液滴定溶液中的
标准溶液滴定溶液中的 ,消耗
,消耗 0.0048mol;滴定后的溶液中铜以
0.0048mol;滴定后的溶液中铜以 形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量
形式存在,通过控制溶液酸度,用间接碘法测定配合物中铜的含量回答下列问题:
(1)该配合物的配体及配位原子分别是
(2)本实验减压过滤所需的主要仪器有抽气泵、吸滤瓶及
(3)根据题干信息分析步骤
 使用的洗涤剂为
使用的洗涤剂为(4)酸性滴定的离子反应方程式为
(5)已知:
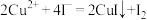 向滴定后的溶液加入足量的KI溶液,用0.6
向滴定后的溶液加入足量的KI溶液,用0.6
 溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为
溶液滴定,以淀粉溶液作指示剂,滴定终点的现象为 溶液的体积为10.00mL。
溶液的体积为10.00mL。 ,步骤
,步骤 中配合物铜的物质的量
中配合物铜的物质的量(6)
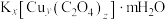 的化学式为:
的化学式为:
您最近一年使用:0次
解题方法
5 . 铁酸锌(ZnFe2O4)是一种性能优良的软磁材料,可溶于浓酸,不溶于碱。某实验小组模拟除杂后的盐酸酸洗废液(含Fe2+、Fe3+和少量Zn2+)制备铁酸锌的实验步骤如下:
1.取150mL除杂后的盐酸酸洗废液,加入4g还原铁粉,充分反应后过滤。
Ⅱ.在步骤I所得滤液中加入一定量NaClO3,加热搅拌充分反应。
Ⅲ.将稍过量ZnCl2固体加入步骤Ⅱ所得溶液,充分溶解。保持温度75℃,加入NaOH溶液调节pH=11,静置。
Ⅳ.冷却后过滤。将沉淀洗涤、干燥后煅烧,得到铁酸锌产品。
已知:ZnO、 均呈两性,
均呈两性, 可溶于pH>11的强碱中。
可溶于pH>11的强碱中。
回答下列问题:
(1)步骤I中加入还原铁粉除了将Fe3+转化为Fe2+外,目的还有_______ ,过滤时用到的玻璃仪器有烧杯、玻璃棒、_______ 。
(2)步骤Ⅱ中NaClO3的作用是_______ 。
(3)步骤Ⅳ中过滤所得沉淀主要成分是_______ ,写出煅烧生成ZnFe2O4的化学反应方程式_______ 。
(4)为得到较纯的纳米铁酸锌,还需将步骤Ⅳ所得产品用8mol/LNaOH溶液洗涤,主要为了洗去_______ 杂质。
(5)实验室也可用ZnCl2和FeCl3作反应物制备ZnFe2O4.该实验小组发现FeCl3溶液为黄色,经查阅Fe3+在水溶液中以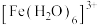 形式存在,
形式存在,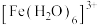 为淡紫色。他们做了如下假设:假设一:黄色与Fe3+水解有关;假设二:黄色与生成
为淡紫色。他们做了如下假设:假设一:黄色与Fe3+水解有关;假设二:黄色与生成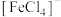 有关。为探究FeCl3溶液呈黄色的原因,他们设计了如下实验,发现①显黄色,②黄色变浅,由此证明假设一成立。Fe3+水解一般分步进行,写出其第一步水解的离子方程式
有关。为探究FeCl3溶液呈黄色的原因,他们设计了如下实验,发现①显黄色,②黄色变浅,由此证明假设一成立。Fe3+水解一般分步进行,写出其第一步水解的离子方程式_______ 。_______ 。
1.取150mL除杂后的盐酸酸洗废液,加入4g还原铁粉,充分反应后过滤。
Ⅱ.在步骤I所得滤液中加入一定量NaClO3,加热搅拌充分反应。
Ⅲ.将稍过量ZnCl2固体加入步骤Ⅱ所得溶液,充分溶解。保持温度75℃,加入NaOH溶液调节pH=11,静置。
Ⅳ.冷却后过滤。将沉淀洗涤、干燥后煅烧,得到铁酸锌产品。
已知:ZnO、
 均呈两性,
均呈两性, 可溶于pH>11的强碱中。
可溶于pH>11的强碱中。回答下列问题:
(1)步骤I中加入还原铁粉除了将Fe3+转化为Fe2+外,目的还有
(2)步骤Ⅱ中NaClO3的作用是
(3)步骤Ⅳ中过滤所得沉淀主要成分是
(4)为得到较纯的纳米铁酸锌,还需将步骤Ⅳ所得产品用8mol/LNaOH溶液洗涤,主要为了洗去
(5)实验室也可用ZnCl2和FeCl3作反应物制备ZnFe2O4.该实验小组发现FeCl3溶液为黄色,经查阅Fe3+在水溶液中以
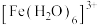 形式存在,
形式存在,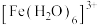 为淡紫色。他们做了如下假设:假设一:黄色与Fe3+水解有关;假设二:黄色与生成
为淡紫色。他们做了如下假设:假设一:黄色与Fe3+水解有关;假设二:黄色与生成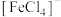 有关。为探究FeCl3溶液呈黄色的原因,他们设计了如下实验,发现①显黄色,②黄色变浅,由此证明假设一成立。Fe3+水解一般分步进行,写出其第一步水解的离子方程式
有关。为探究FeCl3溶液呈黄色的原因,他们设计了如下实验,发现①显黄色,②黄色变浅,由此证明假设一成立。Fe3+水解一般分步进行,写出其第一步水解的离子方程式
您最近一年使用:0次
6 . 铜的配合物在自然界中广泛存在,已知铜离子的配位数通常为4,请回答下列问题:
(1)基态29Cu的核外电子排布式为___________ 。
(2)硫酸铜溶液中存在多种微粒:
①硫酸铜溶液呈蓝色的原因是其中存在配离子___________ (填化学式),配体中提供孤电子对的原子是___________ (填元素符号)。
②SO 中心原子的杂化轨道类型为
中心原子的杂化轨道类型为___________ 。
(3)同学甲设计如图制备铜的配合物的实验:___________ 。
②由上述实验可得出以下结论:结论1:配合物的形成与___________ 、___________ 有关。
结论2:试管b、c中深蓝色配离子的稳定性强弱顺序为:___________ >___________ (填化学式)。
(1)基态29Cu的核外电子排布式为
(2)硫酸铜溶液中存在多种微粒:
①硫酸铜溶液呈蓝色的原因是其中存在配离子
②SO
 中心原子的杂化轨道类型为
中心原子的杂化轨道类型为(3)同学甲设计如图制备铜的配合物的实验:

②由上述实验可得出以下结论:结论1:配合物的形成与
结论2:试管b、c中深蓝色配离子的稳定性强弱顺序为:
您最近一年使用:0次
名校
7 .  是原子序数依次增大的前四周期元素,
是原子序数依次增大的前四周期元素, 的核外电子总数与其电子层数相同;
的核外电子总数与其电子层数相同; 和
和 同主族,
同主族, 的原子序数为
的原子序数为 原子价电子数的3倍;基态
原子价电子数的3倍;基态 原子
原子 轨道中成对电子与单电子的数目比为
轨道中成对电子与单电子的数目比为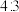 ,由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。回答下列问题:
,由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。回答下列问题:

(1) 中电子占据最高能级的电子云轮廓图为
中电子占据最高能级的电子云轮廓图为___________ 形,第三周期中第一电离能介于镁与磷元素之间的元素有___________ 种。
(2) 原子价电子层上的电子可以进行重排以便提供一个空轨道与
原子价电子层上的电子可以进行重排以便提供一个空轨道与 原子形成配位键,该原子重排后的价电子排布图为
原子形成配位键,该原子重排后的价电子排布图为___________ 。
(3) 、
、 形成的一种化合物以
形成的一种化合物以 的形式存在,其中
的形式存在,其中 的空间结构为
的空间结构为___________ ;下列对 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是___________ (填标号)。
a. b.
b. c.
c. d.
d.
(4) 和
和 为三角锥形,
为三角锥形, 不易与
不易与 形成配离子,解释原因
形成配离子,解释原因___________ 。
(5)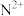 能形成配离子为八面体的配合物
能形成配离子为八面体的配合物 ,在该配合物中,
,在该配合物中,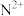 位于八面体的中心。若含
位于八面体的中心。若含 该配合物的溶液与足量
该配合物的溶液与足量 溶液反应可生成
溶液反应可生成 白色沉淀,则该配合物的化学式为
白色沉淀,则该配合物的化学式为___________ 。
(6)磷化硼晶体的晶胞如图所示。

上述晶胞沿体对角线方向的投影图为___________(填标号)。
 是原子序数依次增大的前四周期元素,
是原子序数依次增大的前四周期元素, 的核外电子总数与其电子层数相同;
的核外电子总数与其电子层数相同; 和
和 同主族,
同主族, 的原子序数为
的原子序数为 原子价电子数的3倍;基态
原子价电子数的3倍;基态 原子
原子 轨道中成对电子与单电子的数目比为
轨道中成对电子与单电子的数目比为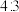 ,由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。回答下列问题:
,由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。回答下列问题:
(1)
 中电子占据最高能级的电子云轮廓图为
中电子占据最高能级的电子云轮廓图为(2)
 原子价电子层上的电子可以进行重排以便提供一个空轨道与
原子价电子层上的电子可以进行重排以便提供一个空轨道与 原子形成配位键,该原子重排后的价电子排布图为
原子形成配位键,该原子重排后的价电子排布图为(3)
 、
、 形成的一种化合物以
形成的一种化合物以 的形式存在,其中
的形式存在,其中 的空间结构为
的空间结构为 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是a.
 b.
b. c.
c. d.
d.
(4)
 和
和 为三角锥形,
为三角锥形, 不易与
不易与 形成配离子,解释原因
形成配离子,解释原因(5)
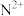 能形成配离子为八面体的配合物
能形成配离子为八面体的配合物 ,在该配合物中,
,在该配合物中,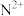 位于八面体的中心。若含
位于八面体的中心。若含 该配合物的溶液与足量
该配合物的溶液与足量 溶液反应可生成
溶液反应可生成 白色沉淀,则该配合物的化学式为
白色沉淀,则该配合物的化学式为(6)磷化硼晶体的晶胞如图所示。

上述晶胞沿体对角线方向的投影图为___________(填标号)。
A. | B. | C. | D. |
您最近一年使用:0次
名校
8 .  的配位化合物较稳定且用运广泛。
的配位化合物较稳定且用运广泛。 可与
可与 、
、 、
、 等配体形成溶液呈浅紫色的
等配体形成溶液呈浅紫色的 、红色的
、红色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验: 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的 的配离子,
的配离子, 不能与
不能与 形成配位离子。下列说法错误的是
形成配位离子。下列说法错误的是
 的配位化合物较稳定且用运广泛。
的配位化合物较稳定且用运广泛。 可与
可与 、
、 、
、 等配体形成溶液呈浅紫色的
等配体形成溶液呈浅紫色的 、红色的
、红色的 、无色的
、无色的 配离子。某同学按如下步骤完成实验:
配离子。某同学按如下步骤完成实验: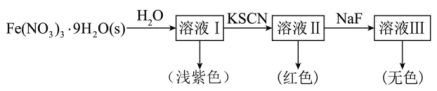
 的溶液中加入KSCN溶液生成蓝色的
的溶液中加入KSCN溶液生成蓝色的 的配离子,
的配离子, 不能与
不能与 形成配位离子。下列说法错误的是
形成配位离子。下列说法错误的是| A.Fe晶体中原子通过金属阳离子和自由电子间的静电作用相结合 |
B.可用NaF和KSCN溶液检验 溶液中是否含有 溶液中是否含有 |
C.溶液Ⅰ中 仅参与形成范德华力和氢键 仅参与形成范德华力和氢键 |
D.上述实验可得出,与 形成配合物的能力: 形成配合物的能力: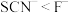 |
您最近一年使用:0次
2024-04-22更新
|
217次组卷
|
3卷引用:安徽省淮南第二中学2023-2024学年高二下学期期中测试化学试题
9 . 由下列实验方案、现象得出的结论不正确的是
实验方案 | 现象 | 结论 | |
| A | 向FeCl3溶液中加入几滴KSCN溶液 | 溶液立即变红 | KSCN溶液可用来检验Fe3+ |
| B | 用毛皮摩擦过的带电橡胶靠近CF2Cl2液流 | 液流方向改变 | CF2Cl2是正四面体结构,为非极性分子 |
| C | 在碘水中加入CCl4,振荡 | 分层,下层紫红色 | I2在水中的溶解度小于在CCl4中的溶解度 |
| D | [Cu(NH3)4]SO4溶液中加入乙醇 | 析出深蓝色固体 | [Cu(NH3)4]SO4在乙醇中溶解度小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-22更新
|
153次组卷
|
2卷引用:安徽省淮南第二中学2023-2024学年高二下学期期中测试化学试题
10 . 辉铜矿( ,含杂质
,含杂质 和
和 )合成
)合成 流程如图所示。下列说法中错误的是
流程如图所示。下列说法中错误的是
 ,含杂质
,含杂质 和
和 )合成
)合成 流程如图所示。下列说法中错误的是
流程如图所示。下列说法中错误的是
A.气体 的主要成分为 的主要成分为 | B.步骤Ⅱ中滤渣主要成分为 |
C.溶液 为深蓝色 为深蓝色 | D.步骤Ⅳ的操作为蒸发结晶 |
您最近一年使用:0次
2024-04-11更新
|
204次组卷
|
2卷引用:安徽省六安第一中学2024届高三下学期质量检测(二 )化学试题



