名校
解题方法
1 . 综合题
 .铁在自然界中有多种存在形式,并且对环境也有重要影响,某化学兴趣小组对土壤中的铁的存在和含量进行了以下的研究:
.铁在自然界中有多种存在形式,并且对环境也有重要影响,某化学兴趣小组对土壤中的铁的存在和含量进行了以下的研究:
(1)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),酸性环境中Fe2+脱除水体中硝态氮(NO )且无污染,写出该反应的离子方程式:
)且无污染,写出该反应的离子方程式:___________ 。
(2)土壤中的铁元素含量的测定:
乙二胺四乙酸又叫 ,是化学中一种良好的配合剂,形成的配合物又叫螯合物。
,是化学中一种良好的配合剂,形成的配合物又叫螯合物。 在配位滴定中用到,一般是测定金属离子的含量。已知:
在配位滴定中用到,一般是测定金属离子的含量。已知: 配离子结构如图,M为Fe3+。
配离子结构如图,M为Fe3+。 中氮原子杂化方式
中氮原子杂化方式___________ ,该配合物中Fe3+配位数是___________ 。
②土壤中的铁元素含量测定步骤:
第一步:取ag土壤试样溶解,加入足量H2O2,将溶液充分加热。
第二步:将上述液体配成100mL溶液,取25.00mL,,滴入两滴二甲酚橙作指示剂,用bmol·L-1EDTA(简写成H2Y2-)标准溶液滴定,反应的离子方程式为Fe3++H2Y2-=FeY-+2H+。达到滴定终点时,消耗EDTA标准溶液的平均体积为12.50mL。该土壤中的铁元素质量分数为___________ (用含a、b的代数式表示)。
③第一步加入足量H2O2的目的是:___________ 。
④若在滴定操作中一些不当操作可能会引起误差,下列操作会使土壤中的铁元素质量分数测定结果偏高的是:___________ 。
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点,读数时发现滴定管尖嘴处悬挂一滴溶液
D.盛放EDTA(简写成H2Y2-)标准溶液的滴定管用蒸馏水洗净后未用标准液润洗
 .铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。___________ 。
(4)若该晶胞的边长为d nm,则该合金的密度为___________  。(列出计算式即可,设阿伏加德罗常数的值为NA)
。(列出计算式即可,设阿伏加德罗常数的值为NA)
(5)若该晶体储氢时,H2分子在晶胞的体心和棱心位置,则含镁 48g的该储氢合金可储存标准状况下H2的体积约为___________ L。
 .铁在自然界中有多种存在形式,并且对环境也有重要影响,某化学兴趣小组对土壤中的铁的存在和含量进行了以下的研究:
.铁在自然界中有多种存在形式,并且对环境也有重要影响,某化学兴趣小组对土壤中的铁的存在和含量进行了以下的研究:(1)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),酸性环境中Fe2+脱除水体中硝态氮(NO
 )且无污染,写出该反应的离子方程式:
)且无污染,写出该反应的离子方程式:(2)土壤中的铁元素含量的测定:
乙二胺四乙酸又叫
 ,是化学中一种良好的配合剂,形成的配合物又叫螯合物。
,是化学中一种良好的配合剂,形成的配合物又叫螯合物。 在配位滴定中用到,一般是测定金属离子的含量。已知:
在配位滴定中用到,一般是测定金属离子的含量。已知: 配离子结构如图,M为Fe3+。
配离子结构如图,M为Fe3+。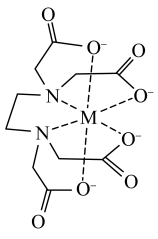
 中氮原子杂化方式
中氮原子杂化方式②土壤中的铁元素含量测定步骤:
第一步:取ag土壤试样溶解,加入足量H2O2,将溶液充分加热。
第二步:将上述液体配成100mL溶液,取25.00mL,,滴入两滴二甲酚橙作指示剂,用bmol·L-1EDTA(简写成H2Y2-)标准溶液滴定,反应的离子方程式为Fe3++H2Y2-=FeY-+2H+。达到滴定终点时,消耗EDTA标准溶液的平均体积为12.50mL。该土壤中的铁元素质量分数为
③第一步加入足量H2O2的目的是:
④若在滴定操作中一些不当操作可能会引起误差,下列操作会使土壤中的铁元素质量分数测定结果偏高的是:
A.滴定终点读数时,俯视滴定管的刻度
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定到终点,读数时发现滴定管尖嘴处悬挂一滴溶液
D.盛放EDTA(简写成H2Y2-)标准溶液的滴定管用蒸馏水洗净后未用标准液润洗
 .铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
.铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。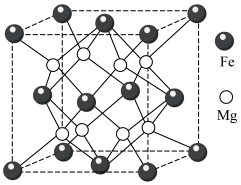
(4)若该晶胞的边长为d nm,则该合金的密度为
 。(列出计算式即可,设阿伏加德罗常数的值为NA)
。(列出计算式即可,设阿伏加德罗常数的值为NA)(5)若该晶体储氢时,H2分子在晶胞的体心和棱心位置,则含镁 48g的该储氢合金可储存标准状况下H2的体积约为
您最近一年使用:0次
名校
2 . 钴配合物 溶于热水,在冷水中微溶,可通过如下反应制备:
溶于热水,在冷水中微溶,可通过如下反应制备:

 。
。
具体步骤如下:
Ⅰ.称取 ,用
,用 水溶解。
水溶解。
Ⅱ.分批加入 后,将溶液温度降至
后,将溶液温度降至 以下,加入
以下,加入 活性炭、
活性炭、 浓氨水,搅拌下逐滴加入
浓氨水,搅拌下逐滴加入 的双氧水。
的双氧水。
Ⅲ.加热至 反应
反应 ,冷却,过滤。
,冷却,过滤。
Ⅳ.将滤得的固体转入含有少量盐酸的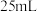 沸水中,趁热过滤。
沸水中,趁热过滤。
Ⅴ.滤液转入烧杯,加入 浓盐酸,冷却结晶、过滤、干燥,得到橙黄色晶体
浓盐酸,冷却结晶、过滤、干燥,得到橙黄色晶体  。回答下列问题:
。回答下列问题:
(1)步骤I中使用的部分仪器如下。 的名称是
的名称是________ 。该步骤中可采取的加快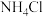 溶解的操作有
溶解的操作有_______ (填1种即可)。
(2)步骤Ⅱ中,将温度降至 以下为了避免
以下为了避免________ ;可选用______ 降低溶液温度。
(3)步骤Ⅳ中,趁热过滤的目的是_______ ,该步中除掉的不溶物主要为_________ 。
(4) 中,中心离子是
中,中心离子是________ ,外界是________ 。配体离子  的空间构型高度对称,呈
的空间构型高度对称,呈______ 形, 所含
所含 键数目为
键数目为_______ 。
 溶于热水,在冷水中微溶,可通过如下反应制备:
溶于热水,在冷水中微溶,可通过如下反应制备:

 。
。具体步骤如下:
Ⅰ.称取
 ,用
,用 水溶解。
水溶解。Ⅱ.分批加入
 后,将溶液温度降至
后,将溶液温度降至 以下,加入
以下,加入 活性炭、
活性炭、 浓氨水,搅拌下逐滴加入
浓氨水,搅拌下逐滴加入 的双氧水。
的双氧水。Ⅲ.加热至
 反应
反应 ,冷却,过滤。
,冷却,过滤。Ⅳ.将滤得的固体转入含有少量盐酸的
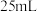 沸水中,趁热过滤。
沸水中,趁热过滤。Ⅴ.滤液转入烧杯,加入
 浓盐酸,冷却结晶、过滤、干燥,得到橙黄色晶体
浓盐酸,冷却结晶、过滤、干燥,得到橙黄色晶体  。回答下列问题:
。回答下列问题:(1)步骤I中使用的部分仪器如下。
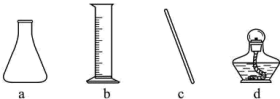
 的名称是
的名称是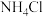 溶解的操作有
溶解的操作有(2)步骤Ⅱ中,将温度降至
 以下为了避免
以下为了避免(3)步骤Ⅳ中,趁热过滤的目的是
(4)
 中,中心离子是
中,中心离子是 的空间构型高度对称,呈
的空间构型高度对称,呈 所含
所含 键数目为
键数目为
您最近一年使用:0次
3 .  是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:
是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:
(1)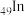 的价层电子排布式为
的价层电子排布式为_______ 。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋量子数,对于基态S原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋量子数,对于基态S原子,其价电子自旋磁量子数的代数和为_______ 。S可以形成两种常见含氧酸,其通式为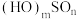 ,解释
,解释 酸性更强的原因
酸性更强的原因_______ 。
(3)矾土含 ,《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的
,《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。_______ 。
②X中C的杂化轨道类型是_______ ,X中不存在的作用力有_______ (填标号)。
A.配位键 B.离子键 C.共价键 D.氢键 F.范德华力
③茜素水溶性较好的原因是_______ 。
(4) (相对分子质量为Mr)的晶胞结构如图a所示,阿伏加德罗常数为
(相对分子质量为Mr)的晶胞结构如图a所示,阿伏加德罗常数为 ,则
,则 晶体的密度为
晶体的密度为_______  (列计算式),图b为Cu原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置
(列计算式),图b为Cu原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置_______ (用“ ”表示S原子)。
”表示S原子)。
 是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:
是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:(1)
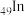 的价层电子排布式为
的价层电子排布式为(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋量子数,对于基态S原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋量子数,对于基态S原子,其价电子自旋磁量子数的代数和为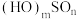 ,解释
,解释 酸性更强的原因
酸性更强的原因(3)矾土含
 ,《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的
,《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。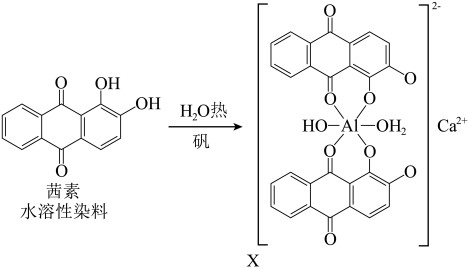
②X中C的杂化轨道类型是
A.配位键 B.离子键 C.共价键 D.氢键 F.范德华力
③茜素水溶性较好的原因是
(4)
 (相对分子质量为Mr)的晶胞结构如图a所示,阿伏加德罗常数为
(相对分子质量为Mr)的晶胞结构如图a所示,阿伏加德罗常数为 ,则
,则 晶体的密度为
晶体的密度为 (列计算式),图b为Cu原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置
(列计算式),图b为Cu原子沿z轴方向向x-y平面投影的位置,在图b中画出S原子在该方向的投影位置 ”表示S原子)。
”表示S原子)。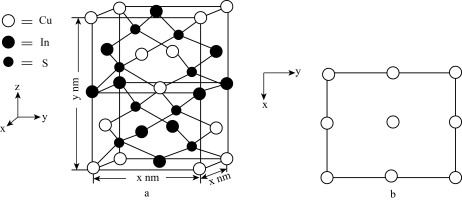
您最近一年使用:0次
名校
解题方法
4 . 秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。通过对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy) 。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供_______ ,配位原子是_______ ,1 mol [Cu(H2O)4]2+中σ键的数目为_________ 。
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式_______________ ,再向溶液中加入乙醇,会析出深蓝色晶体____________ (写出化学式)。
(3)“中国蓝”“中国紫”中存在 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为_______ 。
(4)BaO的熔沸点_____ MgO(填“>”“<”“=”),原因是______________ 。
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为_______ 。NA代表阿伏加德罗常数的值,晶胞参数为a pm,则其晶体密度为___________ g·cm-3。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式
(3)“中国蓝”“中国紫”中存在
 四面体结构,其中Si原子采取的杂化方式为
四面体结构,其中Si原子采取的杂化方式为(4)BaO的熔沸点
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为

您最近一年使用:0次
5 . 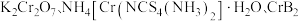 均是铬的重要化合物,回答下列问题:
均是铬的重要化合物,回答下列问题: 原子有
原子有___________ 种能量不同的电子,价电子排布式为___________ 。
(2)已知电子亲和能(E)是基态的气态原子得到电子变为气态阴离子所放出的能量, 。氧的第一电子亲和能
。氧的第一电子亲和能 为
为___________  ;
; ,其原因是
,其原因是___________ 。
(3)雷氏盐的化学式为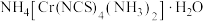 。
。
①H、C、N、O四种元素的电负性由大到小的顺序为___________ 。
②雷氏盐中所含化学键类型___________ 。
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
③配体之一 分子的
分子的 模型名称为
模型名称为___________ ,与配体 互为等电子体的分子和离子有
互为等电子体的分子和离子有___________ 、___________ (各写1种)。
(4)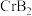 的晶体密度为
的晶体密度为 ,晶体结构(如图)为六棱柱,底边边长为
,晶体结构(如图)为六棱柱,底边边长为 ,高为
,高为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则
,则
___________ (列出计算式)。
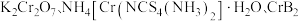 均是铬的重要化合物,回答下列问题:
均是铬的重要化合物,回答下列问题: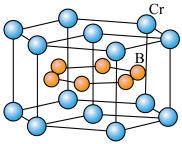
 原子有
原子有(2)已知电子亲和能(E)是基态的气态原子得到电子变为气态阴离子所放出的能量,
 。氧的第一电子亲和能
。氧的第一电子亲和能 为
为 ;
; ,其原因是
,其原因是(3)雷氏盐的化学式为
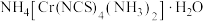 。
。①H、C、N、O四种元素的电负性由大到小的顺序为
②雷氏盐中所含化学键类型
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
③配体之一
 分子的
分子的 模型名称为
模型名称为 互为等电子体的分子和离子有
互为等电子体的分子和离子有(4)
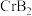 的晶体密度为
的晶体密度为 ,晶体结构(如图)为六棱柱,底边边长为
,晶体结构(如图)为六棱柱,底边边长为 ,高为
,高为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则
,则
您最近一年使用:0次
名校
解题方法
6 . 铜离子可与含N、含O的微粒形成多种结构。向CuSO4溶液中滴加氨水可最终形成如图所示的配离子。___________ 。关于该微粒说法正确的是___________ 。
A.1mol该微粒中有22mol共价键
B.该微粒中的N、O原子构成了立方体结构
C.电负性N>O>H
D.该微粒中可与溶剂水分子形成氢键的只有N、O原子
(2)铜元素位于元素周期表的___________ 区。铜原子价电子排布式 为___________ 。
A.s区 B.p区 C.ds区 D.f区
(3)Cu2+无法与BF3中的B原子形成配位键的原因是___________ 。
(4)Cu2+可形成如图所示晶体。该晶胞中负离子为 CN—,“连接”着每一对相邻的Fe3+与Cu2+(部分 示例位置已用箭头标出)。___________ 个。
②已知相邻的Fe3+与Cu2+核间距为apm,则相邻的Fe3+与K+核间距为___________ pm。
③该晶体的化学式为___________ 。

A.1mol该微粒中有22mol共价键
B.该微粒中的N、O原子构成了立方体结构
C.电负性N>O>H
D.该微粒中可与溶剂水分子形成氢键的只有N、O原子
(2)铜元素位于元素周期表的
A.s区 B.p区 C.ds区 D.f区
(3)Cu2+无法与BF3中的B原子形成配位键的原因是
(4)Cu2+可形成如图所示晶体。该晶胞中

②已知相邻的Fe3+与Cu2+核间距为apm,则相邻的Fe3+与K+核间距为
③该晶体的化学式为
您最近一年使用:0次
7 . 回答下列问题:
(1) 中含有的含氧官能团名称是
中含有的含氧官能团名称是___________ 。碳原子的杂化方式有___________ ;分子式是___________ ;有___________ 个手性碳原子。
(2)已知熔融的BeCl2不导电,则BeCl2属于___________ 晶体,中心原子的杂化类型为___________ 。
(3)氨水是一种速效氮肥:
①氨水中存在___________ 种氢键,氨极易溶于水的原因是___________ ;
②氨水中含有配位键的粒子有H3O+和X,则X离子中形成的配位键中提供孤电子对的原子是___________ ,X离子能否作为其他配合物的配位体___________ (填“能”或“否”)。
(1)
 中含有的含氧官能团名称是
中含有的含氧官能团名称是(2)已知熔融的BeCl2不导电,则BeCl2属于
(3)氨水是一种速效氮肥:
①氨水中存在
②氨水中含有配位键的粒子有H3O+和X,则X离子中形成的配位键中提供孤电子对的原子是
您最近一年使用:0次
名校
8 . 某种新型储氢材料(摩尔质量为188g∙mol–1)的立方晶胞如图,该晶胞可储存6个氢原子。已知M核内中子数比质子数多4,标准状况下氢气的密度为ρg∙cm–3,NA表示阿伏加德罗常数的值。下列说法正确的是

| A.晶胞中[M(NH3)6]n+和[BH4]–的配位数相同 |
| B.M离子最外层电子排布式为3d64s2 |
C.在晶胞体对角线的一维空间上会出现 的排布规律 的排布规律 |
D.该材料的储氢能力[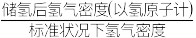 ]为 ]为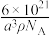 |
您最近一年使用:0次
解题方法
9 . X、Y、Z、R、W为原子序数依次增大的前20号主族元素,X元素原子失去一个电子后是“裸露”质子;R原子最外层电子数是其内层电子总数的一半;X、Y、Z、R形成的化合物表示为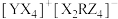 ;W是前20号元素中金属性最强的,下列正确的是
;W是前20号元素中金属性最强的,下列正确的是
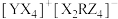 ;W是前20号元素中金属性最强的,下列正确的是
;W是前20号元素中金属性最强的,下列正确的是
A.离子半径: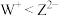 |
| B.元素X、Y、Z形成的化合物可能属于离子化合物 |
C.简单氢化物的沸点: |
D.如上图所示,该物质中,冠醚和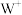 之间的配位键是离子键 之间的配位键是离子键 |
您最近一年使用:0次
10 . 磷酸亚铁锂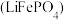 和锰酸锂
和锰酸锂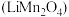 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:
(1)基态O原子的价电子轨道表示式为___________ ;Mn的原子结构示意图为___________ 。
(2) 的熔、沸点
的熔、沸点___________ (填“高于”或“低于”) 。
。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性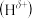 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性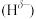 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是___________ 。
(4)已知: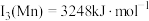 ,
,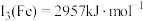 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是___________ 。
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过螯合作用 形成的配位键有___________ mol。
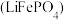 和锰酸锂
和锰酸锂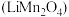 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:(1)基态O原子的价电子轨道表示式为
(2)
 的熔、沸点
的熔、沸点 。
。(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性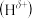 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性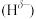 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是(4)已知:
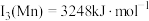 ,
,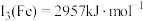 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过
您最近一年使用:0次



