名校
1 . 布洛芬具有抗炎、镇痛、解热的作用,但口服该药对肠道、胃有刺激性,解决方法之一是对该分子进行成酯修饰(如图所示)。下列说法正确的是


| A.电负性:N>C>O | B.R和T中均无手性碳原子 |
C.沸点: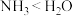 | D.R和T均不能与氧气发生氧化反应 |
您最近一年使用:0次
名校
2 . 下列说法中正确的是
A.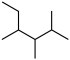 的名称为3,4-二甲基-2-乙基戊烷 的名称为3,4-二甲基-2-乙基戊烷 |
B. 、 、 的空间结构均为平面三角形 的空间结构均为平面三角形 |
| C.HF比HCl沸点高的原因是HF分子内存在氢键 |
D.键角: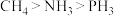 |
您最近一年使用:0次
名校
3 . 8-羟基喹啉衍生物镍(Ⅱ)配合物(N)是一类具有潜在金属基抗癌活性的药物,某团队采用如图所示方法合成:

| A.基态Ni原子核外未成对电子数为2 |
| B.1molM配体与Ni(Ⅱ)形成的配位键有3mol |
| C.有机物N中所有碳原子均采用sp2杂化 |
| D.甲醇的沸点高于二氯甲烷,其原因是甲醇间存在氢键 |
您最近一年使用:0次
2023-07-06更新
|
105次组卷
|
3卷引用:河南省洛阳市创新发展联盟2023-2024学年高三上学期7月阶段性考试化学试题
解题方法
4 . BP晶体超硬、耐磨,是耐高温飞行器的红外增透的理想材料,其合成途径之一为 。BP的晶胞结构如图所示(已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标)。
。BP的晶胞结构如图所示(已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标)。
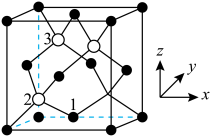
下列说法正确的是
 。BP的晶胞结构如图所示(已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标)。
。BP的晶胞结构如图所示(已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标)。
下列说法正确的是
| A.BBr3、HBr都是极性分子 |
| B.BBr3与PBr3中心原子的价层电子对数相同 |
| C.HF比HBr稳定且沸点高,都与HF分子间能形成氢键有关 |
D.若原子1的分数坐标为( , , ,0),则原子3的分数坐标为( ,0),则原子3的分数坐标为( , , , , ) ) |
您最近一年使用:0次
5 . 下列有关物质结构与性质的说法中错误的是
A.根据VSEPR理论可知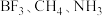 分子内键角依次减小 分子内键角依次减小 |
B. 的电负性比 的电负性比 的大,可推断 的大,可推断 的酸性强于 的酸性强于 |
C.第四周期元素中, 的第一电离能低于 的第一电离能低于 |
D.因为水分子间存在氢键,故 的稳定性大于 的稳定性大于 |
您最近一年使用:0次
2023-07-05更新
|
308次组卷
|
2卷引用:河南省周口市项城市2022-2023学年高二下学期7月期末考试化学试题
解题方法
6 . 按要求回答下列问题:
(1)9.0g某有机化合物完全燃烧可产生0.3molCO2和0.3molH2O。该物质的蒸气对氢气的相对密度是45,则该有机化合物的分子式为_________ 。若该物质为链状结构,其核磁共振氢谱有4组峰,峰面积之比为1∶2∶2∶1,且自身能够发生缩聚反应生成聚酯,其结构简式为_________ 。
(2)氨气极易溶于水的原因是_________ 。
(3)CH3COOH的酸性小于CCl3COOH的原因是_________ 。
(4)三价铬离子能形成多种配位化合物。在 中,提供电子对形成配位键的原子除了N、Cl外,还有
中,提供电子对形成配位键的原子除了N、Cl外,还有_________ (填元素符号), 中含有
中含有_________ molσ键。
(1)9.0g某有机化合物完全燃烧可产生0.3molCO2和0.3molH2O。该物质的蒸气对氢气的相对密度是45,则该有机化合物的分子式为
(2)氨气极易溶于水的原因是
(3)CH3COOH的酸性小于CCl3COOH的原因是
(4)三价铬离子能形成多种配位化合物。在
 中,提供电子对形成配位键的原子除了N、Cl外,还有
中,提供电子对形成配位键的原子除了N、Cl外,还有 中含有
中含有
您最近一年使用:0次
2023-07-02更新
|
77次组卷
|
2卷引用:河南省许昌市2022-2023学年高二下学期7月期末化学试题
7 . 第四次工业革命(工业4.0)开启了智能化时代,高质量的单晶硅是“芯片”的基础,“芯片”是智能的心脏。
(1)下列对于基态硅原子的叙述正确的是___________ (填标号)。
a.原子轨道电子排布半充满时体系能量最低,电子排布式为
b. 轨道的电子总是比
轨道的电子总是比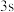 轨道的电子在离核更远的区域运动
轨道的电子在离核更远的区域运动
c.电负性比 高,原子对键合电子的吸引力比
高,原子对键合电子的吸引力比 大
大
(2)近年来美国为了遏制中国发展,对我国发起了以封锁“芯片”为核心的全方位打压,此举激发了中国科技人员自研的决心。2022年10月宁波南大光电 光刻胶生产线正式投产,国内
光刻胶生产线正式投产,国内 芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:
芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:

①该聚碳酸酯中碳原子的杂化方式为___________ ;
②聚碳酸酯膜曝光后的产物加热可汽化或溶于水,加热汽化或溶于水克服的作用力有___________ 。
(3)有机高分子聚合物中掺杂氧化锆等可导电的固体电解质可以提高光刻胶的性能。
①锆是第5周期ⅣB元素,则基态锆原子的价电子排布式为___________ ;
②氟化钙 (CaF2)和氧化锆(ZrO2)的晶体结构如下图,氧化锆的熔点(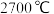 )高于氟化钙(
)高于氟化钙( ),原因是
),原因是___________ 。

(1)下列对于基态硅原子的叙述正确的是
a.原子轨道电子排布半充满时体系能量最低,电子排布式为

b.
 轨道的电子总是比
轨道的电子总是比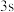 轨道的电子在离核更远的区域运动
轨道的电子在离核更远的区域运动c.电负性比
 高,原子对键合电子的吸引力比
高,原子对键合电子的吸引力比 大
大(2)近年来美国为了遏制中国发展,对我国发起了以封锁“芯片”为核心的全方位打压,此举激发了中国科技人员自研的决心。2022年10月宁波南大光电
 光刻胶生产线正式投产,国内
光刻胶生产线正式投产,国内 芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:
芯片制造材料获得重大突破。一种聚碳酸酯胶的曝光分解原理如下:
①该聚碳酸酯中碳原子的杂化方式为
②聚碳酸酯膜曝光后的产物加热可汽化或溶于水,加热汽化或溶于水克服的作用力有
(3)有机高分子聚合物中掺杂氧化锆等可导电的固体电解质可以提高光刻胶的性能。
①锆是第5周期ⅣB元素,则基态锆原子的价电子排布式为
②氟化钙 (CaF2)和氧化锆(ZrO2)的晶体结构如下图,氧化锆的熔点(
 )高于氟化钙(
)高于氟化钙( ),原因是
),原因是
您最近一年使用:0次
名校
解题方法
8 . 铜及其化合物在工农业生产中有广泛的应用。
(1)向CuSO4溶液中加入过量NaOH溶液可生成Na2[Cu(OH)4]。Na2[Cu(OH)4]中除了配位键外,还存在的化学键类型有___________(填字母)。
(2)将CuO投入NH3、(NH4)2SO4的混合溶液中进行“氨浸”,控制温度为50℃至55℃,pH约为9.5,CuO转化为溶液。
①CuO被浸取的离子方程式为___________ 。
②[Cu(NH3)4]2+结构中,若用两个H2O分子代替两个NH3分子,可以得到两种不同结构的化合物,由此推测的[Cu(NH3)4]2+空间构型为___________ 。
(3)Cu2+可以与乙二胺(H2N-CH2-CH2-NH2) 形成配离子,结构如图所示:
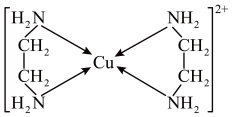
乙二胺分子中N原子成键时采取的VSEPR模型是___________ 。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高很多,原因是___________ 。
(1)向CuSO4溶液中加入过量NaOH溶液可生成Na2[Cu(OH)4]。Na2[Cu(OH)4]中除了配位键外,还存在的化学键类型有___________(填字母)。
| A.离子键 | B.金属键 | C.极性共价键 | D.非极性共价键 |
①CuO被浸取的离子方程式为
②[Cu(NH3)4]2+结构中,若用两个H2O分子代替两个NH3分子,可以得到两种不同结构的化合物,由此推测的[Cu(NH3)4]2+空间构型为
(3)Cu2+可以与乙二胺(H2N-CH2-CH2-NH2) 形成配离子,结构如图所示:

乙二胺分子中N原子成键时采取的VSEPR模型是
您最近一年使用:0次
名校
9 . 已知X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y与X形成的分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)Z元素的元素名称:___________ 。
(2)Y的简单气态氢化物的熔沸点高于PH3的原因为___________ 。
(3)Y、Z、W的简单离子半径由大到小排序为(用元素符号表示):___________ 。
(4)Y、Z气态氢化物的稳定性由大到小排序为(用化学式表示):___________ 。
(5)用电子书写由以上元素中两两形成的化合物中含有离子键和非极性共价键的化合物的形成过程:___________ 。
(6)X、W组成的化合物与水反应的化学反应方程式为:___________ 。
(7)由X、Y、Z所形成的常见离子化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为:___________ 。
(1)Z元素的元素名称:
(2)Y的简单气态氢化物的熔沸点高于PH3的原因为
(3)Y、Z、W的简单离子半径由大到小排序为(用元素符号表示):
(4)Y、Z气态氢化物的稳定性由大到小排序为(用化学式表示):
(5)用电子书写由以上元素中两两形成的化合物中含有离子键和非极性共价键的化合物的形成过程:
(6)X、W组成的化合物与水反应的化学反应方程式为:
(7)由X、Y、Z所形成的常见离子化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为:
您最近一年使用:0次
名校
解题方法
10 . 一水硫酸四氨合铜 是一种易溶于水的晶体,可作高效安全的广谱杀菌剂,实验室制备流程如图:
是一种易溶于水的晶体,可作高效安全的广谱杀菌剂,实验室制备流程如图:
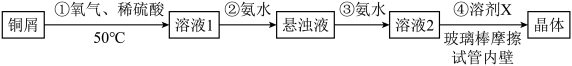
下列说法错误的是
 是一种易溶于水的晶体,可作高效安全的广谱杀菌剂,实验室制备流程如图:
是一种易溶于水的晶体,可作高效安全的广谱杀菌剂,实验室制备流程如图:
下列说法错误的是
| A.铜屑表面的油污可通过“碱煮水洗”去除,利用油污在碱性环境中水解的原理 |
B.过程③中蓝色沉淀溶解,溶液变为深蓝色,生成了配合物,该过程可证明 与 与 配位能力比 配位能力比 与 与 配位能力强 配位能力强 |
| C.过程④中加入的“溶剂X”可以是乙醇,改变了溶液的极性使溶质溶解度减小而析出 |
D.玻璃棒摩擦目的是加快结晶速率,形成的晶体 中含有离子键、共价键、配位键、氢键 中含有离子键、共价键、配位键、氢键 |
您最近一年使用:0次



