名校
解题方法
1 . 下列关于各物质用途的解释不正确 的是
| 选项 | 用途 | 解释 |
| A |  用作制冷剂 用作制冷剂 |  极易溶于水 极易溶于水 |
| B | 氧化铝用作耐火材料 | 氧化铝熔点高 |
| C | 铁粉用作食品的抗氧化剂 | 铁粉具有还原性 |
| D |  用作供氧剂 用作供氧剂 |  与水及 与水及 等反应产生 等反应产生 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-06更新
|
756次组卷
|
5卷引用:2023年高考浙江卷化学真题(6月)变式题(选择题1-5)
名校
解题方法
2 . 现有处于不同主族的短周期元素A、B、C、D、E,其中B原子最外层电子数是电子层数的2倍,C是金属元素, 的D的最高价氧化物的水化物溶液pH<1,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
的D的最高价氧化物的水化物溶液pH<1,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是

 的D的最高价氧化物的水化物溶液pH<1,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
的D的最高价氧化物的水化物溶液pH<1,五种元素的原子半径与原子序数的关系如图所示。下列推断正确的是
| A.除A外,均属于P区元素 |
| B.B、D、E形成的简单氢化物均为极性分子 |
| C.B分别与D、E形成的分子中,后者键角更大 |
| D.五种元素形成的单质中,熔点最高的是B的单质 |
您最近一年使用:0次
解题方法
3 . 下列实验操作对应的实验现象错误的是
| 选项 | 实验操作 | 实验现象 |
| A | 向KI溶液中滴加淀粉溶液 | 溶液变蓝 |
| B | 向 溶液中滴加NaOH溶液 溶液中滴加NaOH溶液 | 白色沉淀→灰绿色沉淀→红褐色沉淀 |
| C | 向饱和 溶液中加入少量纯碱粉末 溶液中加入少量纯碱粉末 | 生成白色沉淀 |
| D | 向酸性 溶液中加入过量甲苯,振荡 溶液中加入过量甲苯,振荡 |  溶液的紫红色消失 溶液的紫红色消失 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-01-14更新
|
221次组卷
|
3卷引用:海南省2022-2023学年高三上学期期末学业水平诊断化学试题
解题方法
4 . 下列表示不正确 的是
A. 的分子结构模型: 的分子结构模型: | B.乙烯的结构简式: |
C.氯原子的结构示意图: | D. 的电子式: 的电子式: |
您最近一年使用:0次
2023-01-09更新
|
397次组卷
|
3卷引用:北京市顺义区2023届高三第一次统练化学试题
5 . 下列装置或操作能达到相应实验目的的是
| 选项 | A | B | C | D |
| 装置或操作 |  |  |  | 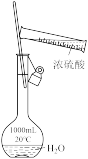 |
| 实验目的 | 排水集气法收集 | 实验室制取氨气 | 测定镁铝合金中铝排水的质量分数 | 配制稀硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 向两份20 ml 0.1 mol/LBa(OH)2溶液中各加入定量的KAl(SO4)2和Al2(SO4)3溶液的导电性随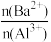 (混合前)的变化关系如图所示,下列分析不正确的是
(混合前)的变化关系如图所示,下列分析不正确的是
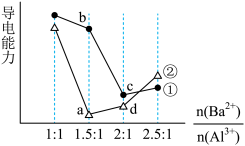
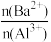 (混合前)的变化关系如图所示,下列分析不正确的是
(混合前)的变化关系如图所示,下列分析不正确的是
| A.a点溶液的pH值约为7 | B.b点溶液中大量存在的阳离子有Al3+和Ba2+ |
| C.c、d两点溶液中OH-均已完全反应 | D.②代表加入Al2(SO4)3的变化曲线 |
您最近一年使用:0次
2023-01-05更新
|
967次组卷
|
3卷引用:安徽省皖南八校2022-2023学年高三上学期第一次大联考化学试题
名校
解题方法
7 . 连二亚硫酸钠(Na2S2O4)是重要的化工产品,可用SO2与Zn、NaOH溶液反应制取。实验室模拟制备的工艺流程及制取装置如图。


已知:①连二亚硫酸钠易溶于水、难溶于乙醇、在碱性介质中较稳定、在空气中易被氧化。
②二价锌在水溶液中的存在形式与pH的关系如图。

请回答下列问题:
(1)通入一段时间SO2的作用除了充当反应物以外还有______ 。需调节溶液为弱碱性的原因______ 。
(2)写出制取连二亚硫酸钠的总化学方程式______ 。
(3)下列说法正确的是______ 。
(4)请选择最佳操作并排序完成制备Na2S2O4•2H2O晶体。安装好整套装置,并检查装置的气密性→______→______→______→过滤取滤液并加入NaCl固体,冷却至室温、过滤,洗涤,干燥得晶体。______
a.将一定量的Zn粉与蒸馏水混合搅拌成悬浊液
b.将一定量的Zn粉与NaOH溶液混合搅拌成悬浊液
c.将一定量的Zn粉与HCl混合搅拌成悬浊液
d.向悬浊液中通入SO2至澄清,并加热
e.28~35℃加热条件下,向悬浊液中通入SO2至澄清
f.28~35℃加热条件下,向悬浊液中加入Na2SO3溶液
g.向溶液中滴加NaOH至pH在8.2~10.5之间
h.向溶液中滴加HCl至pH在8.2以下
i.向溶液中滴加1mol•L-1NaOH至pH在10.5以上
(5)称取上述制得的连二亚硫酸钠样品0.0870g加入另一三颈烧瓶,通过自动电位滴定仪控制滴定管向三颈烧瓶中快速滴加K3[Fe(CN)6]溶液将连二亚硫酸钠氧化为硫酸钠,记录终点读数,共消耗10.00mL0.2000mol•L-1的K3[Fe(CN)6]溶液,则样品中连二亚硫酸钠的纯度为______ 。(结果保留1位小数),样品中可能存在的杂质有______ 。


已知:①连二亚硫酸钠易溶于水、难溶于乙醇、在碱性介质中较稳定、在空气中易被氧化。
②二价锌在水溶液中的存在形式与pH的关系如图。

请回答下列问题:
(1)通入一段时间SO2的作用除了充当反应物以外还有
(2)写出制取连二亚硫酸钠的总化学方程式
(3)下列说法正确的是
| A.将锌粉投入水中形成悬浮液主要是为了加快反应速率 |
| B.向Na2S2O4溶液中加NaCl溶液或固体对Na2S2O4的产率无明显影响 |
| C.洗涤Na2S2O4•2H2O时用冰水洗涤效果比酒精好 |
| D.单向阀的主要作用是防倒吸 |
a.将一定量的Zn粉与蒸馏水混合搅拌成悬浊液
b.将一定量的Zn粉与NaOH溶液混合搅拌成悬浊液
c.将一定量的Zn粉与HCl混合搅拌成悬浊液
d.向悬浊液中通入SO2至澄清,并加热
e.28~35℃加热条件下,向悬浊液中通入SO2至澄清
f.28~35℃加热条件下,向悬浊液中加入Na2SO3溶液
g.向溶液中滴加NaOH至pH在8.2~10.5之间
h.向溶液中滴加HCl至pH在8.2以下
i.向溶液中滴加1mol•L-1NaOH至pH在10.5以上
(5)称取上述制得的连二亚硫酸钠样品0.0870g加入另一三颈烧瓶,通过自动电位滴定仪控制滴定管向三颈烧瓶中快速滴加K3[Fe(CN)6]溶液将连二亚硫酸钠氧化为硫酸钠,记录终点读数,共消耗10.00mL0.2000mol•L-1的K3[Fe(CN)6]溶液,则样品中连二亚硫酸钠的纯度为
您最近一年使用:0次
8 .  是一种优良的饮用水处理剂,可用
是一种优良的饮用水处理剂,可用 、
、 、
、 混合共熔反应制得:
混合共熔反应制得: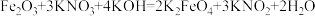 。下列关于该反应的说法
。下列关于该反应的说法不正确 的是
 是一种优良的饮用水处理剂,可用
是一种优良的饮用水处理剂,可用 、
、 、
、 混合共熔反应制得:
混合共熔反应制得: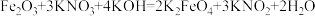 。下列关于该反应的说法
。下列关于该反应的说法A. 是还原剂, 是还原剂,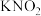 为还原产物 为还原产物 |
B.在熔融条件下氧化性: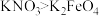 |
C.每生成 ,转移 ,转移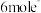 |
D. 在处理饮用水过程中起氧化、杀菌、脱色、除味、净水等作用 在处理饮用水过程中起氧化、杀菌、脱色、除味、净水等作用 |
您最近一年使用:0次
2023-01-02更新
|
527次组卷
|
3卷引用:浙江省杭州学军中学2022-2023学年高三上学期模拟考试化学试题
解题方法
9 . 红矶钠 是重要的化工原料,工业上以铬铁矿(
是重要的化工原料,工业上以铬铁矿( ,含少量
,含少量 、
、 )为主要原料制备红矾钠的工艺流程如下:
)为主要原料制备红矾钠的工艺流程如下:

已知:i. ii.
ii.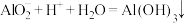
回答下列问题:
(1)焙烧铬铁矿生成 ,并将
,并将 和
和 转化为可溶性钠盐。
转化为可溶性钠盐。
①焙烧时为加快反应速率,可采取的措施是_______ 。
②生成 的化学方程式如下,将其补充完整:
的化学方程式如下,将其补充完整:_______ 。
□ +□
+□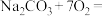 □______+□
□______+□ +□
+□
(2)滤液2中含有的溶质有: 、
、_______ 。
(3)中和时 的理论范围为4.5~9.3,调控
的理论范围为4.5~9.3,调控 不过高也不能过低的理由
不过高也不能过低的理由_______ 。
(4)酸化后所得溶液中主要含有 和
和 。
。

①结晶时,将混合溶液加热浓缩、_______ (填操作)、冷却结晶、过滤得到红矾钠晶体。
②滤液5最适宜返回上述流程_______ 中,参与循环再利用。
(5)工业上还可用膜电解技术(装置如图所示),以 为主要原料制备
为主要原料制备 ,结合化学用语简述制备
,结合化学用语简述制备 的原理:
的原理:_______ 。

(6) 可用于测定水体的COD(COD是指每升水样中还原性物质被氧化所需要
可用于测定水体的COD(COD是指每升水样中还原性物质被氧化所需要 的质量)。现有某水样
的质量)。现有某水样 ,酸化后加入
,酸化后加入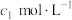 的
的 溶液
溶液 ,使水样中的还原性物质完全被氧化;再用
,使水样中的还原性物质完全被氧化;再用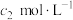 的
的 溶液滴定剩余的
溶液滴定剩余的 ,消耗
,消耗 溶液
溶液 ,则该水样的
,则该水样的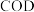 为
为_______  。【
。【 被还原为
被还原为 ;换算关系:
;换算关系: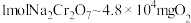 】
】
 是重要的化工原料,工业上以铬铁矿(
是重要的化工原料,工业上以铬铁矿( ,含少量
,含少量 、
、 )为主要原料制备红矾钠的工艺流程如下:
)为主要原料制备红矾钠的工艺流程如下:
已知:i.
 ii.
ii.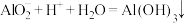
回答下列问题:
(1)焙烧铬铁矿生成
 ,并将
,并将 和
和 转化为可溶性钠盐。
转化为可溶性钠盐。①焙烧时为加快反应速率,可采取的措施是
②生成
 的化学方程式如下,将其补充完整:
的化学方程式如下,将其补充完整:□
 +□
+□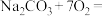 □______+□
□______+□ +□
+□
(2)滤液2中含有的溶质有:
 、
、(3)中和时
 的理论范围为4.5~9.3,调控
的理论范围为4.5~9.3,调控 不过高也不能过低的理由
不过高也不能过低的理由(4)酸化后所得溶液中主要含有
 和
和 。
。
①结晶时,将混合溶液加热浓缩、
②滤液5最适宜返回上述流程
(5)工业上还可用膜电解技术(装置如图所示),以
 为主要原料制备
为主要原料制备 ,结合化学用语简述制备
,结合化学用语简述制备 的原理:
的原理:
(6)
 可用于测定水体的COD(COD是指每升水样中还原性物质被氧化所需要
可用于测定水体的COD(COD是指每升水样中还原性物质被氧化所需要 的质量)。现有某水样
的质量)。现有某水样 ,酸化后加入
,酸化后加入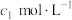 的
的 溶液
溶液 ,使水样中的还原性物质完全被氧化;再用
,使水样中的还原性物质完全被氧化;再用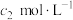 的
的 溶液滴定剩余的
溶液滴定剩余的 ,消耗
,消耗 溶液
溶液 ,则该水样的
,则该水样的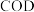 为
为 。【
。【 被还原为
被还原为 ;换算关系:
;换算关系: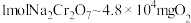 】
】
您最近一年使用:0次
解题方法
10 . 最近,科学家发现对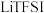 (一种亲水有机盐)进行掺杂和改进,能显著提高锂离子电池传输电荷的能力。
(一种亲水有机盐)进行掺杂和改进,能显著提高锂离子电池传输电荷的能力。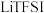 的结构如图所示,其中A、B、C、D为同一短周期元素,C与E位于同一主族。下列叙述正确的是
的结构如图所示,其中A、B、C、D为同一短周期元素,C与E位于同一主族。下列叙述正确的是
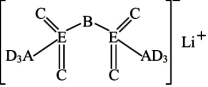
 (一种亲水有机盐)进行掺杂和改进,能显著提高锂离子电池传输电荷的能力。
(一种亲水有机盐)进行掺杂和改进,能显著提高锂离子电池传输电荷的能力。 的结构如图所示,其中A、B、C、D为同一短周期元素,C与E位于同一主族。下列叙述正确的是
的结构如图所示,其中A、B、C、D为同一短周期元素,C与E位于同一主族。下列叙述正确的是
| A.简单气态氢化物的稳定性:D>C>E |
| B.C是空气中含量最高的元素 |
| C.该化合物中只有A、C、D元素原子的最外层满足8电子稳定结构 |
D. 与E的简单阴离子在溶液中能大量共存 与E的简单阴离子在溶液中能大量共存 |
您最近一年使用:0次



