1 . 铁是人类较早使用的金属之一,回答下列问题。
(1)下列所含铁元素只有还原性的物质是___________ (填字母)。
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性,能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是___________ (填字母)。
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:___________ 。
(4)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:___________ 。
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式___________ ;若反应过程中转移了0.3 mol电子,则还原产物的物质的量为___________ mol。
(1)下列所含铁元素只有还原性的物质是
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性,能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(4)请设计实验检验在空气中放置的硫酸亚铁溶液已部分变质:
(5)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式
您最近一年使用:0次
解题方法
2 . 在无色透明强酸性溶液中,能大量共存的离子组是
A. | B. |
C. | D.Na+、Fe2+、Ba2+、ClO- |
您最近一年使用:0次
名校
3 . 能正确表示下列反应的离子方程式的是
| A.氯化铁溶液腐蚀铜箔:Fe3++Cu=Fe2++Cu2+ |
| B.向FeBr2溶液中通入过量Cl2:2Fe2++Cl2=2Fe3++2Cl﹣ |
C.向Na2CO3溶液中滴入少量盐酸:CO +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| D.用“胃舒平”治疗胃酸过多:Al(OH)3+3H+=Al3++3H2O |
您最近一年使用:0次
4 . 下列离子方程式正确的是
| A.Na2O2放入水中:Na2O2+H2O=2Na++2OH-+O2↑ |
| B.Na投入FeSO4溶液:2Na+Fe2+=2Na++Fe |
| C.用铝粉和NaOH溶液反应制取少量H2:Al+OH-+3H2O=2[Al(OH)4]-+3H2↑ |
D.向AlCl3溶液中滴加足量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH |
您最近一年使用:0次
名校
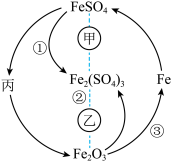
5 . 在一定条件下,某些物质具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题:
(1)根据分析可知丙为________________ (填化学式);甲可能是__________ (填标号,下同),乙可能是__________ 。
A.稀硝酸 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液
(2)实验室保存 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量___________ (填药品名称);可以用______________ (填化学式)溶液来检验 溶液中的
溶液中的 是否被氧化。
是否被氧化。
(3)丙的悬浊液在空气中变色的原因为____________________ (填化学方程式);工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是____________________ (填化学方程式)。
(1)根据分析可知丙为
A.稀硝酸 B.
 溶液 C.
溶液 C. D.
D. 溶液
溶液(2)实验室保存
 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量 溶液中的
溶液中的 是否被氧化。
是否被氧化。(3)丙的悬浊液在空气中变色的原因为
您最近一年使用:0次
2024-04-21更新
|
159次组卷
|
2卷引用:河北省保定市定州市第二中学2023-2024学年高一下学期3月月考化学试题
名校
6 . 铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)湿法制备高铁酸钾的反应体系有六种微粒: 。
。
①在碱性条件下,湿法生产高铁酸钾的离子反应方程式是______ 。
②若反应过程中转移了0.6mol电子,则还原产物的物质的量为______ mol。
③高铁酸钾作为一种理想的水处理剂,其处理水的原理______
(2)铁明矾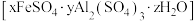 常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
①称取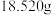 样品,准确配成100mL溶液A。
样品,准确配成100mL溶液A。
②量取 溶液A,加入盐酸酸化的
溶液A,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
体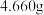 。
。
③再量取 溶液A,滴加适量稀硫酸,用
溶液A,滴加适量稀硫酸,用 溶液滴定至终点,生成
溶液滴定至终点,生成 ,消耗
,消耗 溶液
溶液 。
。
(已知 、
、 的相对分子质量分别是152、342)
的相对分子质量分别是152、342)
①在25.00mL试样中,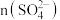
______ mol,
______ mol。
②铁明矾的化学式为______ (写出详细的解题步骤)
(1)湿法制备高铁酸钾的反应体系有六种微粒:
 。
。①在碱性条件下,湿法生产高铁酸钾的离子反应方程式是
②若反应过程中转移了0.6mol电子,则还原产物的物质的量为
③高铁酸钾作为一种理想的水处理剂,其处理水的原理
(2)铁明矾
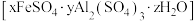 常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。
常用于制备高效复合型高效混凝剂。其组成通过下列实验测定。①称取
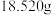 样品,准确配成100mL溶液A。
样品,准确配成100mL溶液A。②量取
 溶液A,加入盐酸酸化的
溶液A,加入盐酸酸化的 溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固
溶液至沉淀完全,过滤、洗涤,干燥至恒重,得到白色固体
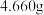 。
。③再量取
 溶液A,滴加适量稀硫酸,用
溶液A,滴加适量稀硫酸,用 溶液滴定至终点,生成
溶液滴定至终点,生成 ,消耗
,消耗 溶液
溶液 。
。(已知
 、
、 的相对分子质量分别是152、342)
的相对分子质量分别是152、342)①在25.00mL试样中,
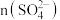

②铁明矾的化学式为
您最近一年使用:0次
名校
7 . 下列过程中的化学反应,相应的离子方程式正确的是
| A.氢氧化钡与稀硫酸溶液混合:H++OH-=H2O |
| B.稀盐酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ |
| C.氯化亚铁溶液中通入Cl2:2Fe2++Cl2=2Fe3++2Cl- |
D.稀盐酸和碳酸钙反应制取CO2: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
您最近一年使用:0次
名校
8 . 下列离子在溶液中因发生氧化还原反应而不能大量共存的是
A.H+、NO 、Fe2+、Na+ 、Fe2+、Na+ | B.Ag+、NO 、Cl-、K+ 、Cl-、K+ |
C.K+、Ba2+、OH-、SO | D.Cu2+、NH 、Br-、OH- 、Br-、OH- |
您最近一年使用:0次
2024-04-21更新
|
85次组卷
|
2卷引用:福建省南安市侨光中学2023-2024学年高一下学期4月月考化学试题
名校
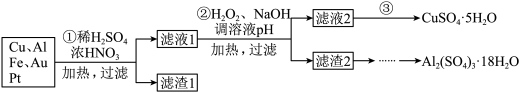
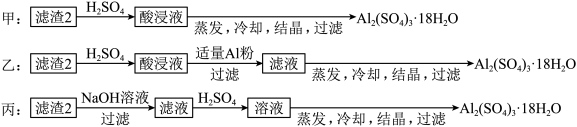
9 . 信息时代产生的大量电子垃圾对环境造成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线。_______ ;得到滤渣1的主要成分为_______ 。
(2)步骤①中能否用稀盐酸代替稀硫酸?_______ (填“能”或“否”)。
(3)步骤②加入H2O2的作用是_______ 。
(4)从滤液2获得硫酸铜晶体的方法是蒸发浓缩、_______ 。该过程可能会用到以下实验仪器中的:_______ 。(写名称)_______ 方案不可行,原因是_______ 。
(2)步骤①中能否用稀盐酸代替稀硫酸?
(3)步骤②加入H2O2的作用是
(4)从滤液2获得硫酸铜晶体的方法是蒸发浓缩、

您最近一年使用:0次
10 . 已知A、B、C均为含铁化合物,请根据以下四种物质的转化过程回答相关问题:
Fe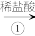 A
A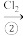 B
B C
C
(1)反应①、②、③中属于氧化还原反应的是 。
(2)关于B的溶液,说法正确的是 。
(3)选择合适的试剂也可以实现B转化为A,且考虑不能引入杂质,能实现该转化的方程式 。
Fe
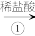 A
A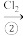 B
B C
C(1)反应①、②、③中属于氧化还原反应的是 。
| A.①② | B.①③ | C.②③ | D.①②③ |
| A.滴入几滴KSCN溶液后,可观察到溶液变血红色 |
| B.可与Fe反应,不能与Cu反应 |
| C.若加入NaOH溶液有红褐色沉淀生成 |
| D.Cl2 是氧化剂,可用双氧水替换 |
| A.2FeCl3+Fe=3FeCl2 | B.2FeCl3+Zn=2FeCl2+ZnCl2 |
| C.4Fe(OH)2+2H2O+O2=4Fe(OH)3 | D.2KI+2FeCl3=2KCl+2FeCl2+I2 |
您最近一年使用:0次



