名校
1 . 下列物质的应用中,利用了氧化还原反应原理的是
A. 补血剂与维生素C配合使用效果 补血剂与维生素C配合使用效果 |
| B.二氧化碳灭火 |
| C.小苏打中和胃酸 |
| D.稀硫酸除铁锈更佳 |
您最近一年使用:0次
名校
2 . 下列各组离子在强酸性条件下能大量共存的是
A.Ba2+、Na+、I-、NO | B.Ca2+、SO 、NO 、NO 、Cl- 、Cl- |
C.K+、Na+、Cl-、SO | D.NH 、Fe2+、Cl-、NO 、Fe2+、Cl-、NO |
您最近一年使用:0次
解题方法
3 . 工业上用FeCl3溶液做印刷电路铜板的腐蚀液。化学小组设计如下流程对腐蚀废液(阳离子主要有H+、Fe3+、Fe2+和Cu2+)进行处理,实现FeCl3溶液再生并回收Cu。
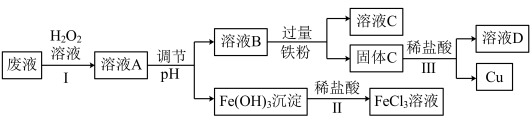
(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:_____________ ;
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为__________ ;
(3)步骤Ⅱ中发生反应的化学方程式为_____________ ;
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?_____________ ;
(5)固体C中的成分为________________ (填化学式);
(6)步骤Ⅲ中发生反应的离子方程式为___________ ,分离的操作名称为_______ 。

(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为
(3)步骤Ⅱ中发生反应的化学方程式为
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?
(5)固体C中的成分为
(6)步骤Ⅲ中发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
4 . 利用下列装置(夹持装置略)进行实验,下列说法不正确的是


| A.用甲装置检验H2中的HCl |
| B.用乙装置可以制取H2、CO2、SO2、NH3、NO等气体 |
| C.装置丙从FeSO4溶液中获得纯净的FeSO4固体 |
| D.甲丁所示仪器不能提纯Fe(OH)3胶体 |
您最近一年使用:0次
解题方法
5 . 某化学兴趣小组利用下列试剂:铁粉、锌粉、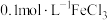 溶液,
溶液,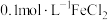 溶液,
溶液, 溶液;淀粉溶液,
溶液;淀粉溶液, 溶液,新制氯水,探究
溶液,新制氯水,探究 的氧化性、还原性,并利用实验结论解决一些问题。
的氧化性、还原性,并利用实验结论解决一些问题。
(1) 原子在周期表中的位置是
原子在周期表中的位置是___________ 。
(2)用所给试剂写出体现 具有还原性的反应的化学方程式
具有还原性的反应的化学方程式___________ 。
(3)设计实验方案,完成下列表格。
(4)该兴趣小组为说明“ 具有氧化性”,提出了向
具有氧化性”,提出了向 溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为
溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为___________ 。
(5) 溶液中加入
溶液中加入 溶液,是为了检验
溶液,是为了检验 的
的___________ (填“氧化性”或“还原性”),在溶液中 与
与
___________ (填“能”或“不能”)大量共存,如果不能大量共存,请写出该反应的离子方程式___________ 。
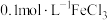 溶液,
溶液,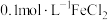 溶液,
溶液, 溶液;淀粉溶液,
溶液;淀粉溶液, 溶液,新制氯水,探究
溶液,新制氯水,探究 的氧化性、还原性,并利用实验结论解决一些问题。
的氧化性、还原性,并利用实验结论解决一些问题。(1)
 原子在周期表中的位置是
原子在周期表中的位置是(2)用所给试剂写出体现
 具有还原性的反应的化学方程式
具有还原性的反应的化学方程式(3)设计实验方案,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 |
探究 具有氧化性 具有氧化性 | ①取少量 溶液,往溶液中加入足量铁粉,再加入少量 溶液,往溶液中加入足量铁粉,再加入少量 溶液 溶液 | 加入铁粉后,溶液颜色变为 |
②取少量 溶液,往溶液中滴入3滴 溶液,往溶液中滴入3滴 溶液,然后再滴加2滴淀粉溶液 溶液,然后再滴加2滴淀粉溶液 | 加入淀粉溶液可观察到 |
(4)该兴趣小组为说明“
 具有氧化性”,提出了向
具有氧化性”,提出了向 溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为
溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为(5)
 溶液中加入
溶液中加入 溶液,是为了检验
溶液,是为了检验 的
的 与
与
您最近一年使用:0次
名校
解题方法
6 . 某兴趣小组研究铁盐的制备和性质。
实验I.制备FeCl2:装置如图所示(加持装置省略);已知FeCl2极易水解。
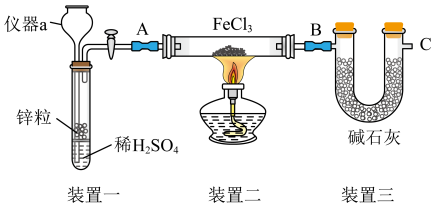
(1)仪器a的名称是_______ 。
(2)装置二中制备FeCl2的化学方程式是_____ ,装置三的作用是①_____ ;②_____ 。
(3)该装置存在一定的缺陷,可在_______ 位置(填“A”“B”或“C”)增加如下装置。如下装置中气体从_______ (填“a”或“b”)流入;洗气瓶中盛装的是_______ 。
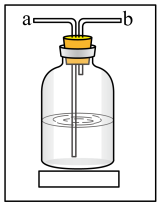
(4)为消除工业废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,用离子方程式表示处理过程的原理_______ 。
实验Ⅱ.探究性质
(5) FeCl2溶液滴加NaOH溶液后会出现灰绿色沉淀,有同学猜测灰绿色沉淀是Fe(OH)2和Fe(OH)3的混合物。为探究是否存在Fe(OH)2,可取灰绿色沉淀,向其中加入_______ 溶液,再加入_______ 溶液,若观察到_______ 现象,证明灰绿色沉淀中含有Fe(OH)2。
实验I.制备FeCl2:装置如图所示(加持装置省略);已知FeCl2极易水解。

(1)仪器a的名称是
(2)装置二中制备FeCl2的化学方程式是
(3)该装置存在一定的缺陷,可在

(4)为消除工业废气中的Cl2对环境的污染,将废气通过含有铁粉的FeCl2溶液,即可有效地除去Cl2,用离子方程式表示处理过程的原理
实验Ⅱ.探究性质
(5) FeCl2溶液滴加NaOH溶液后会出现灰绿色沉淀,有同学猜测灰绿色沉淀是Fe(OH)2和Fe(OH)3的混合物。为探究是否存在Fe(OH)2,可取灰绿色沉淀,向其中加入
您最近一年使用:0次
名校
7 . 下列说法不正确的是
| A.FeO是一种黑色粉末,不稳定,在空气中受热能被O2氧化 |
| B.用Cl2对自来水消毒水,Cl2会与水中的有机物反应,生成的有机氯化物可能对人体有害 |
| C.检验Fe2+时,可在FeCl2溶液中滴加酸性KMnO4溶液,观察紫红色是否褪去 |
| D.硫酸铁、硫酸铝可用于净水 |
您最近一年使用:0次
8 . 下列说法不正确 的是
A. 为白色固体,易被空气氧化 为白色固体,易被空气氧化 |
B.工业上常用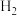 和 和 直接化合的方法生产氯化氢以制得盐酸 直接化合的方法生产氯化氢以制得盐酸 |
C.实验室常用 溶液吸收多余的 溶液吸收多余的 以避免污染 以避免污染 |
D.将废铁屑加入 溶液中,可用于除去工业废气中的 溶液中,可用于除去工业废气中的 |
您最近一年使用:0次
9 . 氧化铁黄 是一种黄色颜料,在环境保护等领域也有广泛应用。
是一种黄色颜料,在环境保护等领域也有广泛应用。
(1)在 下,向
下,向 溶液中边搅拌边分批加入
溶液中边搅拌边分批加入 固体,同时滴加
固体,同时滴加 溶液,使溶液
溶液,使溶液 控制在弱酸性。一段时间后,过滤、洗涤得
控制在弱酸性。一段时间后,过滤、洗涤得 固体。
固体。
①制备 理论上需要
理论上需要 的物质的量为
的物质的量为__________  ;实际生产过程中所加
;实际生产过程中所加 低于理论用量的原因是
低于理论用量的原因是__________ 。
②为检验 已被完全氧化,某同学向过滤所得滤液中滴加酸性
已被完全氧化,某同学向过滤所得滤液中滴加酸性 溶液,该设计方案不合理的理由是
溶液,该设计方案不合理的理由是__________ 。
(2)色光度是产品质量的指标之一,合格氧化铁黄 的色光度值范围为
的色光度值范围为 。氧化过程溶液
。氧化过程溶液 对产率、色光度的影响如题图所示,氧化时应控制
对产率、色光度的影响如题图所示,氧化时应控制 的合理范围是
的合理范围是 过小或过大均会导致产率较低,其可能原因是
过小或过大均会导致产率较低,其可能原因是__________ 。

(3)也可用空气氧化 溶液制取氧化铁黄
溶液制取氧化铁黄 ,该反应中
,该反应中 起催化作用,催化机理分两步完成,第一步:
起催化作用,催化机理分两步完成,第一步: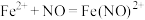 ,第二步:…….请写出第二步反应的离子方程式
,第二步:…….请写出第二步反应的离子方程式__________ 。
(4) 可用于脱除烟气中的
可用于脱除烟气中的 。脱硫、再生过程中可能的物种变化如题图所示。生成的
。脱硫、再生过程中可能的物种变化如题图所示。生成的 (结构如图所示)覆盖在
(结构如图所示)覆盖在 的表面.写出反应Ⅱ的化学方程式
的表面.写出反应Ⅱ的化学方程式__________ 。

 是一种黄色颜料,在环境保护等领域也有广泛应用。
是一种黄色颜料,在环境保护等领域也有广泛应用。(1)在
 下,向
下,向 溶液中边搅拌边分批加入
溶液中边搅拌边分批加入 固体,同时滴加
固体,同时滴加 溶液,使溶液
溶液,使溶液 控制在弱酸性。一段时间后,过滤、洗涤得
控制在弱酸性。一段时间后,过滤、洗涤得 固体。
固体。①制备
 理论上需要
理论上需要 的物质的量为
的物质的量为 ;实际生产过程中所加
;实际生产过程中所加 低于理论用量的原因是
低于理论用量的原因是②为检验
 已被完全氧化,某同学向过滤所得滤液中滴加酸性
已被完全氧化,某同学向过滤所得滤液中滴加酸性 溶液,该设计方案不合理的理由是
溶液,该设计方案不合理的理由是(2)色光度是产品质量的指标之一,合格氧化铁黄
 的色光度值范围为
的色光度值范围为 。氧化过程溶液
。氧化过程溶液 对产率、色光度的影响如题图所示,氧化时应控制
对产率、色光度的影响如题图所示,氧化时应控制 的合理范围是
的合理范围是 过小或过大均会导致产率较低,其可能原因是
过小或过大均会导致产率较低,其可能原因是
(3)也可用空气氧化
 溶液制取氧化铁黄
溶液制取氧化铁黄 ,该反应中
,该反应中 起催化作用,催化机理分两步完成,第一步:
起催化作用,催化机理分两步完成,第一步: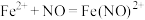 ,第二步:…….请写出第二步反应的离子方程式
,第二步:…….请写出第二步反应的离子方程式(4)
 可用于脱除烟气中的
可用于脱除烟气中的 。脱硫、再生过程中可能的物种变化如题图所示。生成的
。脱硫、再生过程中可能的物种变化如题图所示。生成的 (结构如图所示)覆盖在
(结构如图所示)覆盖在 的表面.写出反应Ⅱ的化学方程式
的表面.写出反应Ⅱ的化学方程式
您最近一年使用:0次
解题方法
10 . 下列离子方程式书写正确的是
A.硫酸铝溶液与过量氨水反应: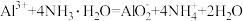 |
B. 与 与 溶液反应: 溶液反应: |
C.向次氯酸钠溶液中通入少量二氧化碳: |
D.向碘化亚铁溶液中通入过量氯气: |
您最近一年使用:0次



