解题方法
1 . X、Y、Z、W为原子序数依次增大的短周期主族元素,X与Y同族;科学家在核反应中用中子(即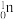 )轰击
)轰击 ,得到核素
,得到核素 和
和 ,即
,即 。下列说法错误的是
。下列说法错误的是
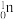 )轰击
)轰击 ,得到核素
,得到核素 和
和 ,即
,即 。下列说法错误的是
。下列说法错误的是| A.4种元素中W的非金属性最强 | B.原子半径: |
| C.Y与X、W均可形成离子化合物 | D.W的氢化物的沸点一定高于Z的氢化物 |
您最近一年使用:0次
2 . 新型碲化镉(CdTe)太阳能电池能量转化效率较高,立方晶系CdTe的晶胞结构如图所示,晶胞参数为apm(已知Te与O同族)。下列说法正确的是

| A.碲原子的价层电子数为4 | B.Cd的配位数为4 |
C.晶胞中Cd与Te的最短距离为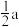 pm pm | D.晶体的密度为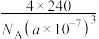 g⋅cm g⋅cm |
您最近一年使用:0次
3 . 工业合成氨是人类科学技术上的一项重大突破,是化学对社会发展的巨大贡献之一。在催化剂作用下发生
 ,回答下列问题:
,回答下列问题:
(1)依据键能信息,
__________  。
。
(2)其他条件不变,下列能加快反应速率,并提高 的平衡转化率的是__________(填字母)。
的平衡转化率的是__________(填字母)。
(3)恒温恒容条件下,下列能说明该反应已达到平衡状态的是____(填字母)
(4)在恒容密闭容器中,初始时氮气和氢气的体积比是1:3,300℃、500℃条件下平衡时氨的体积分数随压强( )的变化示意图,以及10MPa、30MPa条件下平衡时氨的体积分数随温度(
)的变化示意图,以及10MPa、30MPa条件下平衡时氨的体积分数随温度( )的变化示意图如下。
)的变化示意图如下。__________ (填“a”“b”“c”或“d”)。
②M、N、Q三点对应的平衡常数分别为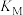 、
、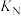 、
、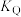 ,三平衡常数的大小关系为
,三平衡常数的大小关系为_________ 。
(5)400℃、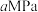 条件下,初始时氮气和氢气的体积比是
条件下,初始时氮气和氢气的体积比是 ,平衡时氨气的体积分数为60%,则该条件下反应的压强平衡常数
,平衡时氨气的体积分数为60%,则该条件下反应的压强平衡常数
__________  。
。
(6)利用质子传导固态电池合成氨示意图如下,生成氨气的电极反应式为____________________ 。 用于制氨水和铵盐。常温下,将浓度均为
用于制氨水和铵盐。常温下,将浓度均为 氨水和
氨水和 溶液等体积混合,混合溶液显
溶液等体积混合,混合溶液显__________ (填“酸性”“碱性”或“中性”),混合溶液
__________ 。已知:常温下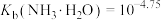

 ,回答下列问题:
,回答下列问题:化学键 |
|
|
|
键能(kJ/mol) | 946 | 436 | 391 |

 。
。(2)其他条件不变,下列能加快反应速率,并提高
 的平衡转化率的是__________(填字母)。
的平衡转化率的是__________(填字母)。A.固定体系体积,加大 投料量 投料量 | B.升高反应体系的温度 |
| C.降低平衡体系的压强 | D.改用效果更好的催化剂 |
| A.气体的密度保持不变 | B. 、 、 、 、 的物质的量之比为 的物质的量之比为 |
| C.气体的平均摩尔质量保持不变 | D.消耗 ,同时消耗 ,同时消耗 |
 )的变化示意图,以及10MPa、30MPa条件下平衡时氨的体积分数随温度(
)的变化示意图,以及10MPa、30MPa条件下平衡时氨的体积分数随温度( )的变化示意图如下。
)的变化示意图如下。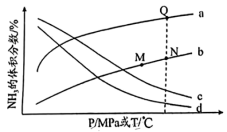
②M、N、Q三点对应的平衡常数分别为
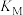 、
、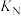 、
、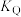 ,三平衡常数的大小关系为
,三平衡常数的大小关系为(5)400℃、
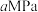 条件下,初始时氮气和氢气的体积比是
条件下,初始时氮气和氢气的体积比是 ,平衡时氨气的体积分数为60%,则该条件下反应的压强平衡常数
,平衡时氨气的体积分数为60%,则该条件下反应的压强平衡常数
 。
。(6)利用质子传导固态电池合成氨示意图如下,生成氨气的电极反应式为
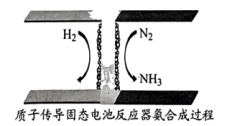
 用于制氨水和铵盐。常温下,将浓度均为
用于制氨水和铵盐。常温下,将浓度均为 氨水和
氨水和 溶液等体积混合,混合溶液显
溶液等体积混合,混合溶液显
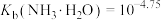
您最近一年使用:0次
4 . 某温度下,饱和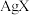 和
和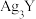 溶液,
溶液,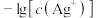 与
与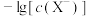 、
、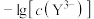 的关系如图所示,
的关系如图所示, 为两线段的交点。下列说法错误的是
为两线段的交点。下列说法错误的是
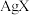 和
和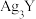 溶液,
溶液,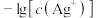 与
与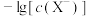 、
、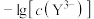 的关系如图所示,
的关系如图所示, 为两线段的交点。下列说法错误的是
为两线段的交点。下列说法错误的是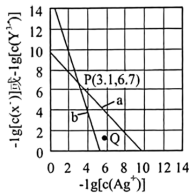
A.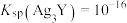 |
| B.图中a代表AgX溶液 |
C.Q点所对应AgX生成沉淀,而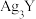 不生成沉淀 不生成沉淀 |
D.向NaX、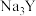 均为 均为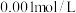 混合溶液中滴加 混合溶液中滴加 溶液,先产生 溶液,先产生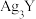 沉淀 沉淀 |
您最近一年使用:0次
5 . 某人体内可合成的重要化合物结构如图,W、X、Y、Z、Q是原子序数依次增大的短周期主族元素。下列叙述错误的是
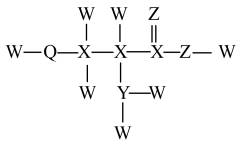
A.第一电离能: | B.物质沸点: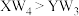 |
C.共价键键角: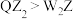 | D.基态Y、Z原子的未成对电子数之比为3:2 |
您最近一年使用:0次
6 . 阿斯巴甜是一种合成甜味剂,结构如图所示。下列有关该物质的说法正确的是
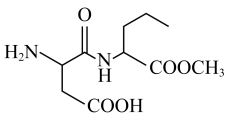
A.分子式为 | B.含有5种官能团 |
| C.1mol该物质可与3molNaOH反应 | D.1mol该物质中含有4mol碳氧 键 键 |
您最近一年使用:0次
7 . 工厂利用电解法处理含醛类废水,并由邻溴硝基苯制备邻溴苯胺,工作原理如图所示:

A.b电极的电极反应为: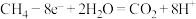 |
B.当生成 邻溴苯胺,同时可以处理含有 邻溴苯胺,同时可以处理含有 的废水 的废水 |
C.电解过程中 极区溶液的酸性减弱 极区溶液的酸性减弱 |
D.工作时,电极 和 和 均发生氧化反应 均发生氧化反应 |
您最近一年使用:0次
解题方法
8 . 草酸合铜酸钾(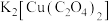 )是一种重要的化工原料,实验室可以通过氧化铜和草酸氢钾反应进行制备,具体步骤如下:
)是一种重要的化工原料,实验室可以通过氧化铜和草酸氢钾反应进行制备,具体步骤如下:
Ⅰ.称取2.0 g (
(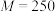 g⋅mol
g⋅mol ),用40 mL水溶解,再加入10 mL 2 mol⋅L
),用40 mL水溶解,再加入10 mL 2 mol⋅L NaOH溶液,加热至沉淀由蓝色变为黑色。
NaOH溶液,加热至沉淀由蓝色变为黑色。
Ⅱ.继续煮沸15 min,稍冷后过滤,洗涤沉淀三次。
Ⅲ.称取3.0 g ,用80 mL水微热溶解。稍冷后分数次加入适量
,用80 mL水微热溶解。稍冷后分数次加入适量 固体,制得
固体,制得 和
和 混合溶液。
混合溶液。
Ⅳ.将Ⅲ的溶液加热至80~85℃,再加入Ⅰ中的黑色沉淀,充分反应至沉淀溶解后,趁热过滤。
V.取滤液,经多步操作,得到固体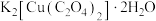 (
(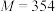 g⋅mol
g⋅mol )。将固体用滤纸吸干后称量,质量为1.77 g。
)。将固体用滤纸吸干后称量,质量为1.77 g。
回答下列问题:
(1)步骤Ⅰ中使用的部分仪器如下。___________ ,加快 溶解的操作有
溶解的操作有___________ 。
(2)步骤Ⅱ中检验沉淀是否洗涤干净的操作和现象为___________ 。
(3)步骤Ⅳ中加入氧化铜后,由 生成
生成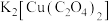 的化学方程式为
的化学方程式为___________ 。
(4)步骤Ⅴ中多步操作包括:___________ ,___________ ,过滤,洗涤。
(5)本实验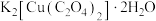 的产率为
的产率为___________ 。
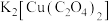 )是一种重要的化工原料,实验室可以通过氧化铜和草酸氢钾反应进行制备,具体步骤如下:
)是一种重要的化工原料,实验室可以通过氧化铜和草酸氢钾反应进行制备,具体步骤如下:Ⅰ.称取2.0 g
 (
(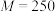 g⋅mol
g⋅mol ),用40 mL水溶解,再加入10 mL 2 mol⋅L
),用40 mL水溶解,再加入10 mL 2 mol⋅L NaOH溶液,加热至沉淀由蓝色变为黑色。
NaOH溶液,加热至沉淀由蓝色变为黑色。Ⅱ.继续煮沸15 min,稍冷后过滤,洗涤沉淀三次。
Ⅲ.称取3.0 g
 ,用80 mL水微热溶解。稍冷后分数次加入适量
,用80 mL水微热溶解。稍冷后分数次加入适量 固体,制得
固体,制得 和
和 混合溶液。
混合溶液。Ⅳ.将Ⅲ的溶液加热至80~85℃,再加入Ⅰ中的黑色沉淀,充分反应至沉淀溶解后,趁热过滤。
V.取滤液,经多步操作,得到固体
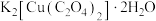 (
(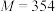 g⋅mol
g⋅mol )。将固体用滤纸吸干后称量,质量为1.77 g。
)。将固体用滤纸吸干后称量,质量为1.77 g。回答下列问题:
(1)步骤Ⅰ中使用的部分仪器如下。

 溶解的操作有
溶解的操作有(2)步骤Ⅱ中检验沉淀是否洗涤干净的操作和现象为
(3)步骤Ⅳ中加入氧化铜后,由
 生成
生成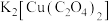 的化学方程式为
的化学方程式为(4)步骤Ⅴ中多步操作包括:
(5)本实验
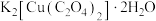 的产率为
的产率为
您最近一年使用:0次
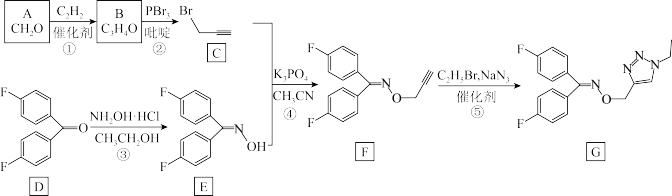
9 . 化合物G具有良好的抗肿瘤生物活性,其合成路线如下:
(1)反应①的反应类型是___________ ;B的结构简式是___________ 。
(2)C的化学名称为___________ 。
(3)D中官能团的名称是___________ 。
(4)反应④的反应方程式为___________ ;研究发现该反应存在反应限度,加入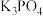 能提高F的产率,其原因是
能提高F的产率,其原因是___________ 。
(5)X是D的同分异构体,写出满足如下条件的X的结构简式___________ 。(不考虑立体异构,只需写出3个)
①与D具有完全相同的官能团;
②含有两个苯环且两个氟原子连接在同一个苯环上。
(6)利用以上合成路线中的相关反应,设计由苯乙烯和溴乙烷制备 的合成路线:
的合成路线:___________ (无机试剂任选)。
(1)反应①的反应类型是
(2)C的化学名称为
(3)D中官能团的名称是
(4)反应④的反应方程式为
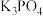 能提高F的产率,其原因是
能提高F的产率,其原因是(5)X是D的同分异构体,写出满足如下条件的X的结构简式
①与D具有完全相同的官能团;
②含有两个苯环且两个氟原子连接在同一个苯环上。
(6)利用以上合成路线中的相关反应,设计由苯乙烯和溴乙烷制备
 的合成路线:
的合成路线:
您最近一年使用:0次
10 . 我国秦俑彩绘和汉代器物上用的颜料被称为“中国蓝”、“中国紫”,近年来,人们对这些颜料的成分进行了研究,发现其主要成分为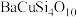 、
、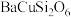 。回答下列问题:
。回答下列问题:
(1)颜料中含有Cu元素,基态Cu原子的价电子排布式为___________ ;Si、O、Ba元素电负性由大到小的顺序为___________ ,干冰、Si、SiC熔点由高到低的顺序为___________ 。
(2)“中国蓝”的发色中心是以 为中心离子的配位化合物,其中提供孤电子对的是
为中心离子的配位化合物,其中提供孤电子对的是___________ 元素。
(3)铜可作 氧化生成
氧化生成 的催化剂。乙醇的沸点高于乙醛,其主要原因是
的催化剂。乙醇的沸点高于乙醛,其主要原因是___________ 。
(4)C、N元素与颜料中的氧元素同周期。
①写出CO的一种常见等电子体分子的电子式___________ 。C、N、O的第一电离能由大到小的顺序为___________ 。
②C、N元素能形成一种类石墨的聚合物半导体 ,其单层平面结构如图1,晶胞结构如图2。
,其单层平面结构如图1,晶胞结构如图2。 中氮原子的杂化类型是
中氮原子的杂化类型是___________ 。已知该晶胞的体积为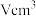 ,中间层原子均在晶胞内部。设阿伏加德罗常数的值为
,中间层原子均在晶胞内部。设阿伏加德罗常数的值为 ,则
,则 的密度是
的密度是___________  (列出计算表达式)。
(列出计算表达式)。
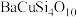 、
、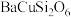 。回答下列问题:
。回答下列问题:(1)颜料中含有Cu元素,基态Cu原子的价电子排布式为
(2)“中国蓝”的发色中心是以
 为中心离子的配位化合物,其中提供孤电子对的是
为中心离子的配位化合物,其中提供孤电子对的是(3)铜可作
 氧化生成
氧化生成 的催化剂。乙醇的沸点高于乙醛,其主要原因是
的催化剂。乙醇的沸点高于乙醛,其主要原因是(4)C、N元素与颜料中的氧元素同周期。
①写出CO的一种常见等电子体分子的电子式
②C、N元素能形成一种类石墨的聚合物半导体
 ,其单层平面结构如图1,晶胞结构如图2。
,其单层平面结构如图1,晶胞结构如图2。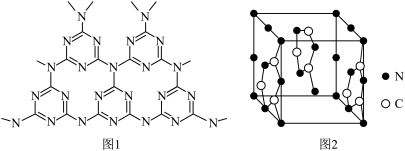
 中氮原子的杂化类型是
中氮原子的杂化类型是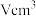 ,中间层原子均在晶胞内部。设阿伏加德罗常数的值为
,中间层原子均在晶胞内部。设阿伏加德罗常数的值为 ,则
,则 的密度是
的密度是 (列出计算表达式)。
(列出计算表达式)。
您最近一年使用:0次






