解题方法
1 . 最近,《NanoEnergy》报道了一种“全氢电池”,吸附层M、N均为惰性电极,其工作原理如图所示。下列说法正确的是
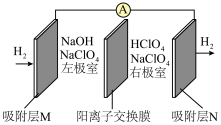
| A.电极电势:吸附层M>吸附层N |
B.吸附层M电极反应为: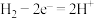 |
C.工作时, 通过阳离子交换膜由右极室移向左极室 通过阳离子交换膜由右极室移向左极室 |
D.工作一段时间后,M电极消耗的 与N电极产生的 与N电极产生的 体积比约为 体积比约为 |
您最近一年使用:0次
解题方法
2 . 宏观辨识与微观探析是化学学科核心素养之一。下列化学实验对应的离子方程式书写正确的是
A.铁丝插入稀硝酸中: |
B.向 溶液中加入稀硫酸: 溶液中加入稀硫酸: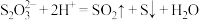 |
C.氯化铜溶液中通入 : :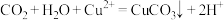 |
D.向 溶液加入足量NaOH溶液: 溶液加入足量NaOH溶液: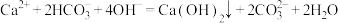 |
您最近一年使用:0次
解题方法
3 . 环丙叉环丙烷(a)是一个新的多功能有机合成分子。以环丙叉环丙烷、 、
、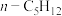 为原料制备化合物b、c、d的反应如下。下列说法正确的是
为原料制备化合物b、c、d的反应如下。下列说法正确的是
 、
、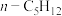 为原料制备化合物b、c、d的反应如下。下列说法正确的是
为原料制备化合物b、c、d的反应如下。下列说法正确的是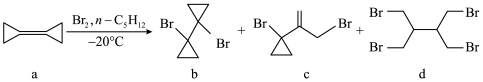
A.a的分子式为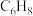 | B.b中所有原子共平面 |
| C.c能发生加成反应,不能发生取代反应 | D.b、c、d互为同系物 |
您最近一年使用:0次
4 . 常温下,向20 mL浓度均为0.1 mol⋅L 盐酸和醋酸(
盐酸和醋酸(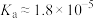 )的混合溶液中滴加0.1 mol⋅L
)的混合溶液中滴加0.1 mol⋅L 的氨水(
的氨水(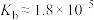 ),测得混合溶液的电阻率(电阻率越大,导电能力越弱)与加入氨水的体积的关系如图所示(忽略混合时体积变化),下列叙述正确的是
),测得混合溶液的电阻率(电阻率越大,导电能力越弱)与加入氨水的体积的关系如图所示(忽略混合时体积变化),下列叙述正确的是
 盐酸和醋酸(
盐酸和醋酸(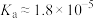 )的混合溶液中滴加0.1 mol⋅L
)的混合溶液中滴加0.1 mol⋅L 的氨水(
的氨水(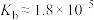 ),测得混合溶液的电阻率(电阻率越大,导电能力越弱)与加入氨水的体积的关系如图所示(忽略混合时体积变化),下列叙述正确的是
),测得混合溶液的电阻率(电阻率越大,导电能力越弱)与加入氨水的体积的关系如图所示(忽略混合时体积变化),下列叙述正确的是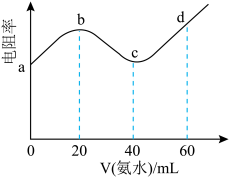
A.a→c过程中,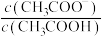 逐渐增大 逐渐增大 |
| B.c→d过程中,水的电离程度一直增大 |
C.c点溶液中,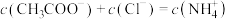 |
D.d点时,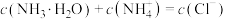 |
您最近一年使用:0次
解题方法
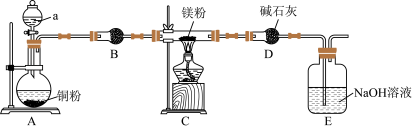
5 . 镁及其化合物是实验设计的热点载体。某学习小组设计实验探究镁与二氧化氮反应的产物,实验装置如图所示。 能与水反应;②反应完后E中有
能与水反应;②反应完后E中有 。
。
回答下列问题:
(1)仪器a的名称为___________ ;a中试剂是___________ 。
(2)实验时,为了防止Mg与空气中氧气等反应,操作为___________ 。
(3)实验测得Mg与 反应生成MgO、
反应生成MgO、 和
和 ,其中
,其中 和
和 的物质的量相等,则C中反应的化学方程式为
的物质的量相等,则C中反应的化学方程式为___________ 。装置D的作用是___________ 。
(4)E装置中发生反应的离子方程式为___________ 。
(5)写出氮化镁与水反应的化学方程式___________ 。
(6)已知浓硝酸分解反应为: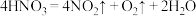 ,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出
,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出 气体能支持燃烧的说法,你认为该说法正确吗?并说明理由
气体能支持燃烧的说法,你认为该说法正确吗?并说明理由___________ 。
 能与水反应;②反应完后E中有
能与水反应;②反应完后E中有 。
。回答下列问题:
(1)仪器a的名称为
(2)实验时,为了防止Mg与空气中氧气等反应,操作为
(3)实验测得Mg与
 反应生成MgO、
反应生成MgO、 和
和 ,其中
,其中 和
和 的物质的量相等,则C中反应的化学方程式为
的物质的量相等,则C中反应的化学方程式为(4)E装置中发生反应的离子方程式为
(5)写出氮化镁与水反应的化学方程式
(6)已知浓硝酸分解反应为:
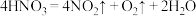 ,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出
,干燥生成的气体后,该气体混合物能使带火星的木条复燃,由此某同学得出 气体能支持燃烧的说法,你认为该说法正确吗?并说明理由
气体能支持燃烧的说法,你认为该说法正确吗?并说明理由
您最近一年使用:0次
解题方法
6 . X、Y、Z、W为原子序数依次增大的短周期主族元素,X与Y同族;科学家在核反应中用中子(即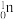 )轰击
)轰击 ,得到核素
,得到核素 和
和 ,即
,即 。下列说法错误的是
。下列说法错误的是
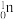 )轰击
)轰击 ,得到核素
,得到核素 和
和 ,即
,即 。下列说法错误的是
。下列说法错误的是| A.4种元素中W的非金属性最强 | B.原子半径: |
| C.Y与X、W均可形成离子化合物 | D.W的氢化物的沸点一定高于Z的氢化物 |
您最近一年使用:0次
7 . 新型碲化镉(CdTe)太阳能电池能量转化效率较高,立方晶系CdTe的晶胞结构如图所示,晶胞参数为apm(已知Te与O同族)。下列说法正确的是

| A.碲原子的价层电子数为4 | B.Cd的配位数为4 |
C.晶胞中Cd与Te的最短距离为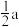 pm pm | D.晶体的密度为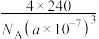 g⋅cm g⋅cm |
您最近一年使用:0次
8 . 工业合成氨是人类科学技术上的一项重大突破,是化学对社会发展的巨大贡献之一。在催化剂作用下发生
 ,回答下列问题:
,回答下列问题:
(1)依据键能信息,
__________  。
。
(2)其他条件不变,下列能加快反应速率,并提高 的平衡转化率的是__________(填字母)。
的平衡转化率的是__________(填字母)。
(3)恒温恒容条件下,下列能说明该反应已达到平衡状态的是____(填字母)
(4)在恒容密闭容器中,初始时氮气和氢气的体积比是1:3,300℃、500℃条件下平衡时氨的体积分数随压强( )的变化示意图,以及10MPa、30MPa条件下平衡时氨的体积分数随温度(
)的变化示意图,以及10MPa、30MPa条件下平衡时氨的体积分数随温度( )的变化示意图如下。
)的变化示意图如下。__________ (填“a”“b”“c”或“d”)。
②M、N、Q三点对应的平衡常数分别为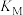 、
、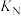 、
、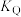 ,三平衡常数的大小关系为
,三平衡常数的大小关系为_________ 。
(5)400℃、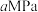 条件下,初始时氮气和氢气的体积比是
条件下,初始时氮气和氢气的体积比是 ,平衡时氨气的体积分数为60%,则该条件下反应的压强平衡常数
,平衡时氨气的体积分数为60%,则该条件下反应的压强平衡常数
__________  。
。
(6)利用质子传导固态电池合成氨示意图如下,生成氨气的电极反应式为____________________ 。 用于制氨水和铵盐。常温下,将浓度均为
用于制氨水和铵盐。常温下,将浓度均为 氨水和
氨水和 溶液等体积混合,混合溶液显
溶液等体积混合,混合溶液显__________ (填“酸性”“碱性”或“中性”),混合溶液
__________ 。已知:常温下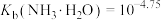

 ,回答下列问题:
,回答下列问题:化学键 |
|
|
|
键能(kJ/mol) | 946 | 436 | 391 |

 。
。(2)其他条件不变,下列能加快反应速率,并提高
 的平衡转化率的是__________(填字母)。
的平衡转化率的是__________(填字母)。A.固定体系体积,加大 投料量 投料量 | B.升高反应体系的温度 |
| C.降低平衡体系的压强 | D.改用效果更好的催化剂 |
| A.气体的密度保持不变 | B. 、 、 、 、 的物质的量之比为 的物质的量之比为 |
| C.气体的平均摩尔质量保持不变 | D.消耗 ,同时消耗 ,同时消耗 |
 )的变化示意图,以及10MPa、30MPa条件下平衡时氨的体积分数随温度(
)的变化示意图,以及10MPa、30MPa条件下平衡时氨的体积分数随温度( )的变化示意图如下。
)的变化示意图如下。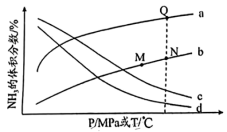
②M、N、Q三点对应的平衡常数分别为
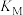 、
、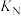 、
、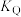 ,三平衡常数的大小关系为
,三平衡常数的大小关系为(5)400℃、
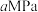 条件下,初始时氮气和氢气的体积比是
条件下,初始时氮气和氢气的体积比是 ,平衡时氨气的体积分数为60%,则该条件下反应的压强平衡常数
,平衡时氨气的体积分数为60%,则该条件下反应的压强平衡常数
 。
。(6)利用质子传导固态电池合成氨示意图如下,生成氨气的电极反应式为
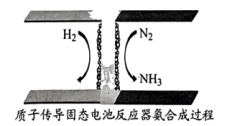
 用于制氨水和铵盐。常温下,将浓度均为
用于制氨水和铵盐。常温下,将浓度均为 氨水和
氨水和 溶液等体积混合,混合溶液显
溶液等体积混合,混合溶液显
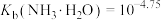
您最近一年使用:0次
9 . 某温度下,饱和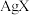 和
和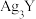 溶液,
溶液,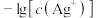 与
与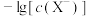 、
、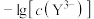 的关系如图所示,
的关系如图所示, 为两线段的交点。下列说法错误的是
为两线段的交点。下列说法错误的是
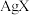 和
和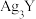 溶液,
溶液,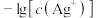 与
与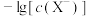 、
、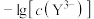 的关系如图所示,
的关系如图所示, 为两线段的交点。下列说法错误的是
为两线段的交点。下列说法错误的是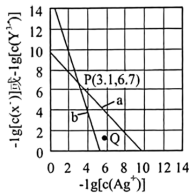
A.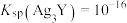 |
| B.图中a代表AgX溶液 |
C.Q点所对应AgX生成沉淀,而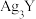 不生成沉淀 不生成沉淀 |
D.向NaX、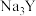 均为 均为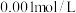 混合溶液中滴加 混合溶液中滴加 溶液,先产生 溶液,先产生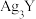 沉淀 沉淀 |
您最近一年使用:0次
10 . 某人体内可合成的重要化合物结构如图,W、X、Y、Z、Q是原子序数依次增大的短周期主族元素。下列叙述错误的是
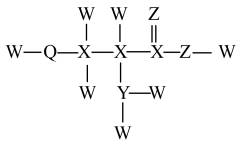
A.第一电离能: | B.物质沸点: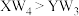 |
C.共价键键角: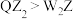 | D.基态Y、Z原子的未成对电子数之比为3:2 |
您最近一年使用:0次






