名校
1 . 下列生活中常见物质不属于传统无机非金属材料的是
| A.水泥 | B.玻璃 | C.陶瓷 | D.铁钉 |
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式正确的是
A.铜和稀硝酸反应:3Cu + 8H+ +2 = 3Cu2+ +2 NO↑ + 4H2O = 3Cu2+ +2 NO↑ + 4H2O |
B.亚硫酸钠溶液与酸化的硝酸钡混合: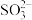 + Ba2+ = BaSO3↓ + Ba2+ = BaSO3↓ |
C.浓NaOH溶液与浓NH4Cl溶液混合加热: +OH- +OH- NH3 NH3 H2O H2O |
D.向Na2SiO3溶液中加入过量CO2: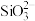 +H2O+CO2=H2SiO3↓+ +H2O+CO2=H2SiO3↓+ |
您最近一年使用:0次
名校
3 . W、X、Y、Z是短周期主族元素中的四种非金属元素,原子序数依次增大,X、Z同主族,Y、Z同周期,W原子中只有一个质子;Z原子的最外层电子数是核外电子层数的2倍。下列说法正确的是
| A.非金属性:X<Z | B.原子半径:Y>Z>X>W |
| C.含氧酸的酸性:Y<Z | D.气态氢化物的稳定性:Y>Z>X |
您最近一年使用:0次
名校
解题方法
4 . 下列离子能大量共存的是
A.Na+、 、I-、OH- 、I-、OH- | B.Na+、H+、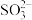 、S2- 、S2- |
| C.Ba2+、K+、Cl-、OH- | D.H+、Ca2+、Fe2+、 |
您最近一年使用:0次
名校
解题方法
5 . 正确掌握化学用语是学好化学的基础,下列化学用语使用正确的是
A. 的质子数为53,中子数为131 的质子数为53,中子数为131 | B.14C和14N互称为同位素 |
| C.次氯酸的结构式:H-O-Cl | D.氟化铵的电子式: |
您最近一年使用:0次
名校
解题方法
6 . 化学与生活、科技密切相关。下列说法正确的是
| A.碳酸钡难溶于水,医疗上可用作X射线透视肠胃的内服药“钡餐” |
| B.可穿戴式智能测温设备的测温芯片主要成分是硅酸盐 |
| C.食品包装袋中常有硅胶、生石灰、还原铁粉等,其作用都是防止食品氧化变质 |
| D.富勒烯是由碳原子构成的一系列笼形分子的总称,属于新型无机非金属材料 |
您最近一年使用:0次
名校
解题方法
7 . 下列变化是通过取代反应来实现的是
| A.CH3CH2OH→CH3 CHO | B.CH2=CHCH3→CH2=CHCH2Cl |
C.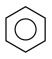 → →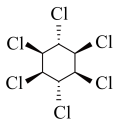 | D.CH3 CHO→CH3 CH2OH |
您最近一年使用:0次
名校
解题方法
8 . 根据要求回答问题
(1)已知:键线式要点
a.分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略
b.环形结构用相应边数的多边形来表示
c.杂原子(非碳、氢原子)不得省略,并且其上连有的氢也不省略
①一氯甲烷生成二氯甲烷___________ 。
②乙烯通入溴水中___________ 。
③苯的硝化___________ 。
④苯和氢气___________ 。
(3)已知有机物有如下转化关系,其中C的产量可用来衡量一个国家的石油化工发展水平,G的分子式为C10H14O4,试回答下列有关问题。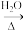 R-OH+NaX (R-表示烃基,X表示卤原子)。
R-OH+NaX (R-表示烃基,X表示卤原子)。
①A的分子式为___________ 。
②G的结构简式为___________ 。
③反应E→F的反应类型:___________ ,B+F→G的反应类型:___________ 。
④C生成D的化学方程式:___________ ;D生成E的化学方程式:___________ ;A生成B的化学方程式:___________ 。
(1)已知:键线式要点
a.分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略
b.环形结构用相应边数的多边形来表示
c.杂原子(非碳、氢原子)不得省略,并且其上连有的氢也不省略
①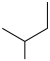 的系统命名为
的系统命名为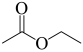 的名称为
的名称为
②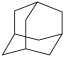 (四个等同的六元环组成)的分子式为
(四个等同的六元环组成)的分子式为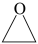 的分子式为
的分子式为
①一氯甲烷生成二氯甲烷
②乙烯通入溴水中
③苯的硝化
④苯和氢气
(3)已知有机物有如下转化关系,其中C的产量可用来衡量一个国家的石油化工发展水平,G的分子式为C10H14O4,试回答下列有关问题。
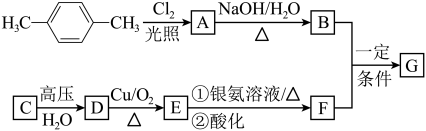
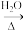 R-OH+NaX (R-表示烃基,X表示卤原子)。
R-OH+NaX (R-表示烃基,X表示卤原子)。①A的分子式为
②G的结构简式为
③反应E→F的反应类型:
④C生成D的化学方程式:
您最近一年使用:0次
名校
解题方法
9 . 某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的离子方程式有___________ 。
(2)要加快上述实验中气体产生的速率,还可采取的措施有___________ (写两种)。
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间。
①请完成此实验设计,其中:V1=___________ ,V6=___________ ,V9=___________ 。
②反应一段时间后,实验A中的金属呈___________ 色,实验E中的金属呈___________ 色。
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率变化的主要原因:___________ 。
(1)上述实验中发生反应的离子方程式有
(2)要加快上述实验中气体产生的速率,还可采取的措施有
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间。
| 混合溶液 | A | B | C | D | E | F |
| 4 mol·L-1 H2SO4溶液/mL | 40 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②反应一段时间后,实验A中的金属呈
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率变化的主要原因:
您最近一年使用:0次
名校
10 . 已知X(g)和Y(g)可以相互转化:2X(g) Y(g)。现将一定量X(g)和Y(g)的混合气体通入一体积为1L的恒温密闭容器中,反应物及生成物的浓度随时间变化的关系如图所示。
Y(g)。现将一定量X(g)和Y(g)的混合气体通入一体积为1L的恒温密闭容器中,反应物及生成物的浓度随时间变化的关系如图所示。
 Y(g)。现将一定量X(g)和Y(g)的混合气体通入一体积为1L的恒温密闭容器中,反应物及生成物的浓度随时间变化的关系如图所示。
Y(g)。现将一定量X(g)和Y(g)的混合气体通入一体积为1L的恒温密闭容器中,反应物及生成物的浓度随时间变化的关系如图所示。
| A.若混合气体的总质量不变,则说明反应已达到化学平衡状态 |
| B.a、b、c、d四个点,表示化学反应处于平衡状态的只有a点 |
| C.25~30min内用X表示的平均反应速率是0.08 mol·L-1·min-1 |
| D.反应进行至25min时,曲线发生变化的原因是增大压强 |
您最近一年使用:0次



