1 . 下列关于苯的叙述正确的是
| A.1 mol苯最多可与3 mol H2发生加成反应 |
| B.苯在光照条件下可以和Cl2发生取代反应 |
| C.苯分子含有不饱和键,可以使溴水和高锰酸钾溶液褪色 |
| D.苯和Br2的四氯化碳溶液混合,能发生加成反应且溶液分为两层 |
您最近一年使用:0次
2 . 由乙烯推测丙烯(CH2=CH-CH3)的结构或性质错误的是
| A.燃烧能产生明亮火焰并伴有黑烟 | B.分子中所有原子都在同一平面上 |
| C.能使溴的四氯化碳溶液褪色 | D.能使酸性高锰酸钾溶液褪色 |
您最近一年使用:0次
名校
3 . 下列说法正确的是
| A.乙烯分子中6个原子一定在同一平面上,结构简式为CH2CH2 |
| B.乙烯能使Br2的CCl4溶液和酸性KMnO4溶液退色,二者退色的原理相同 |
| C.溴水能鉴别乙烷和乙烯,也能除去乙烷中的乙烯 |
| D.乙烯和乙烷均可与Cl2反应制取纯净的氯乙烷 |
您最近一年使用:0次
名校
解题方法
4 . 下列有关烷烃的叙述中,不正确的是
| A.在烷烃分子中,所有的化学键都为单键 |
| B.随着碳原子数的增加,烷烃的熔沸点逐渐升高 |
| C.CH4、CH3Cl都是正四面体结构的烷烃,都能和氯气发生取代反应 |
| D.CH2Cl2只有一种结构能证明甲烷分子是以碳原子为中心的正四面体 |
您最近一年使用:0次
5 .  某烃能与
某烃能与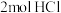 完全加成,加成后产物上的氢原子最多能被
完全加成,加成后产物上的氢原子最多能被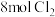 取代,则该烃可能为
取代,则该烃可能为
 某烃能与
某烃能与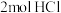 完全加成,加成后产物上的氢原子最多能被
完全加成,加成后产物上的氢原子最多能被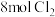 取代,则该烃可能为
取代,则该烃可能为| A.2—丁烯 | B.1,3—丁二烯 | C.正丁烷 | D.乙炔 |
您最近一年使用:0次
名校
解题方法
6 . I.甲醇是重要的化工原料,发展前景广阔。
温度为T1时,向容积为2L的密闭容器甲、乙中分别充入一定量的CO和H2O(g),发生反应:CO(g) + H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g) 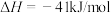 。相关数据如下:
。相关数据如下:
(1)甲容器中,反应在t1 min 内的平均速率v(H2)= ___________ mol/(L·min)。
(2)甲容器中,平衡时,反应放出的热量___________ kJ。
(3)T1时,反应的平衡常数K甲=___________ 。
(4)乙容器中,a=___________ mol。
II.实验探究
兴趣小组同学为探究影响化学反应速率及化学平衡的因素,设计以下实验:___________ 。
(6)利用实验II探究浓度对化学平衡的影响。
已知:Cr2O (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+ 推测B试管中实验现象为
(黄色)+2H+ 推测B试管中实验现象为___________ ,用平衡移动原理解释原因:___________ 。
(7)该小组同学继续用酸性KMnO4溶液和草酸(H2C2O4)溶液进行实验,实验操作及现象如下表:
已知: 。
。
①由实验i、实验ii可得出的结论是___________ 。
②关于实验ii中80s后溶液颜色迅速变浅的原因,该小组同学提出了猜想:反应中生成的Mn2+对反应有催化作用。利用下列提供的试剂设计实验iii,验证猜想。
提供的试剂:0.01mol/L酸性KMnO4溶液,0.1mol/L草酸溶液,3mol/L硫酸, MnSO4固体,蒸馏水。
补全实验iii的操作:向试管中先加入5mL0.01mol/L酸性KMnO4溶液,___________ ,最后加入5mL0.1mol/L草酸溶液。
温度为T1时,向容积为2L的密闭容器甲、乙中分别充入一定量的CO和H2O(g),发生反应:CO(g) + H2O(g)
 CO2(g)+H2(g)
CO2(g)+H2(g) 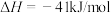 。相关数据如下:
。相关数据如下:| 容器 | 甲 | 乙 | ||
| 反应物 | CO | H2O | CO | H2O |
| 起始时物质的量(mol) | 1.2 | 0.6 | 2.4 | 1.2 |
| 平衡时物质的量(mol) | 0.8 | 0.2 | a | b |
| 达到平衡的时间(min) | t1 | t2 | ||
(2)甲容器中,平衡时,反应放出的热量
(3)T1时,反应的平衡常数K甲=
(4)乙容器中,a=
II.实验探究
兴趣小组同学为探究影响化学反应速率及化学平衡的因素,设计以下实验:

(6)利用实验II探究浓度对化学平衡的影响。
已知:Cr2O
 (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+ 推测B试管中实验现象为
(黄色)+2H+ 推测B试管中实验现象为(7)该小组同学继续用酸性KMnO4溶液和草酸(H2C2O4)溶液进行实验,实验操作及现象如下表:
| 编号 | 实验操作 | 实验现象 |
| i | 向一支试管中先加入5mL0.01mol/L酸性KMnO4溶液,再加入1滴3mol/L硫酸和9滴蒸馏水,最后加入5mL0.1mol/L草酸溶液 | 前10min内溶液紫色无明显变化,后颜色逐渐变浅,30min后几乎变为无色 |
| ii | 向另一支试管中先加入5mL0.01mol/L酸性KMnO4溶液,再加入10滴3mol/L硫酸,最后加入5mL0.1mol/L草酸溶液 | 80s内溶液紫色无明显变化,后颜色迅速变浅,约150s后几乎变为无色 |
 。
。①由实验i、实验ii可得出的结论是
②关于实验ii中80s后溶液颜色迅速变浅的原因,该小组同学提出了猜想:反应中生成的Mn2+对反应有催化作用。利用下列提供的试剂设计实验iii,验证猜想。
提供的试剂:0.01mol/L酸性KMnO4溶液,0.1mol/L草酸溶液,3mol/L硫酸, MnSO4固体,蒸馏水。
补全实验iii的操作:向试管中先加入5mL0.01mol/L酸性KMnO4溶液,
您最近一年使用:0次
7 . 电解质的水溶液跟日常生活、工农业生产和环境保护息息相关。常温下,叠氮酸 是一元弱酸,高锰酸
是一元弱酸,高锰酸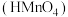 是一元强酸,
是一元强酸, 的高铼酸
的高铼酸 、
、 的高锰酸
的高锰酸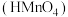 溶液分别与
溶液分别与 的
的 溶液等体积混合,所得溶液均呈中性。请回答下列问题:
溶液等体积混合,所得溶液均呈中性。请回答下列问题:
(1)高铼酸属于___________ (填“强”或“弱”)酸,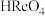 中Re的化合价为
中Re的化合价为___________ 。
(2)常温下,已知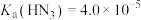 ,则
,则 的
的 溶液中
溶液中
___________  。
。
(3)已知25°C时, 的
的 ;
; 的:
的: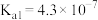
 ;HCN的
;HCN的 ,回答下列问题:
,回答下列问题:
①25°C时,向NaCN溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为___________ 。
②下列措施中能使醋酸的水溶液中 增大的同时
增大的同时 减小的是
减小的是___________ (填标号)。
A.加入 固体 B.加入固体
固体 B.加入固体 C.加入NaCN固体 D.升高温度
C.加入NaCN固体 D.升高温度
(4)常温时
 溶液,
溶液, 浓度为
浓度为___________ ,由水电离的 为
为___________ 。
 是一元弱酸,高锰酸
是一元弱酸,高锰酸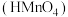 是一元强酸,
是一元强酸, 的高铼酸
的高铼酸 、
、 的高锰酸
的高锰酸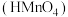 溶液分别与
溶液分别与 的
的 溶液等体积混合,所得溶液均呈中性。请回答下列问题:
溶液等体积混合,所得溶液均呈中性。请回答下列问题:(1)高铼酸属于
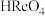 中Re的化合价为
中Re的化合价为(2)常温下,已知
 ,则
,则 的
的 溶液中
溶液中
 。
。(3)已知25°C时,
 的
的 ;
; 的:
的: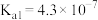
 ;HCN的
;HCN的 ,回答下列问题:
,回答下列问题:①25°C时,向NaCN溶液中通入少量
 ,反应的离子方程式为
,反应的离子方程式为②下列措施中能使醋酸的水溶液中
 增大的同时
增大的同时 减小的是
减小的是A.加入
 固体 B.加入固体
固体 B.加入固体 C.加入NaCN固体 D.升高温度
C.加入NaCN固体 D.升高温度(4)常温时

 溶液,
溶液, 浓度为
浓度为 为
为
您最近一年使用:0次
8 . 下列所述变化为吸热反应的是
A.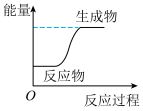 | B. | C. | D. |
您最近一年使用:0次
7日内更新
|
27次组卷
|
2卷引用:宁夏回族自治区石嘴山市平罗县平罗中学2023-2024学年高一下学期5月期中化学试题
名校
解题方法
9 . 下列化学用语表达正确的是
A.HClO的电子式: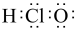 | B.镁原子最外层电子的电子云图: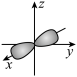 |
C.I3AsF6晶体中,I 的空间结构与水分子相同 的空间结构与水分子相同 | D.N2H4中N的杂化轨道: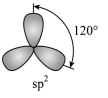 |
您最近一年使用:0次
名校
10 . 下列关于晶体的说法正确的组合是
①H2O比H2S分子更稳定,是因为H2O分子间存在氢键;
②金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低;
③在晶体中只要有阳离子就一定有阴离子;
④CaTiO3晶体的晶胞结构如图所示,则每个Ti4+ 和12个O2- 紧邻;
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合;
⑦1mol冰晶体中含4mol氢键;
⑧钠熔化时金属键被破坏,氯化钠熔化时离子键被破坏。
①H2O比H2S分子更稳定,是因为H2O分子间存在氢键;
②金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低;
③在晶体中只要有阳离子就一定有阴离子;
④CaTiO3晶体的晶胞结构如图所示,则每个Ti4+ 和12个O2- 紧邻;
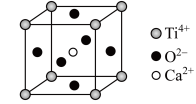
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合;
⑦1mol冰晶体中含4mol氢键;
⑧钠熔化时金属键被破坏,氯化钠熔化时离子键被破坏。
| A.①②③⑥ | B.①②④ | C.③⑤⑦ | D.②④⑧ |
您最近一年使用:0次



