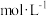1 . 在处理NO废气的过程中,催化剂 会逐渐失活变为
会逐渐失活变为 。
。
某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:i.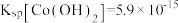 ;
;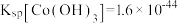 。
。
ii.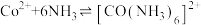
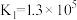 ;
;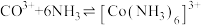
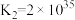 。
。
iii. 和
和 在酸性条件下均能生成
在酸性条件下均能生成 。
。
(1)探 的还原性
的还原性
实验I 粉红色的 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。
实验Ⅱ 向 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。 可以被酸性
可以被酸性 溶液氧化。乙同学补充实验IV,
溶液氧化。乙同学补充实验IV,_______ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。_______ 。
③根据氧化还原反应规律解释还原性 :
: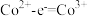 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使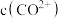 和
和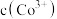 均降低,但
均降低,但_______ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验Ⅲ和IV推测氧化性: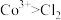 ,设计实验证明:向V中得到的棕褐色沉淀中,
,设计实验证明:向V中得到的棕褐色沉淀中,_______ (补全实验操作及现象),反应方程式为_______ 。
②向V中得到的棕褐色沉淀中,滴加 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是_______ 。
(3)催化剂 的失活与再生
的失活与再生
①结合数据解释 能被氧化为
能被氧化为 而失活的原因:
而失活的原因:_______ 。
②根据以上实验,设计物质转化流程图 实现 的再生:
的再生:_______ 。示例:
 会逐渐失活变为
会逐渐失活变为 。
。某小组为解决这一问题,实验研究
 和
和 之间的相互转化。
之间的相互转化。资料:i.
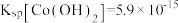 ;
;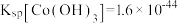 。
。ii.
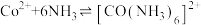
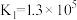 ;
;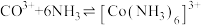
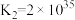 。
。iii.
 和
和 在酸性条件下均能生成
在酸性条件下均能生成 。
。(1)探
 的还原性
的还原性实验I 粉红色的
 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。实验Ⅱ 向
 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。
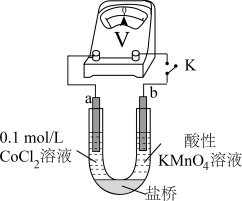
 可以被酸性
可以被酸性 溶液氧化。乙同学补充实验IV,
溶液氧化。乙同学补充实验IV,②探究碱性条件下
 的还原性,进行实验。
的还原性,进行实验。实验V: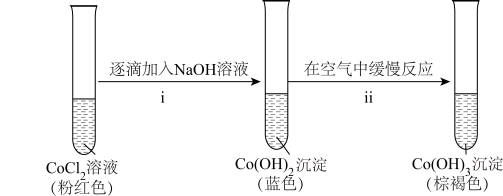
③根据氧化还原反应规律解释还原性
 :
: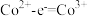 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使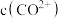 和
和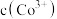 均降低,但
均降低,但(2)探究
 的氧化性
的氧化性①根据实验Ⅲ和IV推测氧化性:
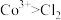 ,设计实验证明:向V中得到的棕褐色沉淀中,
,设计实验证明:向V中得到的棕褐色沉淀中,②向V中得到的棕褐色沉淀中,滴加
 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是(3)催化剂
 的失活与再生
的失活与再生①结合数据解释
 能被氧化为
能被氧化为 而失活的原因:
而失活的原因:②根据以上实验,设计物质转化
 的再生:
的再生:
您最近一年使用:0次
名校
2 . 某小组探究含Cr元素的化合物间的转化,进行如下实验。
资料:
i.含Cr元素的常见粒子: (橙色)、
(橙色)、 (黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、
(黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、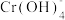 (亮绿色)。
(亮绿色)。
ii.H2O2在碱性环境中比在酸性环境中分解速率快。
iii.在碱性环境中,O2不能氧化+3价铬元素。
实验操作及现象如表:
(1)已知 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:
(黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:_____ 。
(2)I中,溶液由橙色变为绿色的总反应的离子方程式是_____ 。
(3)Ⅱ中,继续滴入NaOH溶液后,又有气泡生成的原因是_____ 。
(4)Ⅱ中,继续滴入NaOH溶液后,预测有Cr(OH)3沉淀生成,但实验时未观察到。
提出假设:在碱性环境中,+3价铬元素被H2O2氧化。
①甲同学设计实验证明假设成立:
取少量I中的绿色溶液,在滴入NaOH溶液前增加一步操作:______ 。然后滴入NaOH溶液,有蓝灰色沉淀生成,继续滴入NaOH溶液,沉淀溶解,溶液变为______ 色。
②乙同学进一步研究碱性环境对+3价铬元素的还原性或H2O2的氧化性的影响,设计如图实验。
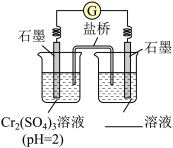
右侧烧杯的溶液中,氧化剂是_____ 。
开始时灵敏电流计指针不偏转,分别继续进行如下实验。
i.向左侧烧杯中滴入NaOH溶液,出现蓝灰色沉淀,继续缓慢滴入NaOH溶液,灵敏电流计指针向右偏转(电子从左向右运动),此时左侧的电极反应式为_____ 。
ii.向右侧烧杯中滴入NaOH溶液,有微小气泡生成,灵敏电流计指针向左偏转,左侧无明显变化。此时原电池中的总反应的化学方程式为_____ 。
(5)由上述实验, 与H2O2、
与H2O2、 与H2O2的氧化性强弱(填“>”或“<”):
与H2O2的氧化性强弱(填“>”或“<”):
酸性条件下,
_____ H2O2;碱性条件下, 
_____ H2O2。
资料:
i.含Cr元素的常见粒子:
 (橙色)、
(橙色)、 (黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、
(黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、 (亮绿色)。
(亮绿色)。ii.H2O2在碱性环境中比在酸性环境中分解速率快。
iii.在碱性环境中,O2不能氧化+3价铬元素。
实验操作及现象如表:
| 装置 | 步骤 | 操作 | 现象 |
 2mL0.0125mol•L-1K2Cr2O7溶液 | I | 先滴入稀硫酸至pH≈2,再滴入5滴5%H2O2溶液,振荡 | 溶液橙色加深。滴入H2O2溶液后迅速变为蓝紫色,有气泡生成。稍后,无明显气泡时,溶液由蓝紫色完全变为绿色 |
| Ⅱ | 继续缓慢滴入10滴2mol•L-1NaOH溶液,边滴,边振荡 | 又有气泡生成,溶液最终变为黄色 |
 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:
(黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:(2)I中,溶液由橙色变为绿色的总反应的离子方程式是
(3)Ⅱ中,继续滴入NaOH溶液后,又有气泡生成的原因是
(4)Ⅱ中,继续滴入NaOH溶液后,预测有Cr(OH)3沉淀生成,但实验时未观察到。
提出假设:在碱性环境中,+3价铬元素被H2O2氧化。
①甲同学设计实验证明假设成立:
取少量I中的绿色溶液,在滴入NaOH溶液前增加一步操作:
②乙同学进一步研究碱性环境对+3价铬元素的还原性或H2O2的氧化性的影响,设计如图实验。

右侧烧杯的溶液中,氧化剂是
开始时灵敏电流计指针不偏转,分别继续进行如下实验。
i.向左侧烧杯中滴入NaOH溶液,出现蓝灰色沉淀,继续缓慢滴入NaOH溶液,灵敏电流计指针向右偏转(电子从左向右运动),此时左侧的电极反应式为
ii.向右侧烧杯中滴入NaOH溶液,有微小气泡生成,灵敏电流计指针向左偏转,左侧无明显变化。此时原电池中的总反应的化学方程式为
(5)由上述实验,
 与H2O2、
与H2O2、 与H2O2的氧化性强弱(填“>”或“<”):
与H2O2的氧化性强弱(填“>”或“<”):酸性条件下,


您最近一年使用:0次
2023-01-07更新
|
408次组卷
|
4卷引用:北京市顺义牛栏山第一中学2022-2023学年高二下学期3月月考化学试题
名校
解题方法
3 . 在处理NO废气的过程中,催化剂[Co(NH3)6]2+会逐渐失活变为[Co(NH3)6]3+。某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105
Co3++6NH3 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035
iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH
(1)探究 的还原性
的还原性
实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。
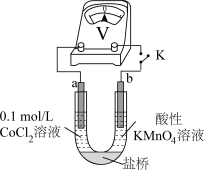
①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,____ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。
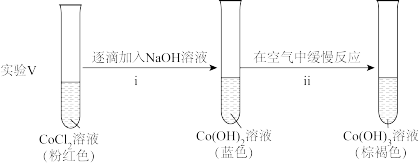
ii中反应的化学方程式是____ 。
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但____ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,____ (补全实验操作及现象),反应的离子方程式是____ 。
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是____ 。
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:____ 。
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:____ 。
示例:Co CoCl2
CoCl2 Co(OH)2
Co(OH)2
 和
和 之间的相互转化。
之间的相互转化。资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3
 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105Co3++6NH3
 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH

(1)探究
 的还原性
的还原性实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。

①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,
②探究碱性条件下
 的还原性,进行实验。
的还原性,进行实验。
ii中反应的化学方程式是
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但
(2)探究
 的氧化性
的氧化性①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:
示例:Co
 CoCl2
CoCl2 Co(OH)2
Co(OH)2
您最近一年使用:0次
2022-05-08更新
|
1351次组卷
|
9卷引用:北京市八一学校2022-2023学年高三上学期12月月考化学试题
4 . 某同学欲探究H2O2的氧化还原性:
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,其原因是___________ 。
(2)探究H2O2的氧化性可以选取的物质是:___________ (填序号)
①淀粉KI溶液 ②FeSO4溶液 ③Cl2④HNO3溶液
任选一个你所选的物质进行实验,观察到___________ 现象,证明H2O2有氧化性,反应的离子方程式为___________ 。
(3)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。
反应的离子方程式为___________ 。
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有___________ 性,能与H2O2反应产生MnO2
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
iii是ii和i的对照实验。
①X是___________ 。
②a是___________ 、b是___________ 。
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,其原因是
(2)探究H2O2的氧化性可以选取的物质是:
①淀粉KI溶液 ②FeSO4溶液 ③Cl2④HNO3溶液
任选一个你所选的物质进行实验,观察到
(3)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。
反应的离子方程式为
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
| 序号 | 实验 | 试剂 | 现象 |
| i | 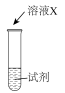 | a | 生成棕褐色固体,产生大量气泡 |
| ii | b | 有少量气泡 | |
| iii | H2O2溶液 | 有少量气泡 |
①X是
②a是
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
您最近一年使用:0次
名校
解题方法
5 . 某小组探究 和
和 的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
【实验探究】
实验i:向装有0.5g 的烧杯中加入20mL30%
的烧杯中加入20mL30% 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊, 片表面附着少量蓝色固体。
片表面附着少量蓝色固体。
(1)写出该反应的化学方程式:_______ 。
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
(2)实验ii中:溶液变蓝的原因是_______ (用离子反应方程式表示);经检验产生的气体为氧气,产生氧气的原因是_______ 。
(3)对比实验i和iii,为探究氨水对 的还原性或
的还原性或 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
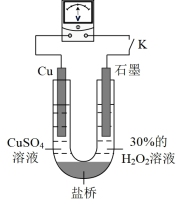
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①利用电极反应解释该实验的结论:_______ 。
②利用该方法也可证明酸性增强可提高 的氧化性,与上述实验操作不同的是
的氧化性,与上述实验操作不同的是_______ 。
(4)总结:物质氧化性和还原性变化的一般规律是_______ 。
(5)应用: 分别与
分别与 的盐酸、氢溴酸、氢碘酸混合,
的盐酸、氢溴酸、氢碘酸混合, 只与氢碘酸发生置换反应,试解释原因
只与氢碘酸发生置换反应,试解释原因_______ 。
 和
和 的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。【实验探究】
实验i:向装有0.5g
 的烧杯中加入20mL30%
的烧杯中加入20mL30% 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊, 片表面附着少量蓝色固体。
片表面附着少量蓝色固体。(1)写出该反应的化学方程式:
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
| 装置 | 序号 | 试剂a | 现象 |
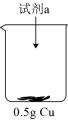 | ii | 20mL30% 与4mL 与4mL5mol/L  混合液 混合液 |  表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
| iii | 20mL30% 与4mL 与4mL5mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡, 表面有少量蓝色不溶物 表面有少量蓝色不溶物 |
(3)对比实验i和iii,为探究氨水对
 的还原性或
的还原性或 氧化性的影响,该同学利用如图装置继续实验。
氧化性的影响,该同学利用如图装置继续实验。
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
①利用电极反应解释该实验的结论:
②利用该方法也可证明酸性增强可提高
 的氧化性,与上述实验操作不同的是
的氧化性,与上述实验操作不同的是(4)总结:物质氧化性和还原性变化的一般规律是
(5)应用:
 分别与
分别与 的盐酸、氢溴酸、氢碘酸混合,
的盐酸、氢溴酸、氢碘酸混合, 只与氢碘酸发生置换反应,试解释原因
只与氢碘酸发生置换反应,试解释原因
您最近一年使用:0次
2022-06-03更新
|
542次组卷
|
4卷引用:北京市东直门中学2023-2024学年高三上学期12月阶段测试化学试题
北京市东直门中学2023-2024学年高三上学期12月阶段测试化学试题北京市和平街第一中学2021-2022学年高三下学期保温化学试题(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题(已下线)微专题 物质性质综合实验探究
名校
解题方法
6 . 某小组探究Cu和H2O2的反应的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
【实验探究】
实验i:向装有0.5g Cu的烧杯中加入20mL30% H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)①写出该反应的化学方程式:_______ 。
②电极反应式:
ⅰ.氧化反应:_______ 。
ⅱ.还原反应: H2O2+ 2e- = 2OH-
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
(2)实验ii中:溶液变蓝的原因是_______ (用化学方程式表示)。
(3)对比实验i和iii,为探究浓氨水对Cu的还原性或H2O2氧化性的影响,该同学利用下图装置继续实验。
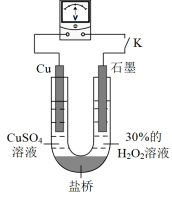
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加浓氨水后,电压减小了y。
c.继续向U型管左侧溶液中滴加浓氨水后,电压增大了z。
①从电极反应角度解释产生现象c的原因:_______ 。
②利用该方法也可证明酸性增强可提高H2O2的氧化性,具体实验操作及现象是_______ 。
(4)总结:物质氧化性和还原性变化的一般规律是_______ 。
【实验探究】
实验i:向装有0.5g Cu的烧杯中加入20mL30% H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)①写出该反应的化学方程式:
②电极反应式:
ⅰ.氧化反应:
ⅱ.还原反应: H2O2+ 2e- = 2OH-
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
| 装置 | 序号 | 试剂a | 现象 |
 | ii | 20mL30% H2O2与4mL5mol/L H2SO4混合液 | Cu表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
| iii | 20mL30% H2O2与4mL5mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物 |
(3)对比实验i和iii,为探究浓氨水对Cu的还原性或H2O2氧化性的影响,该同学利用下图装置继续实验。

已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加浓氨水后,电压减小了y。
c.继续向U型管左侧溶液中滴加浓氨水后,电压增大了z。
①从电极反应角度解释产生现象c的原因:
②利用该方法也可证明酸性增强可提高H2O2的氧化性,具体实验操作及现象是
(4)总结:物质氧化性和还原性变化的一般规律是
您最近一年使用:0次
7 . 某小组同学探究Cu和H2O2的反应。
【猜想预测】
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
【实验探究】
实验ⅰ:向装有0.5 g Cu的烧杯中加入20 mL 30% H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:________ 。
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2++ 4NH3⇌[ Cu(NH3)4]2+,[ Cu(NH3)4]2+为深蓝色;Cu(OH)2可溶于氨水形成深蓝色溶液。
(2)实验ⅱ中:溶液变蓝的原因是________ (用化学用语解释);经检验产生的气体为氧气,产生氧气的原因是________ 。
(3)对比实验ⅰ和ⅲ,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。
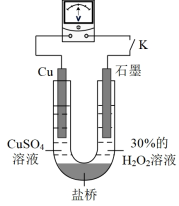
已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U形管右侧溶液中滴加氨水后,电压不变。
c.继续向U形管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:_________ 。利用该方法也可证明酸性增强可提高H2O2的氧化性,导致Cu溶解速率加快。
(4)对比实验ⅱ和ⅲ,实验ⅲ中产生氧气速率明显更快,可能的原因是_______ 。
(5)实验ⅲ有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因:________ 。
(6)基于以上实验,影响Cu与H2O2反应速率的因素有________ 。
【猜想预测】
猜想1:Cu与H2O2不发生反应;
猜想2:Cu与H2O2可能发生氧化还原反应,H2O2作氧化剂。
【实验探究】
实验ⅰ:向装有0.5 g Cu的烧杯中加入20 mL 30% H2O2溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)通过该实验证明了猜想2成立,写出该反应的化学方程式:
【继续探究】
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:Cu2++ 4NH3⇌[ Cu(NH3)4]2+,[ Cu(NH3)4]2+为深蓝色;Cu(OH)2可溶于氨水形成深蓝色溶液。
| 装置 | 序号 | 试剂a | 现象 |
 | ⅱ | 20 mL 30% H2O2与4 mL 5 mol/L H2SO4混合液 | Cu表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
| ⅲ | 20 mL 30% H2O2与4 mL5 mol/L氨水混合液 | 溶液立即变为深蓝色,产生大量气泡,Cu表面有少量蓝色不溶物 |
(2)实验ⅱ中:溶液变蓝的原因是
(3)对比实验ⅰ和ⅲ,为探究氨水对Cu的还原性或H2O2氧化性的影响,该同学利用如图装置继续实验。

已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大。
a.K闭合时,电压为x。
b.向U形管右侧溶液中滴加氨水后,电压不变。
c.继续向U形管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论:
(4)对比实验ⅱ和ⅲ,实验ⅲ中产生氧气速率明显更快,可能的原因是
(5)实验ⅲ有少量蓝色不溶物,小组同学加入少量NH4Cl可使其溶解,结合文字和化学用语解释不溶物溶解的原因:
(6)基于以上实验,影响Cu与H2O2反应速率的因素有
您最近一年使用:0次
2020-06-06更新
|
339次组卷
|
3卷引用:北京市中央民族大学附属中学2021-2022学年高三上学期12月月考化学试题
名校
解题方法
8 . 实验小组探究 溶液与
溶液与 溶液的反应:
溶液的反应:
【资料】① 是强电解质,具有强氧化性。
是强电解质,具有强氧化性。 易被还原为
易被还原为 ;
;
② 可与
可与 发生反应:
发生反应:
③在溶液中 淀粉复合物必须有足够的浓度才能显示明显的蓝色
淀粉复合物必须有足够的浓度才能显示明显的蓝色
Ⅰ.实验小组设计了下列实验验证了 溶液与
溶液与 溶液的反应:
溶液的反应:
(1)实验1-1的目的是_______ 。
(2)请用离子方程式表示实验1-2中的化学反应_______ 。
Ⅱ.实验小组发现, 溶液中若含有
溶液中若含有 ,溶液并不会立刻变蓝,而会等待一段时间后再变蓝。为了解释这一现象,甲同学对此提出两种猜想:
,溶液并不会立刻变蓝,而会等待一段时间后再变蓝。为了解释这一现象,甲同学对此提出两种猜想:
猜想1:其他条件相同时, 与
与 反应速率_______
反应速率_______ 与
与 的反应速率,使溶液中
的反应速率,使溶液中 浓度降低,化学反应速率变慢。(填“
浓度降低,化学反应速率变慢。(填“ ”或“
”或“ ”)
”)
猜想2:其他条件相同时, 与
与 不反应。
不反应。 与
与 反应速率_______
反应速率_______ 与
与 的反应速率(填“
的反应速率(填“ ”或“
”或“ ”)。
”)。
(3)请补全猜想1:_______ 与猜想2:_______ 。
(4)根据资料2可知 的还原性
的还原性_______ (填“强于”或“弱于”) ,甲同学认为,该事实可以用来作为
,甲同学认为,该事实可以用来作为_______ (填“猜想1”或“猜想2”)的依据。
Ⅲ.为了进一步研究 的作用,小组同学分别向两支试管中依次加入下列试剂,并记录变他时间,如下表所示。
的作用,小组同学分别向两支试管中依次加入下列试剂,并记录变他时间,如下表所示。
(5)请补全表格中①_______ 与②_______
(6)乙同学根据现有数据证明Ⅱ中猜想1不成立,理由是_______ 。
Ⅳ.查阅文献表明Ⅱ中猜想2成立:
(7)下列说法正确的是_______(填字母)。
(8)结合实验2-2的数据,计算 内的
内的 消耗的速率
消耗的速率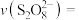
_______ 
 溶液与
溶液与 溶液的反应:
溶液的反应:【资料】①
 是强电解质,具有强氧化性。
是强电解质,具有强氧化性。 易被还原为
易被还原为 ;
;②
 可与
可与 发生反应:
发生反应:
③在溶液中
 淀粉复合物必须有足够的浓度才能显示明显的蓝色
淀粉复合物必须有足够的浓度才能显示明显的蓝色Ⅰ.实验小组设计了下列实验验证了
 溶液与
溶液与 溶液的反应:
溶液的反应:编号 | 1-1 | 1-2 |
实验操作 |
|
|
现象 | 无明显现象 | 溶液立即变蓝 |
(2)请用离子方程式表示实验1-2中的化学反应
Ⅱ.实验小组发现,
 溶液中若含有
溶液中若含有 ,溶液并不会立刻变蓝,而会等待一段时间后再变蓝。为了解释这一现象,甲同学对此提出两种猜想:
,溶液并不会立刻变蓝,而会等待一段时间后再变蓝。为了解释这一现象,甲同学对此提出两种猜想:猜想1:其他条件相同时,
 与
与 反应速率_______
反应速率_______ 与
与 的反应速率,使溶液中
的反应速率,使溶液中 浓度降低,化学反应速率变慢。(填“
浓度降低,化学反应速率变慢。(填“ ”或“
”或“ ”)
”)猜想2:其他条件相同时,
 与
与 不反应。
不反应。 与
与 反应速率_______
反应速率_______ 与
与 的反应速率(填“
的反应速率(填“ ”或“
”或“ ”)。
”)。(3)请补全猜想1:
(4)根据资料2可知
 的还原性
的还原性 ,甲同学认为,该事实可以用来作为
,甲同学认为,该事实可以用来作为Ⅲ.为了进一步研究
 的作用,小组同学分别向两支试管中依次加入下列试剂,并记录变他时间,如下表所示。
的作用,小组同学分别向两支试管中依次加入下列试剂,并记录变他时间,如下表所示。编号 |
|
| 淀粉 溶液 |
| ① | 变色时间 |
2-1 |
|
| 2滴 |
| ② | 立即 |
2-2 |
|
| 2滴 |
|
|
|
(6)乙同学根据现有数据证明Ⅱ中猜想1不成立,理由是
Ⅳ.查阅文献表明Ⅱ中猜想2成立:
(7)下列说法正确的是_______(填字母)。
A.增加溶液中 浓度, 浓度, 的初始反应速率会增加 的初始反应速率会增加 |
B.增加溶液中 浓度,溶液变蓝时间可能增加 浓度,溶液变蓝时间可能增加 |
C.增加溶液中 浓度,溶液可能无法变蓝 浓度,溶液可能无法变蓝 |
| D.升高溶液温度,溶液开始变蓝时间可能增加 |
 内的
内的 消耗的速率
消耗的速率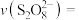

您最近一年使用:0次
名校
解题方法
9 . 某小组探究含 元素的化合物间的转化,进行如下实验。
元素的化合物间的转化,进行如下实验。
资料:
i.含 元素的常见粒子:
元素的常见粒子: (橙色)、
(橙色)、 (黄色)、
(黄色)、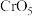 (溶于水,蓝紫色,不稳定)、
(溶于水,蓝紫色,不稳定)、 (绿色)、
(绿色)、 (蓝灰色,难溶于水,可溶于强酸、强碱)、
(蓝灰色,难溶于水,可溶于强酸、强碱)、 溶于强碱形成
溶于强碱形成 (亮绿色)。
(亮绿色)。
ii. 在碱性环境中比在酸性环境中分解速率快。
在碱性环境中比在酸性环境中分解速率快。
iii.在碱性环境中, 不能氧化
不能氧化 价格元素。
价格元素。
实验操作及现象如下:
(1)已知 (橙色)
(橙色) (黄色)
(黄色) 能说明该反应达平衡状态的是
能说明该反应达平衡状态的是_____ (填字母)。
A. 和
和 的浓度相同 B.
的浓度相同 B.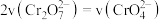 C.溶液的颜色不变
C.溶液的颜色不变
(2)已知 (橙色)
(橙色) (黄色)
(黄色) 。请用化学平衡移动原理解释Ⅰ中滴入稀硫酸后溶液橙色加深的原因:
。请用化学平衡移动原理解释Ⅰ中滴入稀硫酸后溶液橙色加深的原因:_____ 。
(3)Ⅰ中,溶液由橙色变为绿色的总反应的离子方程式是_____ 。
(4)Ⅱ中,继续滴入 溶液后,又有气泡生成的原因是
溶液后,又有气泡生成的原因是_____ 。
(5)Ⅱ中,继续滴入 溶液后,预测有
溶液后,预测有 沉淀生成,但实验时未观察到。提出假设:在碱性环境中,
沉淀生成,但实验时未观察到。提出假设:在碱性环境中, 价铬元素被
价铬元素被 氧化。
氧化。
①甲同学设计实验证明假设成立:
取少量Ⅰ中的绿色溶液,在滴入 溶液前增加一步操作:
溶液前增加一步操作:_____ 。然后滴入 溶液,有蓝灰色沉淀生成,继续滴入
溶液,有蓝灰色沉淀生成,继续滴入 溶液,沉淀溶解,溶液变为
溶液,沉淀溶解,溶液变为_____ 色。
②乙同学通过原电池原理进一步研究碱性环境对 价铬元素的还原性或
价铬元素的还原性或 的氧化性的彩响,经过实验研究得出以下结论:酸性条件下,
的氧化性的彩响,经过实验研究得出以下结论:酸性条件下,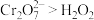 ;碱性条件下,
;碱性条件下,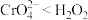
(6)此外,生产中常用 测定含
测定含 废水中
废水中 元素的含量。量取废水
元素的含量。量取废水 ,硫酸酸化后加入过量
,硫酸酸化后加入过量 溶液,发生反应:
溶液,发生反应: 。加入少量淀粉作为指示剂,用
。加入少量淀粉作为指示剂,用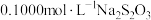 标准溶液滴定至终点,发生反应:
标准溶液滴定至终点,发生反应: 。平行滴定3次,平均消耗标准
。平行滴定3次,平均消耗标准 溶液
溶液 。则废水中
。则废水中 元素的含量为
元素的含量为_____  。
。
 元素的化合物间的转化,进行如下实验。
元素的化合物间的转化,进行如下实验。资料:
i.含
 元素的常见粒子:
元素的常见粒子: (橙色)、
(橙色)、 (黄色)、
(黄色)、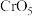 (溶于水,蓝紫色,不稳定)、
(溶于水,蓝紫色,不稳定)、 (绿色)、
(绿色)、 (蓝灰色,难溶于水,可溶于强酸、强碱)、
(蓝灰色,难溶于水,可溶于强酸、强碱)、 溶于强碱形成
溶于强碱形成 (亮绿色)。
(亮绿色)。ii.
 在碱性环境中比在酸性环境中分解速率快。
在碱性环境中比在酸性环境中分解速率快。iii.在碱性环境中,
 不能氧化
不能氧化 价格元素。
价格元素。实验操作及现象如下:
| 装置 | 步骤 | 操作 | 现象 |
2mL0.0125 K2Cr2O7溶液 | Ⅰ | 先滴入稀疏酸至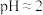 ,再滴入5滴 ,再滴入5滴 溶液,振荡 溶液,振荡 | 溶液橙色加深。滴入 溶液后迅速变为蓝紫色,有气泡生成。稍后,无明显气泡时,溶液由蓝紫色完全变为绿色 溶液后迅速变为蓝紫色,有气泡生成。稍后,无明显气泡时,溶液由蓝紫色完全变为绿色 |
| Ⅱ | 继续缓慢滴入10滴 溶液,边滴,边振荡 溶液,边滴,边振荡 | 又有气泡生成,溶液最终变为黄色 |
(1)已知
 (橙色)
(橙色) (黄色)
(黄色) 能说明该反应达平衡状态的是
能说明该反应达平衡状态的是A.
 和
和 的浓度相同 B.
的浓度相同 B.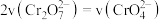 C.溶液的颜色不变
C.溶液的颜色不变(2)已知
 (橙色)
(橙色) (黄色)
(黄色) 。请用化学平衡移动原理解释Ⅰ中滴入稀硫酸后溶液橙色加深的原因:
。请用化学平衡移动原理解释Ⅰ中滴入稀硫酸后溶液橙色加深的原因:(3)Ⅰ中,溶液由橙色变为绿色的总反应的离子方程式是
(4)Ⅱ中,继续滴入
 溶液后,又有气泡生成的原因是
溶液后,又有气泡生成的原因是(5)Ⅱ中,继续滴入
 溶液后,预测有
溶液后,预测有 沉淀生成,但实验时未观察到。提出假设:在碱性环境中,
沉淀生成,但实验时未观察到。提出假设:在碱性环境中, 价铬元素被
价铬元素被 氧化。
氧化。①甲同学设计实验证明假设成立:
取少量Ⅰ中的绿色溶液,在滴入
 溶液前增加一步操作:
溶液前增加一步操作: 溶液,有蓝灰色沉淀生成,继续滴入
溶液,有蓝灰色沉淀生成,继续滴入 溶液,沉淀溶解,溶液变为
溶液,沉淀溶解,溶液变为②乙同学通过原电池原理进一步研究碱性环境对
 价铬元素的还原性或
价铬元素的还原性或 的氧化性的彩响,经过实验研究得出以下结论:酸性条件下,
的氧化性的彩响,经过实验研究得出以下结论:酸性条件下,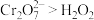 ;碱性条件下,
;碱性条件下,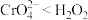
(6)此外,生产中常用
 测定含
测定含 废水中
废水中 元素的含量。量取废水
元素的含量。量取废水 ,硫酸酸化后加入过量
,硫酸酸化后加入过量 溶液,发生反应:
溶液,发生反应: 。加入少量淀粉作为指示剂,用
。加入少量淀粉作为指示剂,用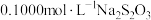 标准溶液滴定至终点,发生反应:
标准溶液滴定至终点,发生反应: 。平行滴定3次,平均消耗标准
。平行滴定3次,平均消耗标准 溶液
溶液 。则废水中
。则废水中 元素的含量为
元素的含量为 。
。
您最近一年使用:0次
名校
解题方法
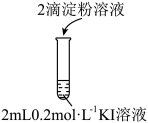
10 . 探究亚硝酸钠( NaNO2 )的化学性质,实验如下:
资料: AgNO2是淡黄色难溶于水的固体;由上述实验所得结论不正确的是
| 实验 | 装置 | 试剂a | 现象 |
| ① | 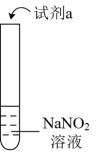 | 酚酞溶液 | 无色溶液变红 |
| ② | AgNO3溶液 | 产生淡黄色沉淀 | |
| ③ | 淀粉KI溶液+稀硫酸 | 无 色溶液立即变蓝 | |
| ④ | 酸性K2Cr2O7溶液 | 无色溶液变为绿色 |
| A.NaNO2溶液显碱性 |
B.NaNO2可与某些盐发生复分解反应: +Ag+= AgNO2↓ +Ag+= AgNO2↓ |
C.NaNO2有氧化性: 2I- +2H++2 =I2+2NO2 ↑+H2O =I2+2NO2 ↑+H2O |
D.NaNO2有还原性: +3 +3 +8H+=3 +8H+=3 +2Cr3++4H2O +2Cr3++4H2O |
您最近一年使用:0次
2022-05-25更新
|
329次组卷
|
6卷引用:北京市北京中国人民大学附属中学2022届高三10月检测化学试卷