解题方法
1 . 燃料电池的种类很多,氢氧燃料电池是目前最成熟的燃料电池,电解质可以是酸性的,也可以是碱性的。回答下列问题:
(1)氢氧燃料电池中,负极上通入的气体是______ ,电池总反应为______ 。
(2)若以稀硫酸作电解质溶液,电池工作时的负极反应为______ 。
(3)若以氢氧化钠溶液作电解质溶液,电池工作时的正极反应为______ 。
(1)氢氧燃料电池中,负极上通入的气体是
(2)若以稀硫酸作电解质溶液,电池工作时的负极反应为
(3)若以氢氧化钠溶液作电解质溶液,电池工作时的正极反应为
您最近一年使用:0次
2 . 海洋是个巨大的资源宝库,利用海水可以获得淡水、食盐、单质溴、单质镁等多种化学物质。结合有关过程回答下列问题:
(1)利用海水制备下列物质,不用通过化学反应过程就可以得到的是______。
(2)氯碱工业中电解饱和食盐水可以得到氢氧化钠、氯气和氢气,写出电解反应的化学方程式______ 。
(3)实验室中通常用浓盐酸和二氧化锰加热制备氯气,反应的化学方程式为______ 。用该种方法制备的氯气中含有杂质,为获得纯净干燥的氯气,可将气体依次通入盛有______ 和浓硫酸的洗气瓶中。
(4)海水中提取镁,先制备MgCl2再进一步获得单质镁,由MgCl2得到单质镁的化学方程式为______ 。
(1)利用海水制备下列物质,不用通过化学反应过程就可以得到的是______。
| A.氢氧化钠 | B.单质镁 | C.淡水 | D.单质溴 |
(3)实验室中通常用浓盐酸和二氧化锰加热制备氯气,反应的化学方程式为
(4)海水中提取镁,先制备MgCl2再进一步获得单质镁,由MgCl2得到单质镁的化学方程式为
您最近一年使用:0次
3 . 磷酸铁锂(LiFePO4)电极材料主要用于各种锂离子电池。回答下列问题。
(1)Fe 位于元素周期表中第_______ 周期第_______ 族,其价层电子排布式为_______ 。
(2)用“>”“<”或“=”填空:离子半径:Li+_______ H-;第一电离能:Li_______ Be;电负性:O_______ P。
(3)下列 Li 原子轨道表示式表示的状态中,能量最低和最高的分别为_______ 、_______ (填字母)。
A.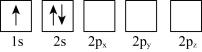 B.
B.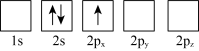
C. D.
D.
(4)基态 P 中未成对电子数为_______ ,其原子核外电子占据的最高能级的电子云轮廓图为_______ 形。
(1)Fe 位于元素周期表中第
(2)用“>”“<”或“=”填空:离子半径:Li+
(3)下列 Li 原子轨道表示式表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(4)基态 P 中未成对电子数为
您最近一年使用:0次
4 . 实验室欲用98%的浓硫酸(密度为1.84 g·cm-3)配制1.5 mol·L-1的稀硫酸90 mL。
(1)仪器的选择:配制溶液时,下列仪器不需要用到的是___________ (填字母)。
A.天平 B.100 mL容量瓶 C.玻璃棒
D.烧杯 E.量筒 F.250 mL容量瓶
还需要补充的仪器是___________ 。
(2)通过计算,用量筒量取浓硫酸的体积为___________ mL。
(3)稀释浓硫酸,冷却后移液,再进行定容、摇匀等一系列操作。从配制好的溶液中取出10 mL,加水稀释至100 mL,稀释后硫酸的物质的量浓度为___________ mol·L-1。
(1)仪器的选择:配制溶液时,下列仪器不需要用到的是
A.天平 B.100 mL容量瓶 C.玻璃棒
D.烧杯 E.量筒 F.250 mL容量瓶
还需要补充的仪器是
(2)通过计算,用量筒量取浓硫酸的体积为
(3)稀释浓硫酸,冷却后移液,再进行定容、摇匀等一系列操作。从配制好的溶液中取出10 mL,加水稀释至100 mL,稀释后硫酸的物质的量浓度为
您最近一年使用:0次
5 . 现有下列几种物质:
①Al2O3、②CuO、③NaHSO4、④FeCl3、⑤Cl2、⑥NaOH、⑦稀硫酸。回答下列问题:
(1)上述物质中属于碱性氧化物的是___________ (填序号,下同),属于两性氧化物的是___________ ,属于混合物的是___________ 。
(2)上述物质在水中能电离出三种离子的是___________ (填序号);写出④的电离方程式:___________ 。
(3)写出①与⑦反应的离子方程式:___________ 。
①Al2O3、②CuO、③NaHSO4、④FeCl3、⑤Cl2、⑥NaOH、⑦稀硫酸。回答下列问题:
(1)上述物质中属于碱性氧化物的是
(2)上述物质在水中能电离出三种离子的是
(3)写出①与⑦反应的离子方程式:
您最近一年使用:0次
6 . 四种短周期主族元素W、X、Y、Z的原子序数依次增大。W与Y同族,且Y的原子序数是W的2倍;X的原子核外电子层数是其最外层电子数的3倍。回答下列问题:
(1)W在周期表中的位置为___________ 。
(2)W、X、Y的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(3)W、X形成的两种化合物的化学式为___________ 。
(4)元素Y、Z中非金属性较强的是___________ (用元素符号表示),下列说法能说明这一事实的是___________ (填字母)。
a.常温时两种元素的单质状态不同
b.气态氢化物的稳定性:Z>Y
c.氧化物对应水化物的酸性:Z>Y
d.简单离子的还原性:Y>Z
(1)W在周期表中的位置为
(2)W、X、Y的简单离子半径由大到小的顺序为
(3)W、X形成的两种化合物的化学式为
(4)元素Y、Z中非金属性较强的是
a.常温时两种元素的单质状态不同
b.气态氢化物的稳定性:Z>Y
c.氧化物对应水化物的酸性:Z>Y
d.简单离子的还原性:Y>Z
您最近一年使用:0次
7 . 回答下列问题。
(1)Na、Fe、Cl、Al是中学化学常见的元素。
①含上述某一种元素的常见化合物中,呈淡黄色的是___________ (填化学式)。
②焰色试验中,Na元素燃烧时的焰色为___________ 色,观察K元素燃烧时的焰色需要透过___________ 。
③实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是___________ ,反应的化学方程式为___________ 。
(2)饮用水质量是关系人类健康的重要问题。
氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为___________ 。
(1)Na、Fe、Cl、Al是中学化学常见的元素。
①含上述某一种元素的常见化合物中,呈淡黄色的是
②焰色试验中,Na元素燃烧时的焰色为
③实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是
(2)饮用水质量是关系人类健康的重要问题。
氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为
您最近一年使用:0次
8 . 下列各组离子能在溶液中大量共存的是
| A.钠离子、二价铁离子、硝酸根离子、氢离子 | B.钠离子、氢离子、碳酸氢根离子、硝酸根 |
| C.钾离子、铵根离子、硫酸根离子、钡离子 | D.氢离子、铜离子、硝酸根、硫酸根 |
您最近一年使用:0次
9 . 电化学原理在电池制造、能量转换、物质合成等方面应用广泛。
(1)若用如图装置,依据反应Cu+2Fe3+=2Fe2++Cu2+设计原电池,则电极X应为___________ (填化学式),石墨电极的电极反应式为___________ 。将石墨换成铁电极后,电池总反应变为___________ 。

(2)燃料电池必须从电池外部源源不断地向电池提供天然气、甲烷、煤气等含氢化合物作为燃料。基于甲烷(CH4)-空气燃料电池,其工作原理如图,a、b均为惰性电极。a为___________ 极,正极的电极反应式为___________ 。当通入4.48L(标准状况下)甲烷气体时,测得电路中转移1.1mol电子,则甲烷的利用率为___________ 。(保留小数点后1位)。

(3)以如图所示装置模拟生产硫酸:

写出通入O2的电极的电极反应式___________ ,若此过程中转移了0.2mol电子,则质子膜两侧电解液的质量变化差(Δm左-Δm右)为___________ g(忽略气体的溶解)。
(4)一种可充电电池装置如图所示,充放电过程中,存在LiCoO2与Li1-xCoO2之间的转化。

①放电过程中Li+的移动方向___________ (填“A→B”或“B→A”);
②写出该电池放电时A极反应___________ ,充电时,阳极的电极反应式为___________ ;
③放电时,当电路中转移0.2NA电子时,A极质量减少___________ g。
(1)若用如图装置,依据反应Cu+2Fe3+=2Fe2++Cu2+设计原电池,则电极X应为

(2)燃料电池必须从电池外部源源不断地向电池提供天然气、甲烷、煤气等含氢化合物作为燃料。基于甲烷(CH4)-空气燃料电池,其工作原理如图,a、b均为惰性电极。a为

(3)以如图所示装置模拟生产硫酸:

写出通入O2的电极的电极反应式
(4)一种可充电电池装置如图所示,充放电过程中,存在LiCoO2与Li1-xCoO2之间的转化。

①放电过程中Li+的移动方向
②写出该电池放电时A极反应
③放电时,当电路中转移0.2NA电子时,A极质量减少
您最近一年使用:0次
10 . 微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以 NaCl 溶液模拟海水,采用惰性电极,用如图装置处理有机废水(以含 CH3COO-的溶液为例)。下列说法错误的是
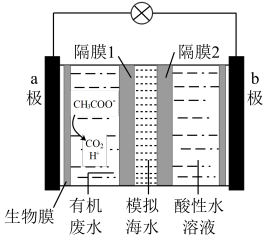

| A.负极反应为CH3COO-+2H2O-8e-=2CO2↑+7H+ |
| B.隔膜 1 为阳离子交换膜,隔膜 2 为阴离子交换膜 |
| C.当电路中转移 1 mol 电子时,模拟海水理论上除盐 58.5 g |
| D.电池工作一段时间后,正、负极产生气体的物质的量之比为 1∶2 |
您最近一年使用:0次



