名校
1 . 有下列物质:①胆矾②氨水③氯气④铜⑤氯化氢⑥蔗糖⑦液氨⑧ ⑨
⑨ ⑩
⑩
(1)属于电解质的是_______ (填序号,下同),
(2)能导电的是_______ 。
 ⑨
⑨ ⑩
⑩
(1)属于电解质的是
(2)能导电的是
您最近一年使用:0次
名校
2 . 在25℃时对氨水进行如下操作。回答下列问题:
(1)向0.1mol/L 20mL氨水中逐滴加入0.1mol/L VmL盐酸。
①若使氨水恰好被中和,则所得溶液的pH_______ 7(填“>”、“<”或“=”),用离子方程式表示其原因:_______ 。
②若所得溶液pH=7,则此时加入盐酸的体积V_______ 20mL(填“>”、“<”或“=”),溶液中 、
、 、
、 、
、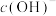 的大小关系为
的大小关系为_______ 。
③若加入盐酸的体积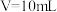 ,则此时溶液中
,则此时溶液中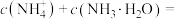
_______ mol/L。
(2)铜元素的价电子轨道表示式为_______ ,向 溶液中滴加氨水产生蓝色沉淀,若所得溶液
溶液中滴加氨水产生蓝色沉淀,若所得溶液 ,已知
,已知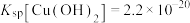 ,则溶液中
,则溶液中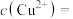
_______ mol/L。
(1)向0.1mol/L 20mL氨水中逐滴加入0.1mol/L VmL盐酸。
①若使氨水恰好被中和,则所得溶液的pH
②若所得溶液pH=7,则此时加入盐酸的体积V
 、
、 、
、 、
、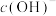 的大小关系为
的大小关系为③若加入盐酸的体积
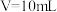 ,则此时溶液中
,则此时溶液中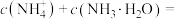
(2)铜元素的价电子轨道表示式为
 溶液中滴加氨水产生蓝色沉淀,若所得溶液
溶液中滴加氨水产生蓝色沉淀,若所得溶液 ,已知
,已知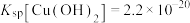 ,则溶液中
,则溶液中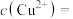
您最近一年使用:0次
名校
解题方法
3 . 按照要求回答下列问题:
(1)已知:①
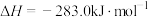
②
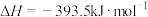
请写出C与 反应生成CO的热化学方程式:
反应生成CO的热化学方程式:_______ 。
(2)已知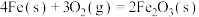
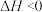 ,该反应的熵如何变化?
,该反应的熵如何变化?_______ (填“增大”、“减小”或“不变”),该反应在什么温度下可以自发进行?_______ (填“低温”、“高温”或“任何温度”)。
(3)盐碱地(含较多 、NaCl)不利于植物生长,盐碱地产生碱性的原因:
、NaCl)不利于植物生长,盐碱地产生碱性的原因:_______ (用离子方程式表示);农业上用石膏降低其碱性的反应原理:_______ (用化学方程式表示)。
(4)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m_______ n(填“>”、“<”或“=”)。
(1)已知:①

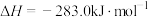
②

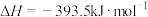
请写出C与
 反应生成CO的热化学方程式:
反应生成CO的热化学方程式:(2)已知
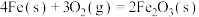
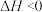 ,该反应的熵如何变化?
,该反应的熵如何变化?(3)盐碱地(含较多
 、NaCl)不利于植物生长,盐碱地产生碱性的原因:
、NaCl)不利于植物生长,盐碱地产生碱性的原因:(4)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题
(1)适量 在1mol
在1mol 中完全燃烧,生成2mol
中完全燃烧,生成2mol ,放出571.6kJ的热量。请写出表示
,放出571.6kJ的热量。请写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式______ 。
(2)电解稀的氢氧化钠溶液:阳极反应式为______ 。
(3)若向氨水中加入稀硫酸至溶液的 ,此时溶液中
,此时溶液中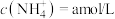 ,则
,则 =
=______ 。
(4)写出基态As原子的简化电子排布式和价层电子的轨道表示式:______ 。
(1)适量
 在1mol
在1mol 中完全燃烧,生成2mol
中完全燃烧,生成2mol ,放出571.6kJ的热量。请写出表示
,放出571.6kJ的热量。请写出表示 燃烧热的热化学方程式
燃烧热的热化学方程式(2)电解稀的氢氧化钠溶液:阳极反应式为
(3)若向氨水中加入稀硫酸至溶液的
 ,此时溶液中
,此时溶液中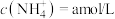 ,则
,则 =
=(4)写出基态As原子的简化电子排布式和价层电子的轨道表示式:
您最近一年使用:0次
名校
解题方法
5 . Ⅰ.化学来源于生活又服务于生活,请用化学用语回答下列问题:
(1)明矾 [ ]可用于净水。往明矾溶液中逐滴加
]可用于净水。往明矾溶液中逐滴加 溶液,若使
溶液,若使 恰好完全沉淀,发生反应的离子方程式为:
恰好完全沉淀,发生反应的离子方程式为:_______ ;若使 恰好完全沉淀,发生反应的离子方程式为:
恰好完全沉淀,发生反应的离子方程式为:_______ 。
(2)饮用水中的 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 。补充完整下列化学方程式,并在方程式上用单线桥标出该反应中电子转移的方向和数目:
。补充完整下列化学方程式,并在方程式上用单线桥标出该反应中电子转移的方向和数目:_________
_______Al+_______ _______NaOH=_______+_______
_______NaOH=_______+_______ _______
_______
Ⅱ.A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示。
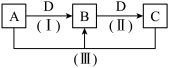
请回答下列问题。
(3)若A是一种黄绿色气体,可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质。写出实验室用 制备A的离子方程式:
制备A的离子方程式:_______ ;写出反应(Ⅲ)的离子方程式:_______ 。
(4)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一
①写出反应(Ⅲ)的离子方程式:_______ 。
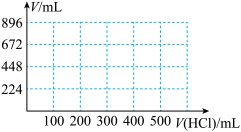
②取100mL B、C的混合溶液,其中B、C浓度均为0.1mol/L,向溶液中缓慢滴加0.1mol/L盐酸至过量,收集并测量产生气体的体积。刚开始滴加盐酸时,反应的离子方程式为_______ 。请将产生气体的体积(标准状况下且不考虑产生气体在水中的溶解)随滴加盐酸的体积变化的曲线绘制在下图坐标系中。______
(1)明矾 [
 ]可用于净水。往明矾溶液中逐滴加
]可用于净水。往明矾溶液中逐滴加 溶液,若使
溶液,若使 恰好完全沉淀,发生反应的离子方程式为:
恰好完全沉淀,发生反应的离子方程式为: 恰好完全沉淀,发生反应的离子方程式为:
恰好完全沉淀,发生反应的离子方程式为:(2)饮用水中的
 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 。补充完整下列化学方程式,并在方程式上用单线桥标出该反应中电子转移的方向和数目:
。补充完整下列化学方程式,并在方程式上用单线桥标出该反应中电子转移的方向和数目:_______Al+_______
 _______NaOH=_______+_______
_______NaOH=_______+_______ _______
_______
Ⅱ.A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示。

请回答下列问题。
(3)若A是一种黄绿色气体,可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质。写出实验室用
 制备A的离子方程式:
制备A的离子方程式:(4)若A、B、C的溶液均显碱性,C为焙制糕点的发酵粉的主要成分之一
①写出反应(Ⅲ)的离子方程式:
②取100mL B、C的混合溶液,其中B、C浓度均为0.1mol/L,向溶液中缓慢滴加0.1mol/L盐酸至过量,收集并测量产生气体的体积。刚开始滴加盐酸时,反应的离子方程式为

您最近一年使用:0次
名校
解题方法
6 . I.高铁酸钾 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比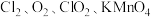 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。
至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为: ,该反应中
,该反应中 做
做_______ (填“氧化剂”、“还原剂”)。
(2)湿法制备高铁酸钾的反应体系中有六种微粒: 。
。
①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:_______ 。
②若反应过程中转移了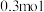 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为_______  。
。
II.将某铁铝合金均分为两份,一份加入足量盐酸,另一份加入足量 溶液,同温同压下产生的气体体积比为5∶4。
溶液,同温同压下产生的气体体积比为5∶4。
(3)样品中铁、铝物质的量之比为_______ 。
 是一种新型、高效、多功能绿色水处理剂,比
是一种新型、高效、多功能绿色水处理剂,比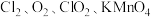 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入
氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入 至饱和,使高铁酸钾析出。
至饱和,使高铁酸钾析出。(1)干法制备高铁酸钠的主要反应为:
 ,该反应中
,该反应中 做
做(2)湿法制备高铁酸钾的反应体系中有六种微粒:
 。
。①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了
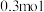 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为 。
。II.将某铁铝合金均分为两份,一份加入足量盐酸,另一份加入足量
 溶液,同温同压下产生的气体体积比为5∶4。
溶液,同温同压下产生的气体体积比为5∶4。(3)样品中铁、铝物质的量之比为
您最近一年使用:0次
名校
7 . 书写下列方程式:
(1)过量碳酸氢钠溶液与石灰水反应的化学方程式:_______
(2)氢氧化亚铁在空气中变质_______
(3)铝与氢氧化钠溶液反应的化学方程式_______
(4)铁与水蒸气反应_______
(5)氯气的实验室制法的化学方程式_______
(6)硫酸氢钠溶液与氢氧化钡溶液反应至硫酸根沉淀完全的化学方程式_______
(7)过氧化钠与水反应_______
(8)溴化亚铁溶液通入少量氯气的化学反应式_______
(1)过量碳酸氢钠溶液与石灰水反应的化学方程式:
(2)氢氧化亚铁在空气中变质
(3)铝与氢氧化钠溶液反应的化学方程式
(4)铁与水蒸气反应
(5)氯气的实验室制法的化学方程式
(6)硫酸氢钠溶液与氢氧化钡溶液反应至硫酸根沉淀完全的化学方程式
(7)过氧化钠与水反应
(8)溴化亚铁溶液通入少量氯气的化学反应式
您最近一年使用:0次
2023-01-05更新
|
316次组卷
|
2卷引用:天津市耀华中学2022-2023学年高一上学期期末考试化学试题
解题方法
8 . 根据所学电化学知识填空。
(1)如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。请回答下列问题:
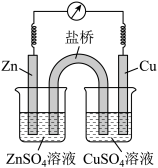
①Zn电极为电池的______ (填“正极”或“负极”)。
②写出电极反应式:Zn电极______ ,Cu电极______ 。
③盐桥中向CuSO4溶液中迁移的离子是______ (填离子符号)。
(2)金属腐蚀现象在生产生活中普遍存在,依据下列两种腐蚀现象回答下列问题:
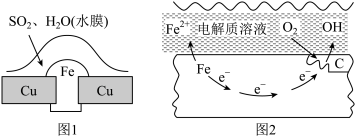
①图1中被腐蚀的金属为______ (填化学式);图2中金属腐蚀类型属于______ (填字母)。
A.化学腐蚀 B.析氢腐蚀 C.吸氧腐蚀
②图1中Cu的作用是______ (填“负极”或“正极”)。
③图2中铁的生锈过程中正极反应式为______ 。
(1)如图为锌铜原电池的装置示意图,其中盐桥内装有含饱和KCl溶液的琼胶。请回答下列问题:

①Zn电极为电池的
②写出电极反应式:Zn电极
③盐桥中向CuSO4溶液中迁移的离子是
(2)金属腐蚀现象在生产生活中普遍存在,依据下列两种腐蚀现象回答下列问题:

①图1中被腐蚀的金属为
A.化学腐蚀 B.析氢腐蚀 C.吸氧腐蚀
②图1中Cu的作用是
③图2中铁的生锈过程中正极反应式为
您最近一年使用:0次
9 . 根据原子核外电子排布规律,回答下列问题:
(1)写出基态S原子的核外电子排布式:______ 。
(2)画出基态N原子的轨道表示式:______ 。
(3)Fe3+比Fe2+的稳定性______ (填“强”或“弱”),从结构上分析原因是______ ;基态Fe2+与Fe3+离子中未成对的电子数之比为______ 。
(4)基态K原子中,核外电子占据最高能层的符号是______ ,占据该能层电子的电子云轮廓图形状为______ 。
(5)在周期表中,与Li的化学性质最相似的邻族元素是______ (填元素符号),该元素基态原子核外M层电子的自旋状态______ (填“相同”或“相反”)。
(6)在KHSO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是______ (填离子符号)。
(1)写出基态S原子的核外电子排布式:
(2)画出基态N原子的轨道表示式:
(3)Fe3+比Fe2+的稳定性
(4)基态K原子中,核外电子占据最高能层的符号是
(5)在周期表中,与Li的化学性质最相似的邻族元素是
(6)在KHSO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是
您最近一年使用:0次
解题方法
10 . 下表列出了①~⑥六种元素在周期表中的位置。
回答下列问题:(用化学用语填空)
(1)元素①的一种核素中,含有1个质子和1个中子,表示该核素组成的符号是_______ 。
(2)元素⑤的原子结构示意图是_______ 。
(3)上述元素中,原子半径最大的是_______ (填元素符号)。
(4)由元素①、⑥组成的化合物的电子式为_______ ,该化合物分子中含有_______ (填“极性”或“非极性”)共价键。
(5)元素⑤和⑥最高价氧化物对应的水化物酸性强的是_______ (填化学式)。
(6)金属性:③_______ ④(填“>”或“<”),它们的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(7)下列说法正确的是_______ (填序号)。
a.元素②、③组成的化合物只有一种
b.元素②的气态氢化物稳定性高于元素⑤的气态氢化物
c.元素⑥在化合物中呈现的最高化合价为+7价
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ |
(1)元素①的一种核素中,含有1个质子和1个中子,表示该核素组成的符号是
(2)元素⑤的原子结构示意图是
(3)上述元素中,原子半径最大的是
(4)由元素①、⑥组成的化合物的电子式为
(5)元素⑤和⑥最高价氧化物对应的水化物酸性强的是
(6)金属性:③
(7)下列说法正确的是
a.元素②、③组成的化合物只有一种
b.元素②的气态氢化物稳定性高于元素⑤的气态氢化物
c.元素⑥在化合物中呈现的最高化合价为+7价
您最近一年使用:0次



