1 . 铜是重要的工业原料,现有Cu、Cu2O组成的混合物,某研究性学习小组为了探究其组成情况,取35.2 g该混合物加入0.5 L 3.6mol/L的稀硝酸中,固体物质完全反应,溶液中铜元素均为Cu2+,且生成4.48 L(标准状况)的NO。向所得溶液中加入a L 2.0 mol/L的NaOH溶液,恰好使溶液中的Cu2+沉淀完全。
(1)Cu与稀硝酸反应的离子方程式为_______ ;
(2)a=_______ L;
(3)求混合物中Cu的质量分数_______ 。
(1)Cu与稀硝酸反应的离子方程式为
(2)a=
(3)求混合物中Cu的质量分数
您最近一年使用:0次
2 . 一定温度下,在10 L密闭容器中加入5 mol SO2和3 mol O2,发生反应:2SO2(g)+O2(g)⇌2SO3(g),10 min时,反应达到平衡状态,此时容器中还含有3 mol SO2。
(1)反应起始时, SO2的浓度为___ ,O2的浓度为___ ,反应生成了___ mol SO3,v(SO2)=___ 。
(2)平衡时SO3的浓度是__ ,SO2的转化率是___ 。
(3)平衡时容器内气体的总物质的量为__ mol。
(4)物质的浓度不再改变标志着该反应已达平衡,下列还可以说明该反应已达平衡的是______ (填序号)。
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2)
⑤n(SO3)∶n(O2)∶n(SO2)=2∶1∶2
(1)反应起始时, SO2的浓度为
(2)平衡时SO3的浓度是
(3)平衡时容器内气体的总物质的量为
(4)物质的浓度不再改变标志着该反应已达平衡,下列还可以说明该反应已达平衡的是
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2)
⑤n(SO3)∶n(O2)∶n(SO2)=2∶1∶2
您最近一年使用:0次
名校
3 . 已知:25℃时,CH3COOH和NH3•H2O的电离常数相等。
(1)25°C时,取10 mL0.1 mol•L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1000 mL,溶液pH数值范围为____ ,溶液中
____ (填“增大”“减小”“不变”或“不能确定”)。
②25℃时,0.1 mol•L-1氨水(NH3•H2O溶液)的pH=___ 。
③25℃时,氨水电离平衡常数约为___ 。
(2)25℃时,现向10 mL0.1 mol•L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中
___ (填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1 mL0.1 mol•L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=-lgc(OH-)。
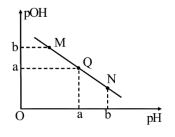
图中M、Q、N三点所示溶液呈中性的点是____ (填字母)。若Q点滴加的醋酸溶液的体积为V2 mL,则V1____ V2(填=,>或<)。
(1)25°C时,取10 mL0.1 mol•L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1000 mL,溶液pH数值范围为

②25℃时,0.1 mol•L-1氨水(NH3•H2O溶液)的pH=
③25℃时,氨水电离平衡常数约为
(2)25℃时,现向10 mL0.1 mol•L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中

a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1 mL0.1 mol•L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=-lgc(OH-)。

图中M、Q、N三点所示溶液呈中性的点是
您最近一年使用:0次
名校
解题方法
4 . (1)9.03×1024个H2O分子的物质的量为___________ ,在标准状况下4.48 LSO2的质量为___________ 。
(2)在标准状况下,22.4L由氮气和氧气组成的混合气体,其质量为30g,则其中氧气的质量为___________ g。
(3)某金属氯化物MClx的摩尔质量为133.5g/mol,取该金属氯化物26.7g配成水溶液,与足量AgNO3溶液完全反应,生成86.1g白色沉淀。则金属M的摩尔质量___________ 。
(4) 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是___________ 。
(2)在标准状况下,22.4L由氮气和氧气组成的混合气体,其质量为30g,则其中氧气的质量为
(3)某金属氯化物MClx的摩尔质量为133.5g/mol,取该金属氯化物26.7g配成水溶液,与足量AgNO3溶液完全反应,生成86.1g白色沉淀。则金属M的摩尔质量
(4)
 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
您最近一年使用:0次
名校
解题方法
5 . 0.6mol O2与0.4mol O3的质量之比为______ ,分子个数之比为_______ ,O原子的物质的量之比为_____
您最近一年使用:0次
2020-11-01更新
|
89次组卷
|
2卷引用:吉林省吉林市第五十五中学2020-2021学年高一上学期期中考试化学试题
6 . 配制0.2mol/LNa2SO4溶液50mL,需要称取固体Na2SO4的质量是多少?
您最近一年使用:0次
2020-10-25更新
|
148次组卷
|
3卷引用:2015-2016学年吉林省吉林五十五中高一上学期期中测试化学试卷
7 . 已知Cu(OH)2的Ksp=2×10-20:某溶液中c(Cu2+)=0.02 mol·L-1,如要生成Cu(OH)2沉淀,应调整溶液的pH大于________ ?(写步骤)
您最近一年使用:0次
2020-01-13更新
|
153次组卷
|
3卷引用:吉林省吉林市第五十五中学2019-2020学年高二上学期期末考试化学试题
8 . 汽车尾气中CO、 以及燃煤废气中的
以及燃煤废气中的 都是大气污染物,对它们的治理具有重要意义。
都是大气污染物,对它们的治理具有重要意义。
 氧化还原法消除
氧化还原法消除 的转化如下所示:
的转化如下所示: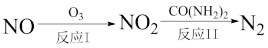
 反应Ⅰ为
反应Ⅰ为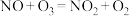 ,生成标准状况下
,生成标准状况下 L
L  时,转移电子的物质的量是
时,转移电子的物质的量是______
mol。
 反应Ⅱ中,当
反应Ⅱ中,当 :
: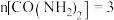 :2时,氧化产物与还原产物的质量比为
:2时,氧化产物与还原产物的质量比为______ 。
 使用“催化转化器”可以减少尾气中的CO和
使用“催化转化器”可以减少尾气中的CO和 ,转化过程中发生反应的化学方程式为
,转化过程中发生反应的化学方程式为 未配平
未配平 ,若
,若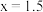 ,则方程式中
,则方程式中 和
和 的化学计量数之比为
的化学计量数之比为______ 。
 吸收
吸收 和NO,获得
和NO,获得 和
和 产品的流程图如图所示
产品的流程图如图所示 为铈元素
为铈元素 。
。

装置Ⅱ中,酸性条件下NO被 氧化的产物主要是
氧化的产物主要是 和
和 ,请写出生成等物质的量的
,请写出生成等物质的量的 和
和 时的离子方程式:
时的离子方程式:______ 。
 已知进入装置Ⅳ的溶液中
已知进入装置Ⅳ的溶液中 的浓度为a
的浓度为a  ,要使1
,要使1  该溶液中的
该溶液中的 完全转化为
完全转化为 ,至少需向装置Ⅳ中通入标准状况下的氧气
,至少需向装置Ⅳ中通入标准状况下的氧气______ 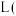 用含a代数式表示,结果保留整数
用含a代数式表示,结果保留整数 。
。
 以及燃煤废气中的
以及燃煤废气中的 都是大气污染物,对它们的治理具有重要意义。
都是大气污染物,对它们的治理具有重要意义。 氧化还原法消除
氧化还原法消除 的转化如下所示:
的转化如下所示: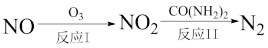
 反应Ⅰ为
反应Ⅰ为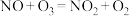 ,生成标准状况下
,生成标准状况下 L
L  时,转移电子的物质的量是
时,转移电子的物质的量是mol。
 反应Ⅱ中,当
反应Ⅱ中,当 :
: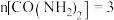 :2时,氧化产物与还原产物的质量比为
:2时,氧化产物与还原产物的质量比为 使用“催化转化器”可以减少尾气中的CO和
使用“催化转化器”可以减少尾气中的CO和 ,转化过程中发生反应的化学方程式为
,转化过程中发生反应的化学方程式为 未配平
未配平 ,若
,若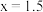 ,则方程式中
,则方程式中 和
和 的化学计量数之比为
的化学计量数之比为 吸收
吸收 和NO,获得
和NO,获得 和
和 产品的流程图如图所示
产品的流程图如图所示 为铈元素
为铈元素 。
。
装置Ⅱ中,酸性条件下NO被
 氧化的产物主要是
氧化的产物主要是 和
和 ,请写出生成等物质的量的
,请写出生成等物质的量的 和
和 时的离子方程式:
时的离子方程式: 已知进入装置Ⅳ的溶液中
已知进入装置Ⅳ的溶液中 的浓度为a
的浓度为a  ,要使1
,要使1  该溶液中的
该溶液中的 完全转化为
完全转化为 ,至少需向装置Ⅳ中通入标准状况下的氧气
,至少需向装置Ⅳ中通入标准状况下的氧气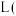 用含a代数式表示,结果保留整数
用含a代数式表示,结果保留整数 。
。
您最近一年使用:0次
2019-12-26更新
|
160次组卷
|
8卷引用:吉林省吉林市2019-2020学年高二下学期期末教学质量检测化学试题
9 . 某温度下,纯水中c(H+) = 2.0×10-7 mol / L,则此溶液的c(OH-)=__________ mol / L;水的离子积常数Kw=_______________ ,此温度________ 25℃(填“大于”、“小于”或“等于”)
您最近一年使用:0次
10 . 6.4gO2的物质的量是多少?___ 含有多少个氧气分子?___ 在标准状况下的体积是多少?___
您最近一年使用:0次



