1 . 反应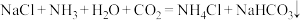 可用于联合制碱。下列说法正确的是
可用于联合制碱。下列说法正确的是
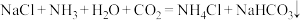 可用于联合制碱。下列说法正确的是
可用于联合制碱。下列说法正确的是A.氯离子的结构示意图: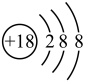 |
| B.反应说明在该温度下碳酸氢钠溶解度较小 |
C. 的电离方程式: 的电离方程式: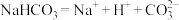 |
D.NaCl和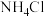 均为离子化合物,他们所含的化学键类型相同 均为离子化合物,他们所含的化学键类型相同 |
您最近一年使用:0次
2 . 由水电离出 的溶液中,一定能大量共存的离子组是
的溶液中,一定能大量共存的离子组是
 的溶液中,一定能大量共存的离子组是
的溶液中,一定能大量共存的离子组是A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
3 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.7.1g  与足量铁粉反应转移的电子数为0.2 与足量铁粉反应转移的电子数为0.2 |
B.1molL-1  溶液中含离子总数为3 溶液中含离子总数为3 |
C.标准状况下,2.24L  分子中含有的σ键的数目为0.4 分子中含有的σ键的数目为0.4 |
D.44g  中 中 杂化的碳原子数目为2 杂化的碳原子数目为2 |
您最近一年使用:0次
4 . 下列化学用语表示正确的是
A.中子数为32的铁原子: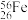 |
B. 中的 中的 夹角为109°28′ 夹角为109°28′ |
C. 的电子式为 的电子式为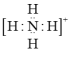 ,离子呈平面正方形结构 ,离子呈平面正方形结构 |
D.金刚石与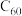 互为同素异形体 互为同素异形体 |
您最近一年使用:0次
5 . 下列过程中,不涉及氧化还原反应的是
A.利用“杯酚”分离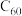 和 和 | B.黄铁矿制硫酸 |
| C.海水提溴 | D.利用铝热反应冶炼铁、铬、锰等金属 |
您最近一年使用:0次
6 . 下列说法正确的是
| A.尼龙是天然纤维 |
| B.食品添加剂应禁止使用,实现零添加 |
| C.电影放映机到银幕间产生光柱是因为丁达尔效应 |
| D.铅笔芯的原料是重金属铅,不可用嘴吮咬铅笔,以免引起铅中毒 |
您最近一年使用:0次
解题方法
7 . 下列离子方程式与所给事实不相符的是
A. 通入氢氧化钠溶液: 通入氢氧化钠溶液: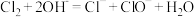 |
B.盐酸去除水垢中的 : :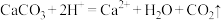 |
C.利用覆铜板制作印刷电路板: |
D.用两个铜电极电解 溶液: 溶液: |
您最近一年使用:0次
8 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,图2装置探究其相关性质。
(1)图1装置中生成 的化学方程式为
的化学方程式为________________ ,
(2)检验圆底烧瓶中已收集满氨气的方法是________________ 。
Ⅱ、探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物
(3)无水硫酸铜的作用是________ ,有同学认为需要在无水硫酸铜的后面再接一个装有无水 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是________________ 。
(4)实验中观察到a中 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为________________ 。
(5)若向a中通入标准状况下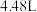 的氨气,最终得到铜的质量为
的氨气,最终得到铜的质量为________ g。
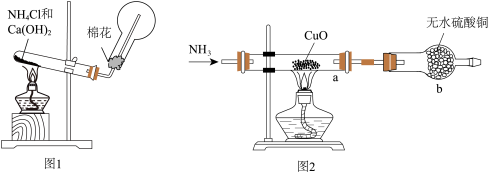
(1)图1装置中生成
 的化学方程式为
的化学方程式为(2)检验圆底烧瓶中已收集满氨气的方法是
Ⅱ、探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物
(3)无水硫酸铜的作用是
 固体的球形干燥管,这样做的目的是
固体的球形干燥管,这样做的目的是(4)实验中观察到a中
 粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
粉末变红,b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为(5)若向a中通入标准状况下
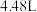 的氨气,最终得到铜的质量为
的氨气,最终得到铜的质量为
您最近一年使用:0次
2024-05-04更新
|
136次组卷
|
2卷引用:天津市第二十一中学2023-2024学年高一下学期第一次月考化学试卷
2024·陕西西安·二模
9 . 二氧化钒( )是一种新型热敏材料,+4价的钒化合物在弱酸性条件下易被氧化,实验室以
)是一种新型热敏材料,+4价的钒化合物在弱酸性条件下易被氧化,实验室以 为原料合成用于制备
为原料合成用于制备 的氧钒(
的氧钒( )碱式碳酸铵晶体。过程如下:
)碱式碳酸铵晶体。过程如下:
(1)步骤i中生成 的同时还产生一种无色无污染的气体,所发生反应的化学方程式为
的同时还产生一种无色无污染的气体,所发生反应的化学方程式为___________ 。只用浓盐酸与 反应也能制备
反应也能制备 溶液,从安全与环保角度分析,该反应不被推广的主要原因是
溶液,从安全与环保角度分析,该反应不被推广的主要原因是___________ 。
(2)步骤ii可用如图仪器组装完成。___________ (用各接口字母表示)。
②B装置的作用是___________ 。
③反应结束后,将三颈烧瓶置于干燥器中一段时间,可得到紫红色晶体,然后抽滤洗涤,先用饱和 溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。用饱和
溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。用饱和 溶液洗涤除去的阴离子主要是
溶液洗涤除去的阴离子主要是___________ ,用无水乙醇洗涤的目的是___________ 。
(3)测定氧钒( )碱式碳酸铵晶体粗产品中钒的含量。
)碱式碳酸铵晶体粗产品中钒的含量。
称量a g样品于锥形瓶中,用20mL蒸馏水与30mL混酸溶解后,加0.02mol/L 溶液至稍过量,充分反应后继续加1%
溶液至稍过量,充分反应后继续加1%  溶液至稍过量。再用尿素除去过量的
溶液至稍过量。再用尿素除去过量的 ,滴入几滴铁氰化钾{
,滴入几滴铁氰化钾{ }溶液,最后用c mol/L
}溶液,最后用c mol/L  标准溶液滴定至终点,消耗体积为b mL。滴定反应为:
标准溶液滴定至终点,消耗体积为b mL。滴定反应为: 。
。
① 溶液的作用是
溶液的作用是___________ 。
②粗产品中钒的质量分数的表达式为___________ 。
 )是一种新型热敏材料,+4价的钒化合物在弱酸性条件下易被氧化,实验室以
)是一种新型热敏材料,+4价的钒化合物在弱酸性条件下易被氧化,实验室以 为原料合成用于制备
为原料合成用于制备 的氧钒(
的氧钒( )碱式碳酸铵晶体。过程如下:
)碱式碳酸铵晶体。过程如下:
(1)步骤i中生成
 的同时还产生一种无色无污染的气体,所发生反应的化学方程式为
的同时还产生一种无色无污染的气体,所发生反应的化学方程式为 反应也能制备
反应也能制备 溶液,从安全与环保角度分析,该反应不被推广的主要原因是
溶液,从安全与环保角度分析,该反应不被推广的主要原因是(2)步骤ii可用如图仪器组装完成。
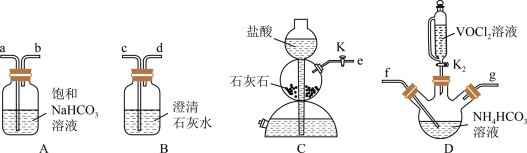
②B装置的作用是
③反应结束后,将三颈烧瓶置于干燥器中一段时间,可得到紫红色晶体,然后抽滤洗涤,先用饱和
 溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。用饱和
溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。用饱和 溶液洗涤除去的阴离子主要是
溶液洗涤除去的阴离子主要是(3)测定氧钒(
 )碱式碳酸铵晶体粗产品中钒的含量。
)碱式碳酸铵晶体粗产品中钒的含量。称量a g样品于锥形瓶中,用20mL蒸馏水与30mL混酸溶解后,加0.02mol/L
 溶液至稍过量,充分反应后继续加1%
溶液至稍过量,充分反应后继续加1%  溶液至稍过量。再用尿素除去过量的
溶液至稍过量。再用尿素除去过量的 ,滴入几滴铁氰化钾{
,滴入几滴铁氰化钾{ }溶液,最后用c mol/L
}溶液,最后用c mol/L  标准溶液滴定至终点,消耗体积为b mL。滴定反应为:
标准溶液滴定至终点,消耗体积为b mL。滴定反应为: 。
。①
 溶液的作用是
溶液的作用是②粗产品中钒的质量分数的表达式为
您最近一年使用:0次
名校
解题方法
10 . 以下反应的离子方程式书写不正确的是
A.将铁粉加入过量的稀硝酸中: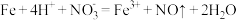 |
B.次氯酸钠溶液吸收少量二氧化硫: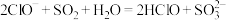 |
C. 与过量NaOH溶液加热: 与过量NaOH溶液加热: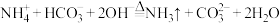 |
D.氨水吸收过量二氧化硫: |
您最近一年使用:0次



