1 . 配位化合物广泛应用于物质分离、定量测定、医药、催化等方面。利用氧化法可制备某些配位化合物,如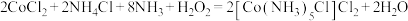 。设
。设 是阿伏加德罗常数的值,下列叙述正确的是
是阿伏加德罗常数的值,下列叙述正确的是
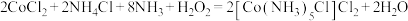 。设
。设 是阿伏加德罗常数的值,下列叙述正确的是
是阿伏加德罗常数的值,下列叙述正确的是A. 中含有 中含有 键的数目为 键的数目为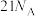 |
B. 和 和 的VSEPR模型完全相同 的VSEPR模型完全相同 |
C. 与足量 与足量 在催化剂作用下合成氨,生成的 在催化剂作用下合成氨,生成的 分子数为 分子数为 |
D. 质量分数为 质量分数为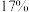 的 的 溶液中,氧原子总数为 溶液中,氧原子总数为 |
您最近一年使用:0次
解题方法
2 .  为紫色固体,易溶于水,微溶于
为紫色固体,易溶于水,微溶于 溶液,不溶于乙醇;有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生
溶液,不溶于乙醇;有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生 。
。
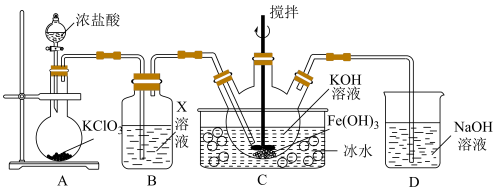
(1)A中发生反应的离子反应方程式是__________ 。
(2)下列试剂中,装置B的X溶液可以选用的是__________(填标号)。
(3)C中得到紫色固体和溶液,生成 的化学方程式是
的化学方程式是__________ ;若要从反应后的装置C中尽可能得到更多的 固体,可以采取的一种措施是
固体,可以采取的一种措施是__________ 。
(4)高铁酸钾与水反应的离子方程式是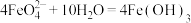 (胶体)
(胶体) ,则其作为水处理剂的原理是
,则其作为水处理剂的原理是__________ 、__________ 。
(5)某同学设计如图装置制备一定量的 ,并使其能在较长时间内存在。
,并使其能在较长时间内存在。
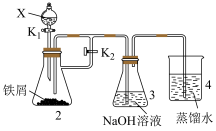
X不能是硝酸,原因是__________ ,装置4的作用是__________ 。
 为紫色固体,易溶于水,微溶于
为紫色固体,易溶于水,微溶于 溶液,不溶于乙醇;有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生
溶液,不溶于乙醇;有强氧化性,在0℃~5℃的强碱性溶液中较稳定,在酸性或中性溶液中快速产生 。
。
(1)A中发生反应的离子反应方程式是
(2)下列试剂中,装置B的X溶液可以选用的是__________(填标号)。
| A.饱和食盐水 | B.浓盐酸 | C.饱和氯水 | D. 溶液 溶液 |
(3)C中得到紫色固体和溶液,生成
 的化学方程式是
的化学方程式是 固体,可以采取的一种措施是
固体,可以采取的一种措施是(4)高铁酸钾与水反应的离子方程式是
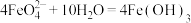 (胶体)
(胶体) ,则其作为水处理剂的原理是
,则其作为水处理剂的原理是(5)某同学设计如图装置制备一定量的
 ,并使其能在较长时间内存在。
,并使其能在较长时间内存在。
X不能是硝酸,原因是
您最近一年使用:0次
解题方法
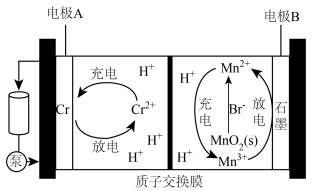
3 . 中科院大连化物所储能技术研究部提出了一种基于 辅助
辅助 放电的混合型液流电池,装置如图所示,下列说法错误的是
放电的混合型液流电池,装置如图所示,下列说法错误的是
 辅助
辅助 放电的混合型液流电池,装置如图所示,下列说法错误的是
放电的混合型液流电池,装置如图所示,下列说法错误的是
A.充电时, 向电极A迁移 向电极A迁移 |
B.在放电过程中,可利用 及时清除电极B上的“死锰” 及时清除电极B上的“死锰”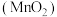 ,提高充放电过程的可逆性 ,提高充放电过程的可逆性 |
C.放电时,电极B上还可能发生: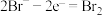 |
D.放电时,在该环境下的氧化性: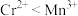 |
您最近一年使用:0次
解题方法
4 . 下列反应的离子方程式正确的是
A.向酸性高锰酸钾溶液加入草酸: |
B.下水道堵塞用铝粉和烧碱溶液疏通: |
C. 与足量 与足量 溶液共热: 溶液共热: |
D. 溶液中通入过量 溶液中通入过量 : :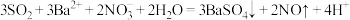 |
您最近一年使用:0次
5 .  为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.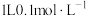 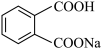 溶液中, 溶液中,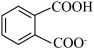 和 和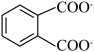 的离子数目之和少于 的离子数目之和少于 |
B.向 溶液中通入适量 溶液中通入适量 ,当有 ,当有 被氧化时,转移电子总数一定等于 被氧化时,转移电子总数一定等于 |
C.电解精炼铜时,以待精炼铜作阳极,以纯铜作阴极,当阳极有 转化为 转化为 时,电路中通过的电子数为 时,电路中通过的电子数为 |
D.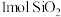 中Si—O键的数目为 中Si—O键的数目为 |
您最近一年使用:0次
解题方法
6 . 化学与社会、生活、科技息息相关,下列说法不正确的是
| A.“青蒿一握,以水二升渍,绞取汁”是提取青蒿素的过程,属于化学变化 |
| B.“熬胆矾铁釜,久之亦化为铜”,该过程发生了氧化还原反应 |
| C.“天问一号”火星车使用的保温材料——纳米气凝胶,具有丁达尔效应 |
| D.我国承诺在2060年前实现“碳中和”,这里的碳是指二氧化碳 |
您最近一年使用:0次
解题方法
7 . 下列离子方程式错误的是
A.饱和碳酸钠溶液中通入足量 : : |
B.硫化钠溶液与稀硝酸混合: |
C.用铁氰化钾溶液检验 : :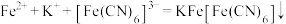 |
D.将少量 通入 通入 溶液中: 溶液中: |
您最近一年使用:0次
2024-03-22更新
|
416次组卷
|
2卷引用:江西省新余市2024届高三下学期第二次模拟考试化学试题
名校
解题方法
8 . 化学实验是研究物质组成和探究物质性质的重要途径。
I.某澄清透明溶液(忽略水的电离),可能含有 、
、 、
、 、
、 、
、 、
、 、
、 等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
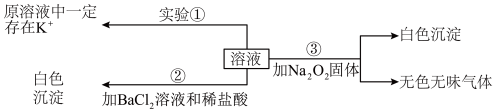
(1)取100mL溶液进行实验②,经足量盐酸洗涤、干燥后,得沉淀质量为2.33g。该溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(2)实验③产生的无色无味气体为_______ ,白色沉淀为_______ (填物质化学式)。原溶液中一定存在的离子有_______ 。
(3)向该溶液中加入硫酸酸化,再通入 气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式
气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式_______ 。
II. 具有强氧化性,
具有强氧化性, 具有还原性,某同学根据氧化还原反应的知识推测,
具有还原性,某同学根据氧化还原反应的知识推测, 与
与 能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A用锌和稀盐酸制取氢气。
能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A用锌和稀盐酸制取氢气。
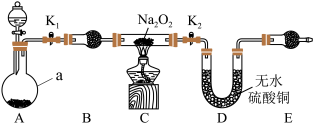
(4)下面是实验过程中的重要操作,正确的顺序是_______。
(5)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出 与
与 反应生成的产物为
反应生成的产物为_______ 。
I.某澄清透明溶液(忽略水的电离),可能含有
 、
、 、
、 、
、 、
、 、
、 、
、 等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
等离子中的几种,且离子的物质的量相等(即离子数目相等),为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如图所示。请你根据上述实验推断:
(1)取100mL溶液进行实验②,经足量盐酸洗涤、干燥后,得沉淀质量为2.33g。该溶液中
 的物质的量浓度为
的物质的量浓度为(2)实验③产生的无色无味气体为
(3)向该溶液中加入硫酸酸化,再通入
 气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式
气体,发生反应使该溶液的颜色发生变化,写出该反应的离子方程式II.
 具有强氧化性,
具有强氧化性, 具有还原性,某同学根据氧化还原反应的知识推测,
具有还原性,某同学根据氧化还原反应的知识推测, 与
与 能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A用锌和稀盐酸制取氢气。
能发生反应。为了验证此推测结果,该同学设计并进行了如图所示实验。其中装置A用锌和稀盐酸制取氢气。
(4)下面是实验过程中的重要操作,正确的顺序是_______。
A.加热至 逐渐熔化,反应一段时间 逐渐熔化,反应一段时间 | B.用小试管收集气体并检验其纯度 |
C.打开 、 、 ,通入氢气 ,通入氢气 | D.停止加热,充分冷却,关闭 、 、 |
(5)实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出
 与
与 反应生成的产物为
反应生成的产物为
您最近一年使用:0次
名校
9 . 铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
氯化铁:熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
氯化亚铁:熔点为670℃,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用如图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:
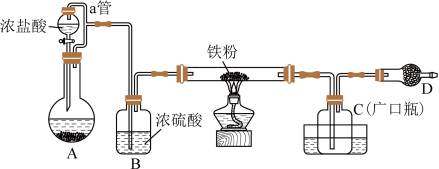
(1)装置A中,用 与浓盐酸反应制取氯气,写出反应的离子方程式:
与浓盐酸反应制取氯气,写出反应的离子方程式:_______ 。
(2)装置A中导管a的作用是______ 。C放置在盛冷水的水槽中,冷水浴的作用是_______ 。
(3)仪器D中装的药品可以是_______(填序号)。
(4)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。若产物中混有 ,是否可用酸性
,是否可用酸性 溶液检验
溶液检验 的存在?
的存在?_______ 。(填“是”或“否”);理由是_______ 。
(5)取装置C中的产物,按以下步骤进行测定:①称取4.60g产品溶于过量的稀盐酸中;②加入足量 溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。写出加入足量
溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。写出加入足量 溶液发生反应的离子方程式:
溶液发生反应的离子方程式:_______ 。
氯化铁:熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
氯化亚铁:熔点为670℃,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用如图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:

(1)装置A中,用
 与浓盐酸反应制取氯气,写出反应的离子方程式:
与浓盐酸反应制取氯气,写出反应的离子方程式:(2)装置A中导管a的作用是
(3)仪器D中装的药品可以是_______(填序号)。
A. | B.碱石灰 | C. | D.浓硫酸 |
(4)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。若产物中混有
 ,是否可用酸性
,是否可用酸性 溶液检验
溶液检验 的存在?
的存在?(5)取装置C中的产物,按以下步骤进行测定:①称取4.60g产品溶于过量的稀盐酸中;②加入足量
 溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。写出加入足量
溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。写出加入足量 溶液发生反应的离子方程式:
溶液发生反应的离子方程式:
您最近一年使用:0次
名校
解题方法
10 .  常作为漂白布匹后的“脱氯剂”,
常作为漂白布匹后的“脱氯剂”, 和
和 反应的产物之一为
反应的产物之一为 ,下列说法错误的是
,下列说法错误的是
 常作为漂白布匹后的“脱氯剂”,
常作为漂白布匹后的“脱氯剂”, 和
和 反应的产物之一为
反应的产物之一为 ,下列说法错误的是
,下列说法错误的是A.该反应中还原剂是 | B. 参与该反应,且作氧化剂 参与该反应,且作氧化剂 |
C.根据该反应可判断氧化性: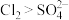 | D.该反应中每消耗1mol ,可脱去4mol ,可脱去4mol |
您最近一年使用:0次



