名校
解题方法
1 . 磷及其化合物在工农业生产中具有重要用途。回答下列问题:
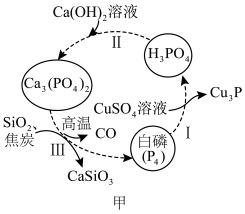
(1)如图甲所示为提纯白磷样品(含惰性杂质)的工艺流程。过程I中,氧化产物与还原产物的物质的量之比为___________ ,过程Ⅲ的化学方程式为___________ 。
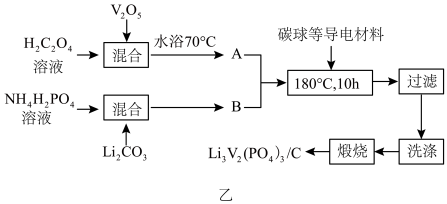
(2)磷酸钒锂/碳复合材料[Li3V2(PO4)3/C]具有能量密度高,循环寿命长,稳定安全等优点,是一种十分具有商业潜力的电极材料,我国科学家研发的一种制备流程如图乙所示:
①向复合材料中加入碳单质的作用是___________ 。
②A的主要成分为V2(C2O4)3,合成A反应的化学方程式为___________ 。
③已知常温下,Li2CO3微溶于水,LiHCO3可溶于水。工业级Li2CO3中含有少量难溶于水且与CO2不反应的杂质。补全下列实验方案:将工业级Li2CO3与水混合,___________ ,得到LiHCO3溶液,控温加热使LiHCO3分解形成Li2CO3沉淀,过滤、洗涤、干燥得到Li2CO3纯品。
④锂离子电池是一种二次电池。若用 和Li3V2(PO4)3/C作电极,放电时的电池总反应为
和Li3V2(PO4)3/C作电极,放电时的电池总反应为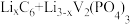 =Li3V2(PO4)3+C6,则电池放电时正极的电极反应式为
=Li3V2(PO4)3+C6,则电池放电时正极的电极反应式为___________ 。
(1)如图甲所示为提纯白磷样品(含惰性杂质)的工艺流程。过程I中,氧化产物与还原产物的物质的量之比为

(2)磷酸钒锂/碳复合材料[Li3V2(PO4)3/C]具有能量密度高,循环寿命长,稳定安全等优点,是一种十分具有商业潜力的电极材料,我国科学家研发的一种制备流程如图乙所示:

①向复合材料中加入碳单质的作用是
②A的主要成分为V2(C2O4)3,合成A反应的化学方程式为
③已知常温下,Li2CO3微溶于水,LiHCO3可溶于水。工业级Li2CO3中含有少量难溶于水且与CO2不反应的杂质。补全下列实验方案:将工业级Li2CO3与水混合,
④锂离子电池是一种二次电池。若用
 和Li3V2(PO4)3/C作电极,放电时的电池总反应为
和Li3V2(PO4)3/C作电极,放电时的电池总反应为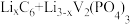 =Li3V2(PO4)3+C6,则电池放电时正极的电极反应式为
=Li3V2(PO4)3+C6,则电池放电时正极的电极反应式为
您最近一年使用:0次
2022-02-22更新
|
826次组卷
|
6卷引用:押江苏卷第15题 化学工业流程综合题 -备战2022年高考化学临考题号押题(江苏卷)
(已下线)押江苏卷第15题 化学工业流程综合题 -备战2022年高考化学临考题号押题(江苏卷)河北省衡水中学2021-2022学年高三上学期五调考试化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)黑龙江省佳木斯市第一中学2022届高三下学期验收测试化学试题河北省新乐市第一中学2023-2024学年上学期高三第一次月考化学试题
2 . 钪的价格昂贵,在地壳里的含量只有0.0005%。从铝土矿生产Al2O3的副产品“赤泥”(主要成分为Al2O3、Fe2O3、TiO2、Sc2O3)中回收钪,同时生产聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]具有极其重要的工业价值,一种工艺流程如下:
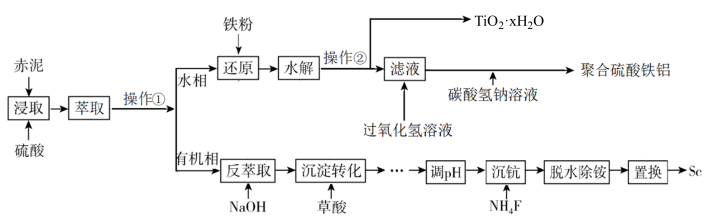
已知:钪离子可以在不同pH下生成[Sc(OH)n] 3-n(n=1~6)。请回答以下问题:
(1)操作②的名称:_______ ,操作①和操作②中都使用的玻璃仪器是_______ 。
(2)加入铁粉的作用:_______ 。
(3)生成聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]的离子方程式为_______ 。
(4)钪是一种重要的稀土金属,化学性质非常活泼,但发现较晚主要是因为_______ 。
(5)“反萃取”时若加入的氢氧化钠过量则 Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应生成 n=6 的含钪产物的化学方程式为_______ 。
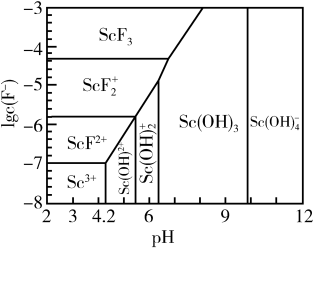
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[1gc(F- )]、pH 的关系如图所示。若溶液中c(F- )=5×10-6,“调 pH”过程中控制 pH=7,则调节pH后三价Sc的存在形式为_______ (填化学式)(lg5=0.7)。
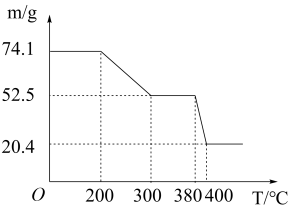
(7)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O 分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至 380-400℃产生白烟,400℃以上质量不再改变。则a=_______ (填数字)。

已知:钪离子可以在不同pH下生成[Sc(OH)n] 3-n(n=1~6)。请回答以下问题:
(1)操作②的名称:
(2)加入铁粉的作用:
(3)生成聚合硫酸铁铝[AlFe(OH)6-2n(SO4)n]的离子方程式为
(4)钪是一种重要的稀土金属,化学性质非常活泼,但发现较晚主要是因为
(5)“反萃取”时若加入的氢氧化钠过量则 Sc(OH)3沉淀会溶解。写出Sc(OH)3与过量NaOH溶液反应生成 n=6 的含钪产物的化学方程式为
(6)常温下,三价Sc的部分存在形式与氟离子浓度的对数[1gc(F- )]、pH 的关系如图所示。若溶液中c(F- )=5×10-6,“调 pH”过程中控制 pH=7,则调节pH后三价Sc的存在形式为

(7)“脱水除铵”过程中,复盐3NH4Cl·ScF3·aH2O 分解得到ScF3,某固体样品质量与温度的关系如图所示。加热至 380-400℃产生白烟,400℃以上质量不再改变。则a=

您最近一年使用:0次
2022-04-22更新
|
1481次组卷
|
11卷引用:押江苏卷第15题 化学工业流程综合题 -备战2022年高考化学临考题号押题(江苏卷)
(已下线)押江苏卷第15题 化学工业流程综合题 -备战2022年高考化学临考题号押题(江苏卷)黑龙江省哈尔滨市第九中学2022届高三下学期第三次模拟考试理综化学试题(已下线)专项15 工艺流程综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)化学-2022年高考考前押题密卷(福建卷)山东师范大学附属中学2022届高三考前预测化学试题吉林市第一中学2021-2022学年高三下学期4月教学质量检测理科综合化学试题湖南省郴州市永兴县第一中学2021-2022学年高三下学期期中考试化学试题湖南省长沙市雅礼中学2022-2023学年高三上学期月考(三)化学试题山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题湖南省攸县第一中学2022-2023学年高三第六次月考化学试题湖南省涟源市第一中学2023届高三第五次月考化学试题
名校
3 . 焦亚硫酸钠Na2S2O5是常用的抗氧化剂,在空气中、受热时均易分解。
(1)化学兴趣小组同学利用下图所示装置(部分夹持装置已略去,实验前已除去装置中的空气)制取Na2S2O5并探究SO2的性质。
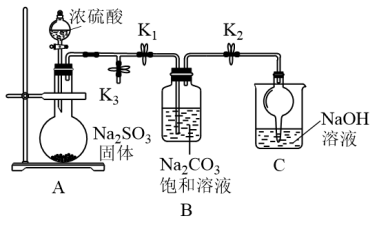
I.打开K1和K2,关闭K3,制取Na2S2O5。
①Na2S2O5中O元素化合价为-2,其中S的化合价为___________ ;装置C中干燥管的作用是______ 。
②B中通入过量SO2充分反应后,经冷却结晶时发生反应2NaHSO3=Na2S2O5+H2O可获得Na2S2O5晶体。B中生成NaHSO3的化学方程式为____ 。
③B中所得Na2S2O5晶体常用饱和SO2水溶液洗涤。用饱和SO2水溶液洗涤的目的除洗去产物表面的杂质离子外还有_______ 。
④已知Na2S2O5、Na2SO3分别与稀硫酸反应得到的产物相同。请设计检验Na2S2O5样品中是否含Na2SO4的实验方案:______ 。
II.更换B瓶中的溶液,探究SO2的性质。
⑤将B中溶液更换为品红的乙醇溶液,无明显现象,而将SO2通入品红的水溶液中,溶液褪色。可推知,_______ 不能使品红褪色。
(2)葡萄酒中常加入Na2S2O5作抗氧化剂。测定某葡萄酒中Na2S2O5残留量的实验步骤如下:取50.00mL葡萄酒样品,用0.0100mol·L-1的I2标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液10.00mL,已知滴定过程中发生的反应为:S2O +I2+H2O
+I2+H2O SO
SO +I-+H+(未配平)。计算该葡萄酒中Na2S2O5的残留量
+I-+H+(未配平)。计算该葡萄酒中Na2S2O5的残留量_____ (以g·L-1为单位,写出计算过程)。
(1)化学兴趣小组同学利用下图所示装置(部分夹持装置已略去,实验前已除去装置中的空气)制取Na2S2O5并探究SO2的性质。

I.打开K1和K2,关闭K3,制取Na2S2O5。
①Na2S2O5中O元素化合价为-2,其中S的化合价为
②B中通入过量SO2充分反应后,经冷却结晶时发生反应2NaHSO3=Na2S2O5+H2O可获得Na2S2O5晶体。B中生成NaHSO3的化学方程式为
③B中所得Na2S2O5晶体常用饱和SO2水溶液洗涤。用饱和SO2水溶液洗涤的目的除洗去产物表面的杂质离子外还有
④已知Na2S2O5、Na2SO3分别与稀硫酸反应得到的产物相同。请设计检验Na2S2O5样品中是否含Na2SO4的实验方案:
II.更换B瓶中的溶液,探究SO2的性质。
⑤将B中溶液更换为品红的乙醇溶液,无明显现象,而将SO2通入品红的水溶液中,溶液褪色。可推知,
(2)葡萄酒中常加入Na2S2O5作抗氧化剂。测定某葡萄酒中Na2S2O5残留量的实验步骤如下:取50.00mL葡萄酒样品,用0.0100mol·L-1的I2标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液10.00mL,已知滴定过程中发生的反应为:S2O
 +I2+H2O
+I2+H2O SO
SO +I-+H+(未配平)。计算该葡萄酒中Na2S2O5的残留量
+I-+H+(未配平)。计算该葡萄酒中Na2S2O5的残留量
您最近一年使用:0次
2022-01-14更新
|
732次组卷
|
2卷引用:江苏省苏州市2021-2022学年高一上学期期末学业质量阳光指标调研化学试题
解题方法
4 . 以Fe2O3/CeO2作催化剂,可用乙烯脱除烟气中SO2并回收单质硫。某兴趣小组同学设计实验验证该反应并检验产物中的CO2,实验装置(夹持装置已略)如图所示:
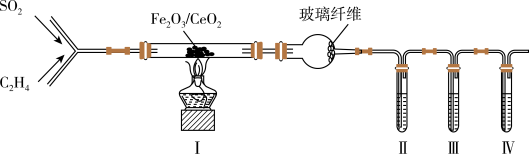
已知:反应原理为:CH2=CH2+3SO2 3S+2CO2+2H2O。装置Ⅰ生成的S、CO2、H2O均为气体。
3S+2CO2+2H2O。装置Ⅰ生成的S、CO2、H2O均为气体。
(1)装置中玻璃纤维的作用是___ 。
(2)为检验CO2,则装置Ⅱ、Ⅲ、Ⅳ中盛放的试剂依次是___ (填序号)。
①酸性KMnO4溶液②澄清石灰水③Br2的CCl4溶液
(3)为制作反应的催化剂,实验小组制备了一定质量的Fe2O3(含FeO杂质)样品,为测定其中Fe2O3的质量分数,现进行如下实验:
步骤1:称取0.20g样品,向样品中加入足量的盐酸使其完全溶解。
步骤2:向溶液中加入足量的KI溶液,充分反应。
步骤3:向溶液中加入0.10mol·L-1Na2S2O3溶液,恰好完全反应时消耗Na2S2O3溶液体积为20.00mL生成Na2S4O6。
计算样品中所含Fe2O3的质量分数___ 。(写出计算过程)

已知:反应原理为:CH2=CH2+3SO2
 3S+2CO2+2H2O。装置Ⅰ生成的S、CO2、H2O均为气体。
3S+2CO2+2H2O。装置Ⅰ生成的S、CO2、H2O均为气体。(1)装置中玻璃纤维的作用是
(2)为检验CO2,则装置Ⅱ、Ⅲ、Ⅳ中盛放的试剂依次是
①酸性KMnO4溶液②澄清石灰水③Br2的CCl4溶液
(3)为制作反应的催化剂,实验小组制备了一定质量的Fe2O3(含FeO杂质)样品,为测定其中Fe2O3的质量分数,现进行如下实验:
步骤1:称取0.20g样品,向样品中加入足量的盐酸使其完全溶解。
步骤2:向溶液中加入足量的KI溶液,充分反应。
步骤3:向溶液中加入0.10mol·L-1Na2S2O3溶液,恰好完全反应时消耗Na2S2O3溶液体积为20.00mL生成Na2S4O6。
计算样品中所含Fe2O3的质量分数
您最近一年使用:0次
2021-06-23更新
|
579次组卷
|
2卷引用:江苏省南京市六校联考2020-2021学年高一下学期期末考试化学试题
5 . 镀镍废水是重金属污染源之一,常见处理含镍废水的一种离子交换和沉淀法工艺如下:
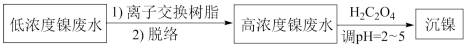
已知该交换树脂为阳离子型树脂HR,HR R-+H+;NiR2(aq)
R-+H+;NiR2(aq) Ni2+(aq)+2R-(aq)。
Ni2+(aq)+2R-(aq)。
(1)Ni2+的核外电子排布式为___________ 。
(2)已知在pH=2时,离子交换过程Ni2+去除率很低,其原因为_______ 。
(3)“脱络”(指镍元素由络合物NiR2转化成游离的Ni2+)过程中,R-与中间产物·OH(羟基自由基)反应生成难以与Ni2+络合的·R(有机物自由基),但·OH也能与H2O2发生反应。反应的方程式如下:
Ⅰ.Fe2++H2O2=Fe3++OH-+·OH
Ⅱ.R-+·OH=OH-+·R
平衡移动的角度解释加入FeSO4和H2O2能够实现“脱络”的原因是___________ 。
(4)NiC2O4隔绝空气高温煅烧可制得Ni2O3,NiC2O4受热分解的化学方程式为___________ 。
(5)硫酸镍铵(NH4)xNiy(SO4)m·nH2O可用于电镀等领域,为测定其组成,进行如下实验:
①称取4.670样品,配成250mL溶液A。
②取25.00mL溶液A,加足量浓NaOH溶液并加热,生成NH3 44.80mL (标准状况)。
③另取25.00mL溶液A,用0.05000mol/L的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),平行测定三次,平均消耗标准EDTA溶液20.00mL。
则硫酸镍铵的化学式为___________ (写出计算过程)。

已知该交换树脂为阳离子型树脂HR,HR
 R-+H+;NiR2(aq)
R-+H+;NiR2(aq) Ni2+(aq)+2R-(aq)。
Ni2+(aq)+2R-(aq)。(1)Ni2+的核外电子排布式为
(2)已知在pH=2时,离子交换过程Ni2+去除率很低,其原因为
(3)“脱络”(指镍元素由络合物NiR2转化成游离的Ni2+)过程中,R-与中间产物·OH(羟基自由基)反应生成难以与Ni2+络合的·R(有机物自由基),但·OH也能与H2O2发生反应。反应的方程式如下:
Ⅰ.Fe2++H2O2=Fe3++OH-+·OH
Ⅱ.R-+·OH=OH-+·R
平衡移动的角度解释加入FeSO4和H2O2能够实现“脱络”的原因是
(4)NiC2O4隔绝空气高温煅烧可制得Ni2O3,NiC2O4受热分解的化学方程式为
(5)硫酸镍铵(NH4)xNiy(SO4)m·nH2O可用于电镀等领域,为测定其组成,进行如下实验:
①称取4.670样品,配成250mL溶液A。
②取25.00mL溶液A,加足量浓NaOH溶液并加热,生成NH3 44.80mL (标准状况)。
③另取25.00mL溶液A,用0.05000mol/L的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),平行测定三次,平均消耗标准EDTA溶液20.00mL。
则硫酸镍铵的化学式为
您最近一年使用:0次
6 . ZnSe是一种光电性能优异的II~VI族半导体材料,人们开发出了多种制备ZnSe纳米粒子的方法。某研究小组用如下方法制备了ZnSe纳米粒子。
①将1mmol的Zn(NO3)2·6H2O溶于去离子水中形成无色澄清溶液,往该溶液中加入1mmolSeO2,超声完全溶解后形成无色澄清溶液;
②再加入过量的水合肼(N2H4·H2O),超声几分钟后将溶液转移到内衬聚四氟乙烯套的不锈钢高压反应釜中,将高压反应釜拧紧密封后放在160°C的恒温干燥箱中保温12小时(已知肼有强还原性,Se在碱性条件下可发生岐化反应);
③反应结束后自然冷却至室温,得到淡黄色沉淀,将产物用蒸馏水和无水乙醇洗涤数次,干燥后得到产物。将产物用X-射线粉末衍射仪(XRD)和X射线能谱仪进行物相和成分分析,发现其Zn和Se的原子个数比接近1:1。
(1)写出过程①中的化学方程式:_______
(2)写出过程②中的离子方程式:_______
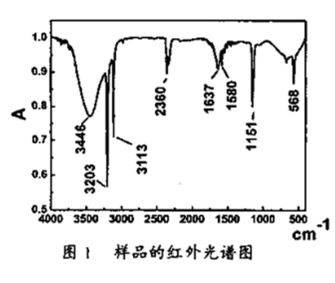
(3)产物样品的红外光谱分析结果如图1所示,该谱图反映出产物有明显的N-H、N-N吸收峰。这是因为产物中可能含有:_______ 。
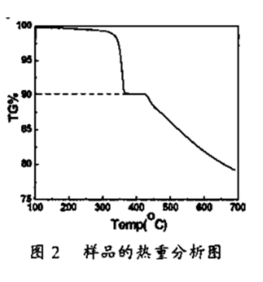
(4)产物样品的热重(重量-温度关系图)分析结果如图2所示,根据图1和图2提供的信息,推测产物的化学式可能为:_______ 。
①将1mmol的Zn(NO3)2·6H2O溶于去离子水中形成无色澄清溶液,往该溶液中加入1mmolSeO2,超声完全溶解后形成无色澄清溶液;
②再加入过量的水合肼(N2H4·H2O),超声几分钟后将溶液转移到内衬聚四氟乙烯套的不锈钢高压反应釜中,将高压反应釜拧紧密封后放在160°C的恒温干燥箱中保温12小时(已知肼有强还原性,Se在碱性条件下可发生岐化反应);
③反应结束后自然冷却至室温,得到淡黄色沉淀,将产物用蒸馏水和无水乙醇洗涤数次,干燥后得到产物。将产物用X-射线粉末衍射仪(XRD)和X射线能谱仪进行物相和成分分析,发现其Zn和Se的原子个数比接近1:1。
(1)写出过程①中的化学方程式:
(2)写出过程②中的离子方程式:
(3)产物样品的红外光谱分析结果如图1所示,该谱图反映出产物有明显的N-H、N-N吸收峰。这是因为产物中可能含有:

(4)产物样品的热重(重量-温度关系图)分析结果如图2所示,根据图1和图2提供的信息,推测产物的化学式可能为:

您最近一年使用:0次
名校
7 . 蓝色钾盐水合物KaCub(C2O4)c·H2O(铜元素为+2价)的组成可通过下列实验确定:
步骤①:称取一定质量的样品置于锥形瓶中,加入适量2 mol·L-1稀硫酸,微热使样品溶解。再加入30 mL水加热,用0.0200 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液12.00 mL(MnO 的还原产物为Mn2+)。
的还原产物为Mn2+)。
步骤②:充分加热滴定后的溶液,冷却后,调节pH并加入过量的KI固体,溶液变为棕色并产生白色沉淀CuI,发生反应2Cu2++4I-=2CuI↓+I2
步骤③:加入少量淀粉溶液作指示剂,用0.0200 mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液15.00 mL,发生反应I2+2 =2I-+
=2I-+
(1)步骤①中需事先配制好250mL 0.0200 mol·L-1KMnO4标准溶液,配制KMnO4溶液时除需用到烧杯、玻璃棒外,还用到的玻璃仪器有___________ 、___________ 。
(2)若步骤②反应后未及时进行步骤③的操作,则测出的Cu2+的物质的量将___________ (填“偏大”、“偏小” 或“不变”) 。
(3)步骤③中滴定终点的现象是___________ 。
(4)通过计算确定a∶b∶c=___________ 。(请写出计算过程,否则不能得分)。
步骤①:称取一定质量的样品置于锥形瓶中,加入适量2 mol·L-1稀硫酸,微热使样品溶解。再加入30 mL水加热,用0.0200 mol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液12.00 mL(MnO
 的还原产物为Mn2+)。
的还原产物为Mn2+)。步骤②:充分加热滴定后的溶液,冷却后,调节pH并加入过量的KI固体,溶液变为棕色并产生白色沉淀CuI,发生反应2Cu2++4I-=2CuI↓+I2
步骤③:加入少量淀粉溶液作指示剂,用0.0200 mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液15.00 mL,发生反应I2+2
 =2I-+
=2I-+
(1)步骤①中需事先配制好250mL 0.0200 mol·L-1KMnO4标准溶液,配制KMnO4溶液时除需用到烧杯、玻璃棒外,还用到的玻璃仪器有
(2)若步骤②反应后未及时进行步骤③的操作,则测出的Cu2+的物质的量将
(3)步骤③中滴定终点的现象是
(4)通过计算确定a∶b∶c=
您最近一年使用:0次
名校
8 . 血液中的钙离子平衡在临床医学中具有重要的意义。某研究小组为测定血液样品中Ca2+的含量,进行的实验如下:
①量取5.0mL血液样品,处理后配制成100mL溶液;
②量取10.0mL溶液,加入过量(NH4)2C2O4溶液,使Ca2+完全转化成CaC2O4沉淀;
③过滤并洗净所得的CaC2O4沉淀,用过量稀硫酸溶解,生成H2C2O4和CaSO4稀溶液;
④加入0.001mol·L-1的酸性KMnO4溶液,使H2C2O4完全氧化,同时产生使澄清石灰水变浑浊的无色无味气体,消耗酸性KMnO4溶液的体积为2.00mL。
(1)步骤①中用到的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、___ 。
(2)配平步骤④中发生反应的化学方程式并用双线桥指明电子转移情况:KMnO4+H2C2O4+H2SO4=↑+K2SO4+MnSO4+H2O。___ 。
氧化产物与还原产物的物质的量之比为___ 。
(3)血样中Ca2+的含量为___ g·mL-1。(写出计算过程)
①量取5.0mL血液样品,处理后配制成100mL溶液;
②量取10.0mL溶液,加入过量(NH4)2C2O4溶液,使Ca2+完全转化成CaC2O4沉淀;
③过滤并洗净所得的CaC2O4沉淀,用过量稀硫酸溶解,生成H2C2O4和CaSO4稀溶液;
④加入0.001mol·L-1的酸性KMnO4溶液,使H2C2O4完全氧化,同时产生使澄清石灰水变浑浊的无色无味气体,消耗酸性KMnO4溶液的体积为2.00mL。
(1)步骤①中用到的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、
(2)配平步骤④中发生反应的化学方程式并用双线桥指明电子转移情况:KMnO4+H2C2O4+H2SO4=↑+K2SO4+MnSO4+H2O。
氧化产物与还原产物的物质的量之比为
(3)血样中Ca2+的含量为
您最近一年使用:0次
名校
解题方法
9 . 亚硝酸钠(NaNO2)是一种工业盐,实验室可用如图装置(略去部分夹持仪器)制备。

已知:
① ;
;
② ;
;
③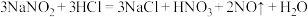 ;
;
④酸性条件下,NO和 都能与
都能与 反应生成
反应生成 和
和 ;
; 能使酸性高锰酸钾溶液褪色。
能使酸性高锰酸钾溶液褪色。
(1)加热装置A前,先通一段时间N2,目的是_______ ;
(2)装置A中发生反应的化学方程式为_______ ;
(3)实验结束后,B瓶溶液中溶质的主要成分是_______ (填化学式)。
(4)仪器C中盛放的药品为_______ (填名称)。
(5)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,_______ ,则产物是NaNO2 (注明试剂、现象)。
(6)装置F的作用是_______ ;
(7)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000molL酸性KMnO4溶液20.00mL,两者恰好完全反应。计算所得固体中亚硝酸钠的质量分数_______ 。(写出计算过程)

已知:
①
 ;
;②
 ;
;③
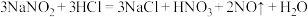 ;
;④酸性条件下,NO和
 都能与
都能与 反应生成
反应生成 和
和 ;
; 能使酸性高锰酸钾溶液褪色。
能使酸性高锰酸钾溶液褪色。(1)加热装置A前,先通一段时间N2,目的是
(2)装置A中发生反应的化学方程式为
(3)实验结束后,B瓶溶液中溶质的主要成分是
(4)仪器C中盛放的药品为
(5)充分反应后,检验装置D中产物的方法是:取产物少许置于试管中,
(6)装置F的作用是
(7)为测定亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,再向锥形瓶中加入0.1000molL酸性KMnO4溶液20.00mL,两者恰好完全反应。计算所得固体中亚硝酸钠的质量分数
您最近一年使用:0次
2021-04-28更新
|
449次组卷
|
4卷引用:江苏省常熟市2020-2021学年高一下学期期中化学试题
解题方法
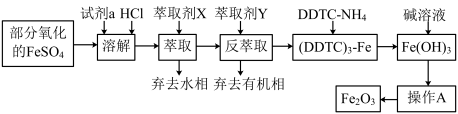
10 . 某化学小组用部分氧化的FeSO4为原料,以萃取剂X(甲基异丁基甲酮)萃取法制取高纯氧化铁(Fe2O3),并进行铁含量的测定。主要操作步骤如下:
已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH4+Fe3+=(DDTC)3-Fe↓+3NH 。
。
请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式___ 。
(2)可作反萃取的萃取剂Y的最佳试剂是___ (填试剂名称)。
(3)操作A为___ 、___ 、___ 。产品处理时,温度对产品的纯度有很大影响。已知温度对产物纯度的影响如图所示,则温度最好控制在___ ℃。

(4)现准确称取4.000g样品,经酸溶、还原为Fe2+,在容量瓶中配成100ml溶液,移取25.00ml溶液于锥形瓶中,用0.1000mol/L的K2Cr2O7溶液进行滴定,消耗K2Cr2O7溶液20.60ml。产品中铁的含量为___ (假设杂质不与K2Cr2O7反应)。

已知:①在较高的盐酸浓度下,Fe3+能溶解于甲基异丁基甲酮,当盐酸浓度降低时,该化合物解离。
②3DDTC-NH4+Fe3+=(DDTC)3-Fe↓+3NH
 。
。请回答下列问题:
(1)写出加入试剂a发生反应的离子方程式
(2)可作反萃取的萃取剂Y的最佳试剂是
(3)操作A为

(4)现准确称取4.000g样品,经酸溶、还原为Fe2+,在容量瓶中配成100ml溶液,移取25.00ml溶液于锥形瓶中,用0.1000mol/L的K2Cr2O7溶液进行滴定,消耗K2Cr2O7溶液20.60ml。产品中铁的含量为
您最近一年使用:0次



