名校
解题方法
1 . 钻(Co)及其化合物在工业上有广泛应用。为从某工业废料中回收钴,某学生设计流程如图(废料中含有Al、Li、Co2O3和Fe2O3等物质)。
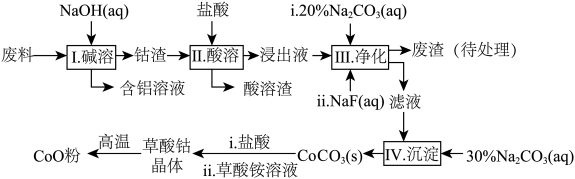
已知: LiF难溶于水,Li2CO3微溶于水。
请回答:
(1)写出I中发生反应的化学方程式并用单线桥标记电子转移的方向和数目________ 。
(2)写出步骤中Co2O3与盐酸反应生成Cl2的离子方程式_______________ 。
(3)步骤II所得废渣的主要成分除了LiF外,还有________________ 。
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤IV所起的作用是___________ 。
(5)在空气中加热10.98g草酸钴晶体(CoC2O4•2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。已知:M(CoC2O4•2H2O)=183g/mol。
经测定,加热到210℃时,固体物质的化学式为_____ 。加热到210--290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是_________ 。温度高于890℃时,固体产物发生分解反应,固体产物为__________ 。

已知: LiF难溶于水,Li2CO3微溶于水。
请回答:
(1)写出I中发生反应的化学方程式并用单线桥标记电子转移的方向和数目
(2)写出步骤中Co2O3与盐酸反应生成Cl2的离子方程式
(3)步骤II所得废渣的主要成分除了LiF外,还有
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤IV所起的作用是
(5)在空气中加热10.98g草酸钴晶体(CoC2O4•2H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。已知:M(CoC2O4•2H2O)=183g/mol。
| 温度范围/℃ | 固体质量/g |
| 150--210 | 8.82 |
| 290--320 | 4.82 |
| 890--920 | 4.5 |
经测定,加热到210℃时,固体物质的化学式为
您最近一年使用:0次
2018-05-13更新
|
504次组卷
|
2卷引用:【全国百强校】河南省南阳市第一中学2018届高三第十五次考试理科综合化学试题
名校
2 . (1)某小组的同学欲探究NH3经一系列反应得到HNO3和NH4NO3的过程,NH3的转化过程如下图所示。
甲、乙两同学分别按下图所示装置进行实验。用于A、B装置中的可选药品:浓氨水、30%H2O2溶液、蒸馏水、NaOH固体、MnO2

①装置A的圆底烧瓶中发生反应的化学方程式为__________ 。装置E有多种作用,下列关于装置E的作用或其中所盛液体的说法中,不正确的是_________ (填下列序号字母)。
a.使氨气和氧气充分混合 b.控制通入氨气和氧气的体积比
c.平衡装置内的压强 d.锥形瓶内液体是饱和食盐水
②甲同学先点燃酒精灯,再打开K1、K2、K3、K4,反应一段时间后,成功模拟了反应过程,并将实验中产生的气体持续通入装置H一段时间后,H中的溶液变成蓝色,则其中铜片所参与反应的离子方程式为_______ ,若制得的氨气仅按I→Ⅱ→III的顺序完全转化为硝酸,欲使H装置中所得溶液为纯净的CuSO4溶液(忽略Cu2+的水解),理论上所需氨气在标准状况下的体积为______ L(假设硝酸与铜反应产生的还原产物全部排出反应装置);
③乙同学为模拟过程IV的反应,在甲同学操作的基础上对该装置进行了下列各项中的一项操作,使G处圆底烧瓶中产生大量白烟,你认为这项操作是_________ (填下列序号字母)。
a.关闭K3并熄灭酒精灯 b.关闭K4并熄灭酒精灯 c.关闭K3、K4并熄灭酒精灯
④丙同学认为该系列实验装置存在一处明显的设计缺陷,你认为该设计缺陷是__________ 。
(2)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。

①如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置是_____ (填写字母)。
②若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有40%亚硫酸钠(质量分数),被氧化成硫酸钠,则至少需称取该亚硫酸钠_______ g(保留一位小数)。
③某热电厂上空大气中所含二氧化硫严重超标,现对该区域雨水样品进行探究。首先用pH试纸测定雨水样品的pH,操作方法为_______________ ,测得样品pH约为3;为进一步探究由SO2所形成酸雨的性质,将一定量的SO2通入蒸馏水中,配成pH为3的溶液,然后将溶液分为A、B两份,将溶液B久置于空气中,与密闭保存的A相比,久置后的溶液B中水的电离程度将_______ (填“增大”、“减小”或“不变”)。

甲、乙两同学分别按下图所示装置进行实验。用于A、B装置中的可选药品:浓氨水、30%H2O2溶液、蒸馏水、NaOH固体、MnO2

①装置A的圆底烧瓶中发生反应的化学方程式为
a.使氨气和氧气充分混合 b.控制通入氨气和氧气的体积比
c.平衡装置内的压强 d.锥形瓶内液体是饱和食盐水
②甲同学先点燃酒精灯,再打开K1、K2、K3、K4,反应一段时间后,成功模拟了反应过程,并将实验中产生的气体持续通入装置H一段时间后,H中的溶液变成蓝色,则其中铜片所参与反应的离子方程式为
③乙同学为模拟过程IV的反应,在甲同学操作的基础上对该装置进行了下列各项中的一项操作,使G处圆底烧瓶中产生大量白烟,你认为这项操作是
a.关闭K3并熄灭酒精灯 b.关闭K4并熄灭酒精灯 c.关闭K3、K4并熄灭酒精灯
④丙同学认为该系列实验装置存在一处明显的设计缺陷,你认为该设计缺陷是
(2)实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。

①如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置是
②若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有40%亚硫酸钠(质量分数),被氧化成硫酸钠,则至少需称取该亚硫酸钠
③某热电厂上空大气中所含二氧化硫严重超标,现对该区域雨水样品进行探究。首先用pH试纸测定雨水样品的pH,操作方法为
您最近一年使用:0次
2017-10-30更新
|
203次组卷
|
2卷引用:河南省安阳市第三十六中学2018届高三上学期第一次月考化学试题
3 . 保险粉(Na2S2O4)有极强的还原性,遇热水或潮湿空气会分解发热,但在碱性环境下较稳定。回答下列问题:
(1)二氧化硫的制备
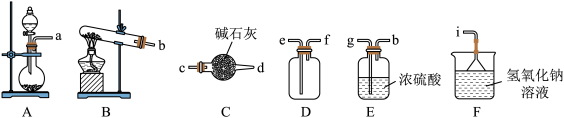
①二氧化硫的发生装置可以选择上图中的_____________ (填大写字母),反应的化学方程式为______________________ 。
②欲收集一瓶干燥的二氧化硫,选择上图中的装置,其接口的连接顺序为发生装置→__________________ →______ →______ →______ → ____________ 。(按气流方向,用小写字母表示)
(2)保险粉的制备
在35-45℃下,将SO2气体通入锌粉一水悬浮液中(如图),使之发生反应生成ZnS2O4;待反应完全后,移走恒温水浴装置并冷却至室温,向三颈烧瓶中加入18%的NaOH溶液,使之发生反应生成Na2S2O4和Zn(OH)2;经一系列操作后得到无水Na2S2O4样品。
①实验开始时,应先关闭止水夹K3、打开K1和K2,通入一段时间SO2,其原因是__________ 。
②通过观察_________________ ,调节止水夹K1来控制SO2的流速。
③由ZnS2O4生成Na2S2O4的化学方程式为_____________ 。
(3)称取2.0gNa2S2O4样品溶于冷水中,配成100mL吐溶液,取出10mL该溶液于试管中,用0 .10 mol/L的KMnO4溶液滴定(滴定至终点时产物为Na2SO4和MnSO4),重复上述操作2次,平均消耗溶液12.00mL。则该样品中Na2S2O4的质量分数为_______ (杂质不参与反应)。
(1)二氧化硫的制备

①二氧化硫的发生装置可以选择上图中的
②欲收集一瓶干燥的二氧化硫,选择上图中的装置,其接口的连接顺序为发生装置→
(2)保险粉的制备
在35-45℃下,将SO2气体通入锌粉一水悬浮液中(如图),使之发生反应生成ZnS2O4;待反应完全后,移走恒温水浴装置并冷却至室温,向三颈烧瓶中加入18%的NaOH溶液,使之发生反应生成Na2S2O4和Zn(OH)2;经一系列操作后得到无水Na2S2O4样品。

①实验开始时,应先关闭止水夹K3、打开K1和K2,通入一段时间SO2,其原因是
②通过观察
③由ZnS2O4生成Na2S2O4的化学方程式为
(3)称取2.0gNa2S2O4样品溶于冷水中,配成100mL吐溶液,取出10mL该溶液于试管中,用0 .10 mol/L的KMnO4溶液滴定(滴定至终点时产物为Na2SO4和MnSO4),重复上述操作2次,平均消耗溶液12.00mL。则该样品中Na2S2O4的质量分数为
您最近一年使用:0次
2017-03-14更新
|
666次组卷
|
3卷引用:2017届河南省豫南九校(中原名校)高三下学期质量考评八理综化学试卷
4 . CaS可用于制备发光漆、用作脱毛剂、杀虫剂、硫脲等,还用于医药工业、重金属处理及环保中。某化学探究小组在实验室中利用反应: CaSO4+C CaS+CaO+SO2↑+CO↑+CO2↑制备硫化钙并检验产物,可选用的装置如下。回答下列问题:
CaS+CaO+SO2↑+CO↑+CO2↑制备硫化钙并检验产物,可选用的装置如下。回答下列问题:
已知:①C及E ~ H中的试剂均为足量。
②酸性KMnO4溶液作氧化剂时,锰元素被还原成Mn2+
③CaS与H2O反应生成Ca(OH)2和H2S。
(1)实验1:若只检验生成物中是否含有CO,可采用的装置组合为______ (按气流方向,填字母组合),生成物中存在CO的现象是________________________ 。
(2)实验2:若只检验生成物中是否含有CO2,可采用的最简单的装置组合为______ (按气流方向,填字母组合),除去SO2的离子方程式为__________________________ 。
(3)实验3:若同时检验CO2和SO2,采用的装置组合为_______ (按气流方向,填字母组合)。
(4)若制备反应的条件完全相同,将产生的气体全部通入上述实验装置中,得到的有关数据如下表:
写出CaSO4和焦炭在高温条件下反应生成CaS的化学方程式:_______________ 。
(5)为了证明硫化钙的化学式设计如下实验:将一定质量(m1)的样品溶于足量的饱和Na2CO3溶液中,通过____ 操作,称得固体质量为m2,则表示硫化钙组成的计算式为n(Ca):n(S)=__________ (用含m1、m2的代数式表示)。
 CaS+CaO+SO2↑+CO↑+CO2↑制备硫化钙并检验产物,可选用的装置如下。回答下列问题:
CaS+CaO+SO2↑+CO↑+CO2↑制备硫化钙并检验产物,可选用的装置如下。回答下列问题:

已知:①C及E ~ H中的试剂均为足量。
②酸性KMnO4溶液作氧化剂时,锰元素被还原成Mn2+
③CaS与H2O反应生成Ca(OH)2和H2S。
(1)实验1:若只检验生成物中是否含有CO,可采用的装置组合为
(2)实验2:若只检验生成物中是否含有CO2,可采用的最简单的装置组合为
(3)实验3:若同时检验CO2和SO2,采用的装置组合为
(4)若制备反应的条件完全相同,将产生的气体全部通入上述实验装置中,得到的有关数据如下表:
| 实验前 | 实验后 | |
| 实验1 | 装置C硬质玻璃管连同CuO质量为26.80 g | 装置C硬质玻璃管连同反应后固体质量为26.64 g |
| 实验2 | 装置G连同溶液质量为187.50g | 装置G连同反应后溶液及沉淀的质量为188.38 g |
| 实验3 | 装置D、H连同溶液质量和为373.60g | 装置D、H连同溶液质量和为374.24 g |
(5)为了证明硫化钙的化学式设计如下实验:将一定质量(m1)的样品溶于足量的饱和Na2CO3溶液中,通过
您最近一年使用:0次
2013·江苏·一模
解题方法
5 . K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备K2SO4和Mn3O4的工艺流程如下:
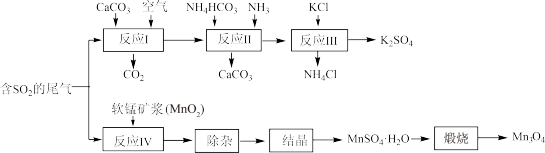
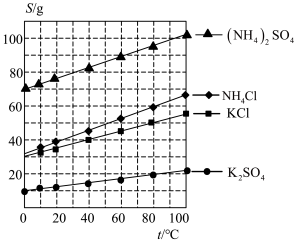

(1)几种盐的溶解度见上图。反应Ⅲ中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行蒸发浓缩、______ 、洗涤、干燥等操作即得K2SO4产品。
(2)检验K2SO4样品是否含有氯化物杂质的实验操作是______ 。
(3)反应Ⅳ的化学方程式为______ 。
(4)Mn3O4与浓盐酸加热时发生反应的离子方程式为______ 。
(5)上图煅烧MnSO4·H2O时温度与剩余固体质量变化曲线。
①该曲线中B段所表示物质的化学式为______ 。
②煅烧过程中固体锰含量随温度的升高而增大,但当温度超过1000℃时,再冷却后,测得产物的总锰含量反而减小。试分析产物总锰含量减小的原因______ 。



(1)几种盐的溶解度见上图。反应Ⅲ中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行蒸发浓缩、
(2)检验K2SO4样品是否含有氯化物杂质的实验操作是
(3)反应Ⅳ的化学方程式为
(4)Mn3O4与浓盐酸加热时发生反应的离子方程式为
(5)上图煅烧MnSO4·H2O时温度与剩余固体质量变化曲线。
①该曲线中B段所表示物质的化学式为
②煅烧过程中固体锰含量随温度的升高而增大,但当温度超过1000℃时,再冷却后,测得产物的总锰含量反而减小。试分析产物总锰含量减小的原因
您最近一年使用:0次
2016-12-09更新
|
1279次组卷
|
4卷引用:2016届河南省中原名校联盟高三4月高考仿真模拟联考化学试卷
2016届河南省中原名校联盟高三4月高考仿真模拟联考化学试卷2016届河南省中原名校联盟高三四月高考仿真模拟理综化学试卷(已下线)2013届江苏省苏锡常镇徐连六市高三3月教学情况调研(一)化学试卷2016届江西省吉安一中高三5月模拟考试理综化学试卷
解题方法
6 . 某学习小组在实验室制取乙酸乙酯的主要步骤如下:
①配制2mL浓硫酸、3mL乙醇(含18O)和2mL乙酸的混合溶液
②按如图连接好装置并加入混合液,用小火均匀加热3~5min
③待试管乙收集到一定量产物后停止加热,撤出试管乙用力振荡,然后静置待分层
④分离出乙酸乙酯,洗涤、干燥。
回答问题:

(1)装置中球形干燥管,除起冷凝作用外,另一重要作用是___________________ 。
(2)步骤(2)安装好实验装置,加入样品前还应检查____________________ 。
(3)反应中浓硫酸的作用是_____________________ ;
写出能表示18O位置的制取乙酸乙酯的化学方程式_______________________ 。
(4)上述实验中饱和碳酸钠溶液的作用是(填字母)____________ 。
(5)步骤③所观察到的现象是____________________ ;从试管乙中分离出乙酸乙酯的实验操作名称是 __________________ 。
①配制2mL浓硫酸、3mL乙醇(含18O)和2mL乙酸的混合溶液
②按如图连接好装置并加入混合液,用小火均匀加热3~5min
③待试管乙收集到一定量产物后停止加热,撤出试管乙用力振荡,然后静置待分层
④分离出乙酸乙酯,洗涤、干燥。
回答问题:

(1)装置中球形干燥管,除起冷凝作用外,另一重要作用是
(2)步骤(2)安装好实验装置,加入样品前还应检查
(3)反应中浓硫酸的作用是
写出能表示18O位置的制取乙酸乙酯的化学方程式
(4)上述实验中饱和碳酸钠溶液的作用是(填字母)
| A.中和乙酸并吸收乙醇 |
| B.中和乙酸和乙醇 |
| C.减少乙酸乙酯的溶解 |
| D.加速酯的生成,提高其产率 |
您最近一年使用:0次
2016-12-09更新
|
709次组卷
|
2卷引用:2016-2017学年河南省许昌市五校高二上学期第一次联考化学试卷



