名校
1 . 氧化锌为白色固体,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下:

提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是 MnO2。回答下列问题:
(1)为加快步骤①的浸取速率,下列措施中无法达到目的是_____ (填字母)。
a.将样品粉碎 b.延长浸取时间 c.充分搅拌
d.适当增加硫酸浓度 e.适当升高温度
(2)反应②中除掉的杂质离子是_____ (填离子符号),发生反应的离子方程式为:_____ 。
(3)加入高锰酸钾溶液前,若 pH 较低,对除杂的影响是_____ 。
(4)步骤③过滤得到的滤渣中,除了过量的锌外还有_____ 。
(5)反应④中产物的成分可能是 ZnCO3•xZn(OH)2。取干燥后的滤饼 11.2 g,煅烧后可得到产品 8.1 g,则 x=_____ 【ZnCO3、Zn(OH)2的相对分子质量分别为:125、99】。

提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是 MnO2。回答下列问题:
(1)为加快步骤①的浸取速率,下列措施中无法达到目的是
a.将样品粉碎 b.延长浸取时间 c.充分搅拌
d.适当增加硫酸浓度 e.适当升高温度
(2)反应②中除掉的杂质离子是
(3)加入高锰酸钾溶液前,若 pH 较低,对除杂的影响是
(4)步骤③过滤得到的滤渣中,除了过量的锌外还有
(5)反应④中产物的成分可能是 ZnCO3•xZn(OH)2。取干燥后的滤饼 11.2 g,煅烧后可得到产品 8.1 g,则 x=
您最近一年使用:0次
2 . 叠氮化钠(NaN3)是汽车安全气囊的主要成分,实验室制取叠氮化钠的实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气。
②加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
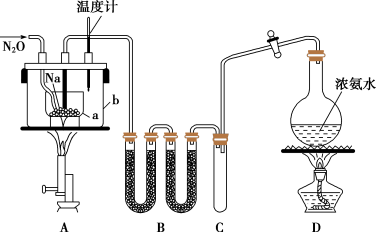
(1)装置B中盛放的药品为____ 。
(2)步骤①中先加热通氨气一段时间的目的是____ ;步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为____ 。步骤③中最适宜的加热方式为___ (填“水浴加热”,“油浴加热”)。
(3)生成NaN3的化学方程式为____ 。
(4)产率计算
①称取2.0 g叠氮化钠试样,配成100 mL溶液,并量取10.00 mL溶液于锥形瓶中。
②用滴定管加入0.10 mol·L-1六硝酸铈铵[(NH4)2Ce(NO3)6]溶液40.00 mL[发生的反应为2(NH4)2Ce(NO3)6+2NaN3===4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑](杂质均不参与反应)。
③充分反应后滴入2滴邻菲罗啉指示液,并用0.10 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]为标准液,滴定过量的Ce4+,终点时消耗标准溶液20.00 mL(滴定原理:Ce4++Fe2+=Ce3++Fe3+)。计算可知叠氮化钠的质量分数为____ (保留2位有效数字)。若其他操作及读数均正确,滴定到终点后,下列操作会导致所测定样品中叠氮化钠质量分数偏大的是____ (填字母代号)。
A.锥形瓶使用叠氮化钠溶液润洗
B.滴加六硝酸铈铵溶液时,滴加前仰视读数,滴加后俯视读数
C.滴加硫酸亚铁铵标准溶液时,开始时尖嘴处无气泡,结束时出现气泡
D.滴定过程中,将挂在锥形瓶壁上的硫酸亚铁铵标准液滴用蒸馏水冲进瓶内
(5)叠氮化钠有毒,可以使用次氯酸钠溶液对含有叠氮化钠的溶液进行销毁,反应后溶液碱性明显增强,且产生无色无味的无毒气体,试写出反应的离子方程式____ 。
①打开装置D导管上的旋塞,加热制取氨气。
②加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。

(1)装置B中盛放的药品为
(2)步骤①中先加热通氨气一段时间的目的是
(3)生成NaN3的化学方程式为
(4)产率计算
①称取2.0 g叠氮化钠试样,配成100 mL溶液,并量取10.00 mL溶液于锥形瓶中。
②用滴定管加入0.10 mol·L-1六硝酸铈铵[(NH4)2Ce(NO3)6]溶液40.00 mL[发生的反应为2(NH4)2Ce(NO3)6+2NaN3===4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑](杂质均不参与反应)。
③充分反应后滴入2滴邻菲罗啉指示液,并用0.10 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]为标准液,滴定过量的Ce4+,终点时消耗标准溶液20.00 mL(滴定原理:Ce4++Fe2+=Ce3++Fe3+)。计算可知叠氮化钠的质量分数为
A.锥形瓶使用叠氮化钠溶液润洗
B.滴加六硝酸铈铵溶液时,滴加前仰视读数,滴加后俯视读数
C.滴加硫酸亚铁铵标准溶液时,开始时尖嘴处无气泡,结束时出现气泡
D.滴定过程中,将挂在锥形瓶壁上的硫酸亚铁铵标准液滴用蒸馏水冲进瓶内
(5)叠氮化钠有毒,可以使用次氯酸钠溶液对含有叠氮化钠的溶液进行销毁,反应后溶液碱性明显增强,且产生无色无味的无毒气体,试写出反应的离子方程式
您最近一年使用:0次
3 . 为了探究Cu(NO3)2 的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
Ⅰ.Cu(NO3)2的氧化性
将光亮的铁丝伸入Cu(NO3)2溶液中,一段时间后将铁丝取出。为检验溶液中Fe 的氧化产物,将溶液中的Cu2+除尽后,进行了如下实验。可选用的试剂KSCN 溶液、K3[Fe(CN)6]溶液、氯水。
请完成下表:
Ⅱ.Cu(NO3)2 的热稳定性
在如图所示的实验装置A 中,用酒精喷灯对Cu(NO3)2固体加强热,产生红棕色气体,在装置C中收集到无色气体,经验证为O2。当反应结束以后,试管中残留固体为红色。
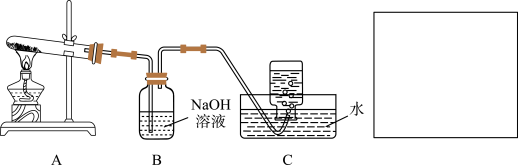
(1)装置B 的作用是_______ 。
(2)从实验安全角度考虑,需要在A、B 间加入装置M,请在方框中画出M 装置。_________
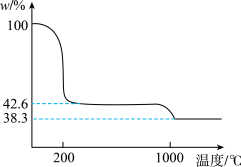
(3)下图为Cu(NO3)2样品高温过程的热重曲线(样品质量分数w%随温度变化的曲线)。Cu(NO3)2加热到200℃的化学方程式为___________ ,继续高温至1000℃生成_______ (填化学式)固体。
 。
。
Ⅰ.Cu(NO3)2的氧化性
将光亮的铁丝伸入Cu(NO3)2溶液中,一段时间后将铁丝取出。为检验溶液中Fe 的氧化产物,将溶液中的Cu2+除尽后,进行了如下实验。可选用的试剂KSCN 溶液、K3[Fe(CN)6]溶液、氯水。
请完成下表:
| 操作 | 反应或现象 | 结论 |
| (1)取少量除尽 Cu2+后的溶液于试管中,加入 | 现象 | 存在 Fe3+ |
| (2)取少量除尽 Cu2+后的溶液于试管中,加入 K3[Fe(CN)6]溶液,振荡 | 离子方程式 | 存在 Fe2+ |
Ⅱ.Cu(NO3)2 的热稳定性
在如图所示的实验装置A 中,用酒精喷灯对Cu(NO3)2固体加强热,产生红棕色气体,在装置C中收集到无色气体,经验证为O2。当反应结束以后,试管中残留固体为红色。

(1)装置B 的作用是
(2)从实验安全角度考虑,需要在A、B 间加入装置M,请在方框中画出M 装置。
(3)下图为Cu(NO3)2样品高温过程的热重曲线(样品质量分数w%随温度变化的曲线)。Cu(NO3)2加热到200℃的化学方程式为
 。
。
您最近一年使用:0次
2019-09-17更新
|
371次组卷
|
3卷引用:四川省成都实验中学2020-2021学年度高2022届高二上学期开学考试化学试题
名校
4 . 草酸亚铁晶体(FeC2O4·2H2O,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究。
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:
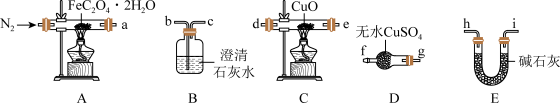
①装置D的名称为______ 。
②按照气流从左到右的方向,上述装置的连接顺序为_____ →尾气处理装置(填仪器接口的字母编号)。
③实验前先通入一段时间N2,其目的为_______ 。
④实验证明了气体产物中含有CO,依据的实验现象为______ 。
(2)固体产物成分的探究。充分反应后,A处反应管中残留黑色固体。查阅资料可知,黑色固体可能为Fe或FeO。小组成员设计实验证明了其成分只有FeO,其操作及现象为___ 。
(3)依据(1)和(2)结论,可知A处反应管中发生反应的化学方程式为____ 。
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液。
步骤2:取上述溶液25.00mL,用c mol·L−1 KMnO4标准液滴定至终点,消耗标准液V1 mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用c mol·L−1 KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤3中加入锌粉的目的为______ 。
(5)草酸亚铁晶体样品的纯度为_____ ;若步骤1配制溶液时部分Fe2+被氧化,则测定结果将______ (填“偏高”、“偏低”或“不变”)。
I.纯净草酸亚铁晶体热分解产物的探究。
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:

①装置D的名称为
②按照气流从左到右的方向,上述装置的连接顺序为
③实验前先通入一段时间N2,其目的为
④实验证明了气体产物中含有CO,依据的实验现象为
(2)固体产物成分的探究。充分反应后,A处反应管中残留黑色固体。查阅资料可知,黑色固体可能为Fe或FeO。小组成员设计实验证明了其成分只有FeO,其操作及现象为
(3)依据(1)和(2)结论,可知A处反应管中发生反应的化学方程式为
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取mg草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液。
步骤2:取上述溶液25.00mL,用c mol·L−1 KMnO4标准液滴定至终点,消耗标准液V1 mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用c mol·L−1 KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤3中加入锌粉的目的为
(5)草酸亚铁晶体样品的纯度为
您最近一年使用:0次
2019-03-26更新
|
1827次组卷
|
9卷引用:四川省泸州市泸县第四中学2020届高三上学期期中考试理综化学试题
名校
解题方法
5 . 铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
【氯化铁】熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
【氯化亚铁】熔点为670℃,易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用下图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:

(1)在装置A中,用KMnO4与浓盐酸反应制取氯气,反应的离子方程式为_________ 。仪器D的名称是__________________ 。
(2)D中装的药品是碱石灰,其作用是__________________________ 。
(3)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。若产物中混有FeCl2,可用下列试剂中的_____ (只能选取一种试剂,填序号)进行检测,实验现象是__________________________________ 。
①H2O2溶液 ②KI-淀粉溶液 ③KSCN溶液 ④酸性KMnO4溶液
(4)定量分析。取装置C中的产物,按以下步骤进行测定:①称取4.60g产品溶于过量的稀盐酸中;②加入足量H2O2溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。则该样品中铁元素的质量分数为_______ %(结果精确到小数点后两位)。
(5)由(4)定量分析数据得出结论,并提出改进措施。
①用题目所给的装置制得的产物中,铁元素含量______ (填“相等”、“偏高”或“偏低”),说明含有FeCl2杂质。
②若要得到较纯净的无水氯化铁,可采取的“装置”改进措施是_________ 。
【氯化铁】熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
【氯化亚铁】熔点为670℃,易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用下图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:

(1)在装置A中,用KMnO4与浓盐酸反应制取氯气,反应的离子方程式为
(2)D中装的药品是碱石灰,其作用是
(3)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。若产物中混有FeCl2,可用下列试剂中的
①H2O2溶液 ②KI-淀粉溶液 ③KSCN溶液 ④酸性KMnO4溶液
(4)定量分析。取装置C中的产物,按以下步骤进行测定:①称取4.60g产品溶于过量的稀盐酸中;②加入足量H2O2溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。则该样品中铁元素的质量分数为
(5)由(4)定量分析数据得出结论,并提出改进措施。
①用题目所给的装置制得的产物中,铁元素含量
②若要得到较纯净的无水氯化铁,可采取的“装置”改进措施是
您最近一年使用:0次
2019-01-07更新
|
667次组卷
|
4卷引用:四川省广安友谊中学2018-2019学年高一上学期期末模拟化学试题
6 . Co(CH3COO)2(乙酸钴)可用作酯交换反应的催化剂并可用于制备高质量锂电池电极。在氮气氛围中,乙酸钴受热分解生成CO、CO2和C2H6等产物。某研究小组利用下列装置检验乙酸钴热分解的部分产物。
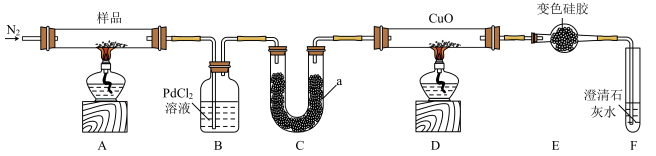
已知:①CO+PdCl2+H2O==CO2+Pd↓(黑色)+2HCl;
②变色硅胶为深蓝色,吸水后变为粉红色。
回答下列问题:
(1)B装置的作用是____ ,要检验乙酸钴分解产物中的CO2,对以上装置的改进方案是______ 。
(2)仪器a中的试剂是_______ ,其作用是_______ 。
(3)能证明乙酸钴的分解产物含有C2H6的实验现象是______ 。
(4)装置D中C2H6被CuO完全氧化的化学方程式是________ 。
(5)另取一定量乙酸钴结晶水合物样品[Co(CH3COO)2·nH2O]在空气中加热,样品的固体残留率(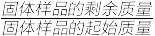 ×100%)随温度的变化如图所示(样品在200 ℃时已完全失去结晶水,350 ℃以上残留固体为金属氧化物)。根据以上实验数据列出残留氧化物CoxOy中x∶y的计算式:
×100%)随温度的变化如图所示(样品在200 ℃时已完全失去结晶水,350 ℃以上残留固体为金属氧化物)。根据以上实验数据列出残留氧化物CoxOy中x∶y的计算式:_____ 。

已知:①CO+PdCl2+H2O==CO2+Pd↓(黑色)+2HCl;
②变色硅胶为深蓝色,吸水后变为粉红色。
回答下列问题:
(1)B装置的作用是
(2)仪器a中的试剂是
(3)能证明乙酸钴的分解产物含有C2H6的实验现象是
(4)装置D中C2H6被CuO完全氧化的化学方程式是
(5)另取一定量乙酸钴结晶水合物样品[Co(CH3COO)2·nH2O]在空气中加热,样品的固体残留率(
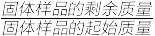 ×100%)随温度的变化如图所示(样品在200 ℃时已完全失去结晶水,350 ℃以上残留固体为金属氧化物)。根据以上实验数据列出残留氧化物CoxOy中x∶y的计算式:
×100%)随温度的变化如图所示(样品在200 ℃时已完全失去结晶水,350 ℃以上残留固体为金属氧化物)。根据以上实验数据列出残留氧化物CoxOy中x∶y的计算式: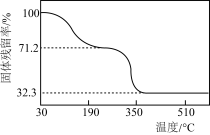
您最近一年使用:0次
7 . 叠氮化钠(NaN3)常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
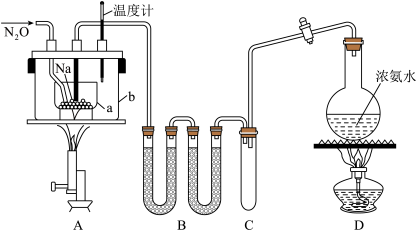
已知:I.NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
II.NaNH2熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)装置B中盛放的药品为_____________ ;装置C的主要作用是______________________ 。
(2)步骤①中先加热通氨气的目的是_____________________________________ ;步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为_______________________________ 。步骤③中最适宜的加热方式为 ___________ (填“水浴加热”,“油浴加热”)。
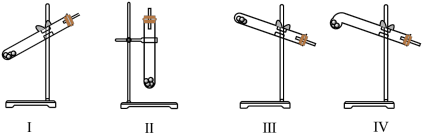
(3)N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则可选择的气体发生装置是(填序号)___________ 。
(4)生成NaN3的化学方程式为_____________________________________ 。
(5)图中仪器a用的是铁质而不用玻璃,其主要原因是__________________ 。
(6)步骤④中用乙醚洗涤的主要目的是_______________________________ 。
(7)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500 g试样配成500.00 mL溶液。②取50.00 mL溶液置于锥形瓶中,加入50.00 mL 0.1010 mol·L-1(NH4)2Ce(NO3)6溶液。③充分反应后,将溶液稍稀释,向溶液中加入8 mL浓硫酸,滴入3滴邻菲啰啉指示液,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为29.00mL。测定过程的反应方程式为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑;Ce4++Fe2+=Ce3++Fe3+;试样中NaN3的质量分数为_______________ 。
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210~220℃,然后通入N2O。
④冷却,向产物中加入乙醇(降低NaN3的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。

已知:I.NaN3是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
II.NaNH2熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)装置B中盛放的药品为
(2)步骤①中先加热通氨气的目的是
(3)N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则可选择的气体发生装置是(填序号)

(4)生成NaN3的化学方程式为
(5)图中仪器a用的是铁质而不用玻璃,其主要原因是
(6)步骤④中用乙醚洗涤的主要目的是
(7)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500 g试样配成500.00 mL溶液。②取50.00 mL溶液置于锥形瓶中,加入50.00 mL 0.1010 mol·L-1(NH4)2Ce(NO3)6溶液。③充分反应后,将溶液稍稀释,向溶液中加入8 mL浓硫酸,滴入3滴邻菲啰啉指示液,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为29.00mL。测定过程的反应方程式为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑;Ce4++Fe2+=Ce3++Fe3+;试样中NaN3的质量分数为
您最近一年使用:0次
2019-03-28更新
|
1086次组卷
|
2卷引用:四川绵阳南山中学高2020届二诊模拟(四)
8 . 铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
【氯化铁】熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
【氯化业铁】熔点为670℃,易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用下图所示的装詈(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:
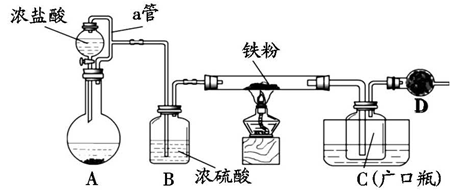
(1)在装置A中,用KMnO4与浓盐酸反应制取氯气,反应的离子方程式为____ 。
(2)仪器D的名称是____ ;D中装的约品是碱石灰,其作用是____ 。
(3)定性分析。取C中的少量产物溶于稀盐酸中配成稀溶液待用。若产物中混有FeCl2,可用下列试剂中的____ (只能选取一种试剂,填序号)进行检测,实验现象是____ 。
①H2O2溶液②K3[Fe(CN)6]溶液③KSCN溶液
④酸性KMnO4溶液⑤KI一淀粉溶液
(4)定量分析。取装置C中的产物,按以下步骤进行测定:①称取4.60g产品溶于过量的稀盐酸中;②加入足量H2O2溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。则该样品中铁元素的质量分数为____ %(结果精确到小数点后两位)。
(5)由(4)定量分析数据得出结论,并提出改进措施:
①用题目所给的装置制得的产物中,铁元素含量____ (填“相等”、“偏高”或“偏低”),说明含有FeCl2杂质。
②若要得到较纯净的无水氯化铁,可采取的“装置”改进措施是____ 。
【氯化铁】熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
【氯化业铁】熔点为670℃,易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用下图所示的装詈(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:

(1)在装置A中,用KMnO4与浓盐酸反应制取氯气,反应的离子方程式为
(2)仪器D的名称是
(3)定性分析。取C中的少量产物溶于稀盐酸中配成稀溶液待用。若产物中混有FeCl2,可用下列试剂中的
①H2O2溶液②K3[Fe(CN)6]溶液③KSCN溶液
④酸性KMnO4溶液⑤KI一淀粉溶液
(4)定量分析。取装置C中的产物,按以下步骤进行测定:①称取4.60g产品溶于过量的稀盐酸中;②加入足量H2O2溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40g。则该样品中铁元素的质量分数为
(5)由(4)定量分析数据得出结论,并提出改进措施:
①用题目所给的装置制得的产物中,铁元素含量
②若要得到较纯净的无水氯化铁,可采取的“装置”改进措施是
您最近一年使用:0次
9 . 富马酸亚铁(C4H2O4Fe)常用于治疗缺铁性贫血,也可作食品营养强化剂,它可由糠醛(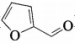 )和硫酸亚铁制备。已知
)和硫酸亚铁制备。已知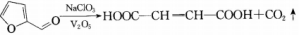 。
。
回答下列问题
I.制备富马酸(实验装置如图所示,夹持装置已略去)
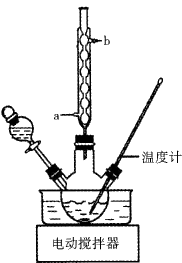
(1)将45.0g氯酸钠、0.2g五氧化二钒置于三颈烧瓶中,加入适量水,滴加糠醛并加热至90~100℃,维持此温度3~4h。实验中冷凝管的作用是_________ ,冷却液宜从___________ (填a”或“b”)处进入。
(2)冰水冷却使其结晶,并通过___________ 操作可以得到富马酸粗品。
(3)再用1mol·L-1HCl溶液重结晶,得到纯富马酸。该操作中用1mol·L-1HCl溶液的原因是_____________ 。
Ⅱ.合成富马酸亚铁
(4)取富马酸溶于适量水中,加入碳酸钠并加热、搅拌,调节pH6.5~6.7,产生大量气泡。写出该反应的化学方程式:___________ 。
(5)将硫酸亚铁溶液和适量的Na2SO3溶液缓慢加入上述反应液中,维持温度100℃并充分搅拌3~4h。
①该操作过程中加入适量的Na2SO3溶液,其目的是___________ 。
②写出生成富马酸亚铁的离子方程式:_____________ 。
(6)过滤、干燥得到产品。
过滤时滤纸要紧贴漏斗内壁,原因是________ 。
Ⅲ.产品纯度测定
(7)取0.300g样品置于250mL锥形瓶中,加入15.00mL硫酸,加热溶解后冷却,再加入50.00mL新沸过的冷水和2滴邻二氮菲指示液,此时溶液呈红色;立即用0.1000mol·L-1硫酸铈(Ⅳ)铵[(NH4)2Ce(SO4)3]标准液滴定(还原产物为Ce3+),滴定终点溶液变为浅蓝色。平行测定三次,平均消耗17.30mL标准液,则样品的纯度为___________ 。
 )和硫酸亚铁制备。已知
)和硫酸亚铁制备。已知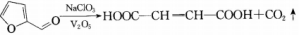 。
。回答下列问题
I.制备富马酸(实验装置如图所示,夹持装置已略去)

(1)将45.0g氯酸钠、0.2g五氧化二钒置于三颈烧瓶中,加入适量水,滴加糠醛并加热至90~100℃,维持此温度3~4h。实验中冷凝管的作用是
(2)冰水冷却使其结晶,并通过
(3)再用1mol·L-1HCl溶液重结晶,得到纯富马酸。该操作中用1mol·L-1HCl溶液的原因是
Ⅱ.合成富马酸亚铁
(4)取富马酸溶于适量水中,加入碳酸钠并加热、搅拌,调节pH6.5~6.7,产生大量气泡。写出该反应的化学方程式:
(5)将硫酸亚铁溶液和适量的Na2SO3溶液缓慢加入上述反应液中,维持温度100℃并充分搅拌3~4h。
①该操作过程中加入适量的Na2SO3溶液,其目的是
②写出生成富马酸亚铁的离子方程式:
(6)过滤、干燥得到产品。
过滤时滤纸要紧贴漏斗内壁,原因是
Ⅲ.产品纯度测定
(7)取0.300g样品置于250mL锥形瓶中,加入15.00mL硫酸,加热溶解后冷却,再加入50.00mL新沸过的冷水和2滴邻二氮菲指示液,此时溶液呈红色;立即用0.1000mol·L-1硫酸铈(Ⅳ)铵[(NH4)2Ce(SO4)3]标准液滴定(还原产物为Ce3+),滴定终点溶液变为浅蓝色。平行测定三次,平均消耗17.30mL标准液,则样品的纯度为
您最近一年使用:0次
2019-01-14更新
|
511次组卷
|
2卷引用:【校级联考】四川省华大新高考联盟2019届高三上学期1月教学质量测评理科综合化学试题
10 . 实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中逐滴加入5mol/L NaOH溶液,所加的NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示,下列说法不正确的是
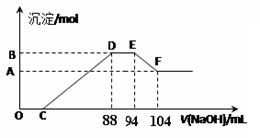

| A.稀硝酸与铝粉、铁粉反应,其还原产物为硝酸铵 |
| B.图中C点对应溶液体积为48mL |
| C.原硝酸溶液中含硝酸的物质的量为0.5mol |
| D.样品中铝粉和铁粉的物质的量之比5:3 |
您最近一年使用:0次
2019-01-30更新
|
143次组卷
|
2卷引用:2016届四川省乐山沫若中学高三上学期12月月考理综化学试卷



