名校
1 . 已知 ,则c为
,则c为
 ,则c为
,则c为| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
2023-03-03更新
|
115次组卷
|
2卷引用:甘肃省张掖市高台县第一中学2022-2023学年高一下学期2月月考化学试题
名校
解题方法
2 . 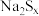 在碱性溶液中可被
在碱性溶液中可被 氧化为
氧化为 ,而
,而 被还原为
被还原为 ,若反应中
,若反应中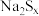 ,与
,与 的物质的量之比为
的物质的量之比为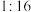 ,则x的值为
,则x的值为
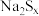 在碱性溶液中可被
在碱性溶液中可被 氧化为
氧化为 ,而
,而 被还原为
被还原为 ,若反应中
,若反应中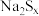 ,与
,与 的物质的量之比为
的物质的量之比为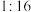 ,则x的值为
,则x的值为| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
2023-02-08更新
|
632次组卷
|
36卷引用:甘肃省张掖市第二中学2020-2021学年高一上学期期中考试化学试题
甘肃省张掖市第二中学2020-2021学年高一上学期期中考试化学试题(已下线)湖南省衡阳市第八中学2010届高三年级第五次月考化学试题(已下线)2012届高三上学期一轮复习化学单元验收试卷(4)(新人教版)(已下线)2012届黑龙江省大庆实验中学高三上学期期中考试化学试卷(已下线)2011-2012学年湖南衡阳一、八中高一下学期期中联考化学试卷(已下线)2013届河北省邯郸一中高三9月月考化学化学试卷(已下线)2014届浙江省湖州市八校高三上学期第二次联考化学试卷福建省德化一中、永安一中、漳平一中2018届高三上学期三校联考化学试题黑龙江省齐齐哈尔市实验中学2017-2018学年高一上学期期中考试化学试题安徽省六安市霍邱县第二中学2019-2020学年高一上学期段考化学试题辽宁省辽河油田第二高级中学2020届高三12月考试化学试题2019年秋高三化学复习强化练习—— 氧化还原反应(强化练)2020届高三化学二轮复习 氧化还原反应过关检测(强化训练)湖南省岳阳市岳阳楼区岳阳楼市第一中学2020届高三考前模拟理科综合化学试题(已下线)【南昌新东方】2019 南昌五中 高一上期中辽宁省丹东市2020届高三总复习阶段测试化学试题黑龙江省哈尔滨市三中2020届高三第二次月考化学试题辽宁省东北育才学校科学高中部2020-2021学年高一上学期第一学段检测化学试题河南省周口市中英文学校2020-2021学年高三上学期第一次月考化学试题山西省临汾市县底中学校2020-2021学年高三上学期开学考试化学试题山东省济南市历城第一中学2021届高三上学期10月月考化学试题吉林省松原市乾安七中2020-2021学年高二下学期第七次质量检测化学试题(已下线)专题05 氧化还原反应 (热点讲义)-2022届高考化学一轮复习热点题型归纳与变式训练山西省运城市稷山中学2022届高三上学期月考(一)化学试题河北省沧州市第一中学2020-2021学年高一下学期开学测试化学试题陕西省韩城市西庄中学2021-2022学年高三上学期9月月考化学试题江苏省常州市第一中学2021-2022学年高一上学期期中考试化学试题四川省成都市树德中学2021-2022学年高一上学期11月阶段性测试(期中)化学试题重庆市南开中学校2021-2022学年高一上学期阶段性测试化学试题重庆市璧山中学校2021-2022学年高一上学期期中考试化学试题吉林省吉林市第一中学2021-2022学年高二6月月考(平行班)化学试题陕西省宝鸡市千阳县千阳中学2020-2021学年高一上学期期中考试化学试题湖北省武汉中学2022-2023学年高一上学期期中阶段性考试化学试题第一章 化学物质及其变化 第5讲 氧化还原反应的计算与方程式的配平(已下线)题型18 氧化还原反应规律的应用(已下线)专题05 氧化还原反应方程式的配平与计算(一题多问)
3 . 氧化剂和还原剂在生产生活中应用非常广泛。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝石(KNO3)、木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。在该反应中,氧化剂是_______ ,还原剂是_______ ,氧化产物是_______ ,还原产物是_______ 。
(2)水是生命之源,在常温常压下为无色无味液体,作为一种化学物质,水也会参与很多化学反应,如:
①2Na+2H2O=2NaOH+H2↑
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2H2O=2H2↑+O2↑
以上反应中,H2O只作氧化剂的是_______ ;H2O只作还原剂的是_______ ;H2O既作氧化剂,又作还原剂的是_______ ;H2O既不作氧化剂,又不作还原剂的是_______ 。
(3)高锰酸钾和浓盐酸可以发生如下反应制备氯气(Cl2):2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①已知KMnO4和MnCl2皆属于可溶盐,写出该反应的离子方程式_______ ;
②抄写化学方程式,用单线桥法标出电子转移的方向和数目_______ ;
③其中,氧化剂和还原剂的个数比为_______ 。
④在酸性溶液中,氧化性:KMnO4_______ Cl2(填大于或小于)。
(4)次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2的化学方程式:_______ 。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝石(KNO3)、木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。在该反应中,氧化剂是
(2)水是生命之源,在常温常压下为无色无味液体,作为一种化学物质,水也会参与很多化学反应,如:
①2Na+2H2O=2NaOH+H2↑
②3NO2+H2O=2HNO3+NO
③2F2+2H2O=4HF+O2
④2H2O=2H2↑+O2↑
以上反应中,H2O只作氧化剂的是
(3)高锰酸钾和浓盐酸可以发生如下反应制备氯气(Cl2):2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①已知KMnO4和MnCl2皆属于可溶盐,写出该反应的离子方程式
②抄写化学方程式,用单线桥法标出电子转移的方向和数目
③其中,氧化剂和还原剂的个数比为
④在酸性溶液中,氧化性:KMnO4
(4)次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2的化学方程式:
您最近一年使用:0次
4 . 家庭用的洗涤去污剂有下列几种,其含有的有效成分如下:
(1)管道疏通剂可用于疏通管道中因毛发、残渣等造成的堵塞,使用时会产生大量气泡,且要防止明火,以免发生爆炸,则疏通时反应的离子方程式为___________ ,在该反应中每生成1mol气体,被还原的物质的质量为___________ g.也不能与“洁厕灵”混合使用,降低疏通效果,其原因是___________ 。
(2)洁厕灵与84消毒液混合使用会产生黄绿色的有毒气体,易造成危险,反应的离子方程式为___________ 。
(3)彩漂剂使用时会释放出一种无色无味的气体,使污垢活化,易于洗涤。但是不能长期存放,会降低彩漂效果,则发生的反应的还原产物为___________ (写化学式)。
(4)某兴趣小组做如下探究实验,请回答下列问题:
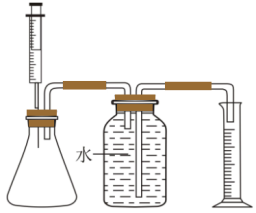
①如图组装实验装置,并___________ ;
②向锥形瓶加入10mL的84消毒液,注射器中吸入10mL的彩漂剂,
③将注射器中的彩漂剂慢慢注入锥形瓶中,产生无色无味的气体,发生的化学方程式为___________ 。
④直至不再产生气泡。
| 示例 |  |  |  |  |
| 名称 | 管道疏通剂 | 洁厕灵 | 彩漂剂 | 84消毒液 |
| 有效成分 | 氢氧化物和铝粉 | 浓盐酸 | 双氧水 | NaClO溶液 |
| 用途 | 清理管道污垢,防堵塞 | 清理马桶污垢,除异味 | 漂洗衣物,使色彩鲜艳 | 消毒漂白 |
(2)洁厕灵与84消毒液混合使用会产生黄绿色的有毒气体,易造成危险,反应的离子方程式为
(3)彩漂剂使用时会释放出一种无色无味的气体,使污垢活化,易于洗涤。但是不能长期存放,会降低彩漂效果,则发生的反应的还原产物为
(4)某兴趣小组做如下探究实验,请回答下列问题:

①如图组装实验装置,并
②向锥形瓶加入10mL的84消毒液,注射器中吸入10mL的彩漂剂,
③将注射器中的彩漂剂慢慢注入锥形瓶中,产生无色无味的气体,发生的化学方程式为
④直至不再产生气泡。
您最近一年使用:0次
名校
解题方法
5 . 刚玉在工业上有广泛的用途,其主要成分为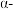 氧化铝。利用铝灰(主要成分为
氧化铝。利用铝灰(主要成分为 ,含少量杂质
,含少量杂质 、
、 、
、 )制备刚玉的工艺流程如下:
)制备刚玉的工艺流程如下:
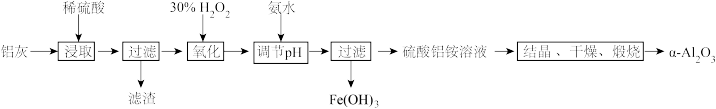
已知: 是酸性氧化物,且不与水反应。
是酸性氧化物,且不与水反应。
回答下列问题:
(1)滤渣的主要成分是_______ (填化学式);过滤时用到的玻璃仪器有漏斗、烧杯和_______ 。
(2)“氧化”操作的目的为_______ ,该过程中发生反应的离子方程式为_______ 。
(3)已知:生成氢氧化物沉淀的 如下表所示。
如下表所示。
用氨水“调节 ”,
”, 的范围是
的范围是_______ 。
(4)写出用氨水调节 生成
生成 沉淀的离子方程式:
沉淀的离子方程式:_______ 。
 氧化铝。利用铝灰(主要成分为
氧化铝。利用铝灰(主要成分为 ,含少量杂质
,含少量杂质 、
、 、
、 )制备刚玉的工艺流程如下:
)制备刚玉的工艺流程如下:
已知:
 是酸性氧化物,且不与水反应。
是酸性氧化物,且不与水反应。回答下列问题:
(1)滤渣的主要成分是
(2)“氧化”操作的目的为
(3)已知:生成氢氧化物沉淀的
 如下表所示。
如下表所示。| 氢氧化物 |  |  |  |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
 ”,
”, 的范围是
的范围是(4)写出用氨水调节
 生成
生成 沉淀的离子方程式:
沉淀的离子方程式:
您最近一年使用:0次
2022-12-18更新
|
121次组卷
|
2卷引用:甘肃省武威市天祝一中、古浪一中、民勤一中联考2022-2023学年高一下学期3月月考化学试题
名校
6 . 亚硝酸( )是一种不稳定的酸,易分解为
)是一种不稳定的酸,易分解为 和
和 。亚硝酸钠是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质,常用作漂白剂、媒染剂。回答下列问题:
。亚硝酸钠是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质,常用作漂白剂、媒染剂。回答下列问题:
(1)亚硝酸钠会与人体中的血红蛋白作用,将二价铁氧化为三价铁,使血红蛋白丧失输送氧气的功能而使人体中毒。一旦发生亚硝酸盐中毒,应立即注射美蓝溶液进行治疗,据此可推断美蓝溶液具有___________ (填“氧化”或“还原”)性。
(2)亚硝酸钠外观极像食盐,且和食盐一样有咸味。工业上常用下列两种方法检验食盐中是否混有亚硝酸钠。
①取样品,加稀硫酸,若观察到___________ (填现象),则说明样品中含有亚硝酸钠。
②取样品,加___________ (填试剂名称),酸化后溶液变蓝,则说明样品中含有亚硝酸钠。
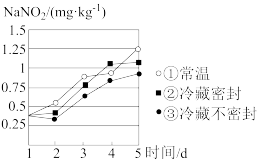
(3)研究不同条件下保存萝卜,得到萝卜中亚硝酸钠含量随时间变化的关系如图所示,若要保证在亚硝酸钠含量低于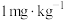 时食用,则三种条件下保存时间由长到短的顺序是
时食用,则三种条件下保存时间由长到短的顺序是___________ (填序号)。
(4)鱼塘中亚硝酸钠浓度过高,会导致鱼不吃食甚至死亡。可用适量二氧化氯( )处理亚硝酸钠,
)处理亚硝酸钠, 被还原为
被还原为 ,反应的离子方程式为
,反应的离子方程式为___________ ;若有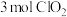 参与反应,则转移的电子数是
参与反应,则转移的电子数是___________ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
 )是一种不稳定的酸,易分解为
)是一种不稳定的酸,易分解为 和
和 。亚硝酸钠是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质,常用作漂白剂、媒染剂。回答下列问题:
。亚硝酸钠是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质,常用作漂白剂、媒染剂。回答下列问题:(1)亚硝酸钠会与人体中的血红蛋白作用,将二价铁氧化为三价铁,使血红蛋白丧失输送氧气的功能而使人体中毒。一旦发生亚硝酸盐中毒,应立即注射美蓝溶液进行治疗,据此可推断美蓝溶液具有
(2)亚硝酸钠外观极像食盐,且和食盐一样有咸味。工业上常用下列两种方法检验食盐中是否混有亚硝酸钠。
①取样品,加稀硫酸,若观察到
②取样品,加
(3)研究不同条件下保存萝卜,得到萝卜中亚硝酸钠含量随时间变化的关系如图所示,若要保证在亚硝酸钠含量低于
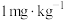 时食用,则三种条件下保存时间由长到短的顺序是
时食用,则三种条件下保存时间由长到短的顺序是
(4)鱼塘中亚硝酸钠浓度过高,会导致鱼不吃食甚至死亡。可用适量二氧化氯(
 )处理亚硝酸钠,
)处理亚硝酸钠, 被还原为
被还原为 ,反应的离子方程式为
,反应的离子方程式为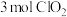 参与反应,则转移的电子数是
参与反应,则转移的电子数是 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
名校
解题方法
7 . 黄色固体X是由四种元素组成的化合物,用作颜料和食品的抗结剂,为测定其组成,进行如下实验。已知气体D能使澄清石灰水变浑浊,溶液F中只含有一种溶质。回答下列问题:
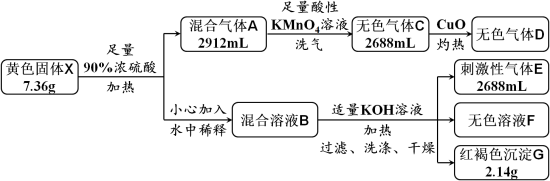
(1)固体X的组成元素是_______ 。
(2)混合气体A中所含物质的化学式为_______ 。
(3)实验中溶液B由X转化而来的溶质与KOH反应的总离子方程式为_______ 。
(4)证明沉淀G中的金属元素已完全沉淀的方法是_______ 。
(5)X与酸性KMnO4溶液反应,可生成一种与X组成元素相同,但式量比其小39的化合物,该反应的化学方程式为_______ 。

(1)固体X的组成元素是
(2)混合气体A中所含物质的化学式为
(3)实验中溶液B由X转化而来的溶质与KOH反应的总离子方程式为
(4)证明沉淀G中的金属元素已完全沉淀的方法是
(5)X与酸性KMnO4溶液反应,可生成一种与X组成元素相同,但式量比其小39的化合物,该反应的化学方程式为
您最近一年使用:0次
2022-12-09更新
|
417次组卷
|
4卷引用:甘肃省两县高中联考2023-2024学年高三上学期12月月考化学试题
甘肃省两县高中联考2023-2024学年高三上学期12月月考化学试题浙江省诸暨海亮高级中学2021-2022学年高三12月份选考模拟化学试题浙江省舟山中学2022-2023学年高三上学期首考模拟卷(三)化学试题(已下线)浙江省温州市普通高中2023届高三下学期第二次适应性考试化学试题变式题(无机推断题)
8 . Ⅰ.化学反应速率和化学平衡影响因素较多,经常采用变量控制思想分析问题。某小组利用 溶液和酸性
溶液和酸性 溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:
溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:
请回答:
(1)已知 酸性溶液与
酸性溶液与 溶液反应有
溶液反应有 生成,用化学方程式表示该实验的实验原理:
生成,用化学方程式表示该实验的实验原理:___________ 。
(2)根据表中的实验数据,可以得到的结论是___________ 。
(3)利用实验3中数据计算,用 溶液的浓度变化表示的反应速率为
溶液的浓度变化表示的反应速率为
___________ 。
Ⅱ.研究 的综合利用对促进“低碳经济”的发展有重要意义。工业上以
的综合利用对促进“低碳经济”的发展有重要意义。工业上以 、,为原料生产尿素
、,为原料生产尿素 ,
,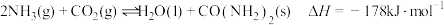 ,
,
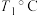 时,在1L的密闭容器中充入
时,在1L的密闭容器中充入 和模拟工业生产,
和模拟工业生产, ,图中是
,图中是 平衡转化率
平衡转化率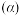 与
与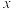 的关系。
的关系。
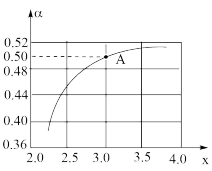
(4)图中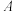 点
点 的平衡转化率
的平衡转化率
___________ %(结果保留3位有效数字)。
(5)当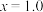 时,若起始的压强为
时,若起始的压强为 ,水为液态平衡时压强变为起始的
,水为液态平衡时压强变为起始的 ,则该反应的平衡常数
,则该反应的平衡常数 =
=___________ ( 为以分压表示的平衡常数,分压=总压
为以分压表示的平衡常数,分压=总压 体积分数)。
体积分数)。
 溶液和酸性
溶液和酸性 溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:
溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
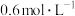  溶液 溶液 |  |   溶液 溶液 |  稀硫酸 稀硫酸 | ||
| 1 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
请回答:
(1)已知
 酸性溶液与
酸性溶液与 溶液反应有
溶液反应有 生成,用化学方程式表示该实验的实验原理:
生成,用化学方程式表示该实验的实验原理:(2)根据表中的实验数据,可以得到的结论是
(3)利用实验3中数据计算,用
 溶液的浓度变化表示的反应速率为
溶液的浓度变化表示的反应速率为
Ⅱ.研究
 的综合利用对促进“低碳经济”的发展有重要意义。工业上以
的综合利用对促进“低碳经济”的发展有重要意义。工业上以 、,为原料生产尿素
、,为原料生产尿素 ,
,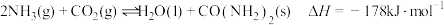 ,
,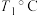 时,在1L的密闭容器中充入
时,在1L的密闭容器中充入 和模拟工业生产,
和模拟工业生产, ,图中是
,图中是 平衡转化率
平衡转化率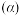 与
与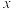 的关系。
的关系。
(4)图中
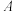 点
点 的平衡转化率
的平衡转化率
(5)当
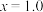 时,若起始的压强为
时,若起始的压强为 ,水为液态平衡时压强变为起始的
,水为液态平衡时压强变为起始的 ,则该反应的平衡常数
,则该反应的平衡常数 =
= 为以分压表示的平衡常数,分压=总压
为以分压表示的平衡常数,分压=总压 体积分数)。
体积分数)。
您最近一年使用:0次
解题方法
9 . 某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如表:(不考虑溶液混合所引起的体积变化)
(1)通过实验A、B,可探究出浓度的改变对反应速率的影响,其中V1=____ ;通过实验____ (填实验序号)可探究出温度变化对化学反应速率的影响。
(2)C组实验中溶液褪色时间t1____ (填“>”或“<”)8。
(3)写出相应反应的离子方程式:____ 。
| 实验序号 | 实验温度/K | 物质 | 溶液颜色褪至无色时所需时间/s | ||||
| KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | 6 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | 3 | 0.1 | 1 | t1 |
(2)C组实验中溶液褪色时间t1
(3)写出相应反应的离子方程式:
您最近一年使用:0次
名校
解题方法
10 . 完成以下填空:
(1)写出下列反应的离子方程式
①过氧化钠与水反应的离子方程式:_______ ;
②制取漂白液(“84”消毒液)的离子方程式为_______ 。
(2)配平下列化学方程式:
①
______
②
______
(3)某无色透明溶液中可能大量存在 、
、 、
、 、
、 、
、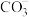 、
、 、
、 、
、 中的几种,用化学方法进行了定性鉴定。请填写下列空白:
中的几种,用化学方法进行了定性鉴定。请填写下列空白:
①不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
②取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是_______ ,有关的离子方程式为_______ 。
③取②中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有_______ ,此过程中涉及到的离子方程式有_______ 。
④通过以上定性实验可知,溶液中除了①中不存在的离子外,肯定不存在的离子还有 、
、_______ ,可能存在的离子是_______ ,为确定其是否存在,还需要进行的操作是_______ 。
(1)写出下列反应的离子方程式
①过氧化钠与水反应的离子方程式:
②制取漂白液(“84”消毒液)的离子方程式为
(2)配平下列化学方程式:
①

②

(3)某无色透明溶液中可能大量存在
 、
、 、
、 、
、 、
、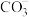 、
、 、
、 、
、 中的几种,用化学方法进行了定性鉴定。请填写下列空白:
中的几种,用化学方法进行了定性鉴定。请填写下列空白:①不做任何实验就可以肯定原溶液中不存在的离子是
②取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
③取②中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有
④通过以上定性实验可知,溶液中除了①中不存在的离子外,肯定不存在的离子还有
 、
、
您最近一年使用:0次



