1 . 如图为实验室制取纯净、干燥的Cl2,并用Cl2与铜反应。
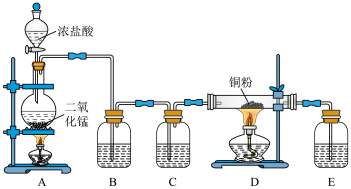
试回答下列问题:
(1)写出A中反应的离子方程式___________ 。
(2)反应中浓盐酸显示出来的性质是___________。
(3)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,C瓶中加入___________ 试剂。(填试剂名称)
(4)装置E的作用是___________ ;E处发生反应的离子方程式为___________ 。

试回答下列问题:
(1)写出A中反应的离子方程式
(2)反应中浓盐酸显示出来的性质是___________。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
(3)为得到干燥纯净的氯气,一般在B瓶中加入饱和食盐水,C瓶中加入
(4)装置E的作用是
您最近半年使用:0次
解题方法
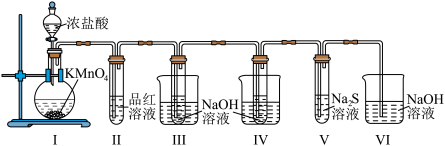
2 . 按如图装置进行实验,将浓盐酸滴入Ⅰ中的圆底烧瓶中(已知: 和
和 溶液在加热条件下会生成
溶液在加热条件下会生成 ),下列说法不正确的是
),下列说法不正确的是
 和
和 溶液在加热条件下会生成
溶液在加热条件下会生成 ),下列说法不正确的是
),下列说法不正确的是
| A.Ⅰ中圆底烧瓶内的反应,体现了盐酸的酸性和还原性 |
| B.Ⅱ试管内的红色褪去后,再加热又恢复原来的红色 |
| C.Ⅲ和Ⅳ试管分别进行冷水浴和热水浴,反应的还原产物相同 |
D.Ⅴ试管内出现浑浊,氧化性: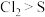 |
您最近半年使用:0次
名校
解题方法
3 . 下图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸。向 晶体滴加浓盐酸后,立即用另一培养皿扣在上面。
晶体滴加浓盐酸后,立即用另一培养皿扣在上面。
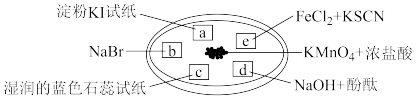
能全面解释实验现象且正确的是
 晶体滴加浓盐酸后,立即用另一培养皿扣在上面。
晶体滴加浓盐酸后,立即用另一培养皿扣在上面。
能全面解释实验现象且正确的是
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性: |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-09-10更新
|
618次组卷
|
6卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高一上学期1月期末考试化学试题
4 . 氯气与碱溶液反应,在低温和稀碱溶液中主要产物是ClO-和Cl-,在75℃以上和浓碱溶液中主要产物是ClO 和Cl-。研究小组用如科实验装置(部分夹持装置略去)制取氯酸钾(KClO3),并测定其纯度。
和Cl-。研究小组用如科实验装置(部分夹持装置略去)制取氯酸钾(KClO3),并测定其纯度。
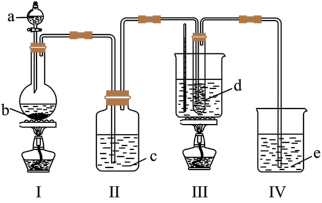
a为浓盐酸,b为MnO2,c为饱和食盐水,d为30%KOH溶液,e为NaOH溶液
回答下列问题:
(1)检查装置气密性后,添加药品,待装置Ⅲ水温升至75℃开始反应。从装置Ⅲ的试管中分离得到KClO3粗产品,其中混有的杂质除KOH外还有___ 和___ 。
(2)已知碱性条件下,ClO-有强氧化性。设计实验证明“碱性条件下,H2O2能够被ClO-氧化”:___ 。
(必须选择的试剂和药品有:次氯酸钠溶液,H2O2溶液,NaOH溶液,木条。请写出实验操作及现象)。
(3)已知碱性条件下,ClO3-氧化性较弱,不能氧化H2O2。为测定产品KClO3的纯度,进行如下实验:
步骤1:取2.45g样品溶于水配成250mL溶液。
步骤2:取25.00mL溶液于锥形瓶中,调至pH=10,滴加足量H2O2溶液充分反应,然后煮沸溶液1~2分钟,冷却。
步骤3:加入过量KI溶液,再逐滴加入足量稀硫酸。(发生的反应为:ClO +I-+H+—Cl-+I2+H2O未配平)
+I-+H+—Cl-+I2+H2O未配平)
步骤4:加入指示剂,用0.5000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。(2S2O +I2=S4O
+I2=S4O +2I-)
+2I-)
①步骤2中如果不进行煮沸所测定的KClO3纯度___ (填偏高、偏低或无影响)。
②样品中KClO3的质量分数为___ 。(KClO3相对分子质量:122.5)写出计算过程。
 和Cl-。研究小组用如科实验装置(部分夹持装置略去)制取氯酸钾(KClO3),并测定其纯度。
和Cl-。研究小组用如科实验装置(部分夹持装置略去)制取氯酸钾(KClO3),并测定其纯度。
a为浓盐酸,b为MnO2,c为饱和食盐水,d为30%KOH溶液,e为NaOH溶液
回答下列问题:
(1)检查装置气密性后,添加药品,待装置Ⅲ水温升至75℃开始反应。从装置Ⅲ的试管中分离得到KClO3粗产品,其中混有的杂质除KOH外还有
(2)已知碱性条件下,ClO-有强氧化性。设计实验证明“碱性条件下,H2O2能够被ClO-氧化”:
(必须选择的试剂和药品有:次氯酸钠溶液,H2O2溶液,NaOH溶液,木条。请写出实验操作及现象)。
(3)已知碱性条件下,ClO3-氧化性较弱,不能氧化H2O2。为测定产品KClO3的纯度,进行如下实验:
步骤1:取2.45g样品溶于水配成250mL溶液。
步骤2:取25.00mL溶液于锥形瓶中,调至pH=10,滴加足量H2O2溶液充分反应,然后煮沸溶液1~2分钟,冷却。
步骤3:加入过量KI溶液,再逐滴加入足量稀硫酸。(发生的反应为:ClO
 +I-+H+—Cl-+I2+H2O未配平)
+I-+H+—Cl-+I2+H2O未配平)步骤4:加入指示剂,用0.5000mol·L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。(2S2O
 +I2=S4O
+I2=S4O +2I-)
+2I-)①步骤2中如果不进行煮沸所测定的KClO3纯度
②样品中KClO3的质量分数为
您最近半年使用:0次
名校
解题方法
5 . 实验小组同学制备KClO3并探究其性质,过程如下:

下列说法不正确 的是

下列说法
| A.可用饱和NaOH溶液净化氯气 |
B.生成KClO3的离子方程式为3Cl2+6OH- ClO ClO +5Cl-+3H2O +5Cl-+3H2O |
| C.推测若取无色溶液a于试管中,滴加稀H2SO4后再加入少量CCl4,下层液体变紫色 |
| D.上述实验说明碱性条件下氧化性:Cl2>KClO3,酸性条件下氧化性:Cl2<KClO3 |
您最近半年使用:0次
名校
6 . 氯气是一种重要的化工原料,在生产生活中具有广泛的应用。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式_______ 。若产生标准状况下4.48 LCl2,则反应过程中被氧化的HCl的物质的量是_______ mol。
②为了防止氯气污染环境,需将剩余氯气通入_______ ,发生的化学反应方程式_______ 。
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下: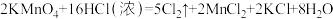 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是_______ (填写字母)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式_______ 。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式
②为了防止氯气污染环境,需将剩余氯气通入
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
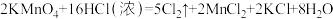 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式
您最近半年使用:0次
解题方法
7 . 实验室要制取一瓶纯净干燥的氯气。现有如图所示仪器和药品可供使用:

(1)实验室制取氯气的原理:
其中HCl所表现的性质是
(2)接上述仪器的正确顺序是 。
| A.ABCEFGHD | B.ABCFEGHD | C.AFEBCGHD | D.AFEBCHGD |
A.除去氯气中的水蒸气 B.除去氯气中的氯化氢
C.尾气吸收 D.收集氯气
您最近半年使用:0次
2022-12-07更新
|
328次组卷
|
2卷引用:黑龙江省海林林业局第一中学2021-2022学年高一上学期第二次月考化学试题
名校
解题方法
8 . 下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向 晶体上滴加一滴浓盐酸后,立即把另一培养皿扣在上面。
晶体上滴加一滴浓盐酸后,立即把另一培养皿扣在上面。
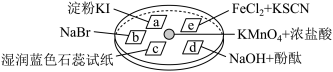
已知: (浓)
(浓)
对实验现象的解释或结论正确的是
 晶体上滴加一滴浓盐酸后,立即把另一培养皿扣在上面。
晶体上滴加一滴浓盐酸后,立即把另一培养皿扣在上面。
已知:
 (浓)
(浓)
对实验现象的解释或结论正确的是
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性: |
| B | c处先变红,后褪色 | 氯气与水反应生成了酸性物质 |
| C | d处立即褪色 | 氯气与水反应生成了漂白性物质 |
| D | e处变红色 |  有还原性 有还原性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-10-09更新
|
319次组卷
|
2卷引用:北京市海淀实验中学2022-2023学年高三上学期10月学科展示化学试题
名校
解题方法
9 . 氯气在工业生产中有重要的用途。某课外活动小组利用下列化学反应在实验室中制备氯气,并进行有关氯气性质的研究。
(1)该小组同学欲用如图1所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。
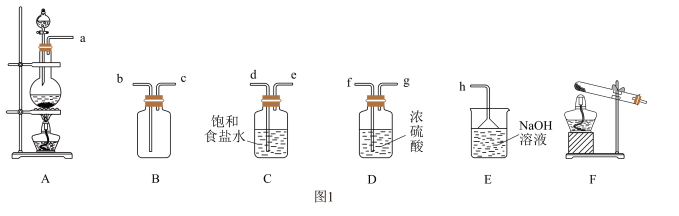
①写出实验室制氯气的化学反应方程式:______ ;浓盐酸起酸性作用和还原剂作用的物质的量之比为______ 。
②选择装置,将各仪器按先后顺序连接起来,应该是a接______ 、______ 接______ 、______ 接______ 、______ 接 。(用导管口处的字母表示)
。(用导管口处的字母表示)
(2)E装置吸收氯气,可得漂白液的有效成分:______ (填化学式);若将氯气通入冷的石灰乳中,可得漂白粉,写出反应方程式:______ 。
(3)该小组同学设计并分别利用图2和图3所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。
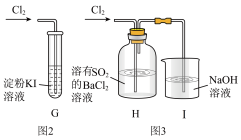
①G中溶液变蓝,原因是______ (用离子方程式表示)。
②H中的现象是______ 。
(1)该小组同学欲用如图1所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。

①写出实验室制氯气的化学反应方程式:
②选择装置,将各仪器按先后顺序连接起来,应该是a接
 。(用导管口处的字母表示)
。(用导管口处的字母表示)(2)E装置吸收氯气,可得漂白液的有效成分:
(3)该小组同学设计并分别利用图2和图3所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。

①G中溶液变蓝,原因是
②H中的现象是
您最近半年使用:0次
10 . 下图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸。向 晶体滴加浓盐酸后,立即用另一培养皿扣在上面。已知:
晶体滴加浓盐酸后,立即用另一培养皿扣在上面。已知: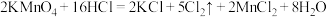 、
、 、
、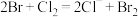 (溴单质为深红棕色)
(溴单质为深红棕色)

能全面解释实验现象且正确的是
 晶体滴加浓盐酸后,立即用另一培养皿扣在上面。已知:
晶体滴加浓盐酸后,立即用另一培养皿扣在上面。已知: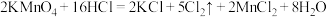 、
、 、
、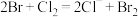 (溴单质为深红棕色)
(溴单质为深红棕色)
能全面解释实验现象且正确的是
| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性: |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变红色 | 还原性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-03-18更新
|
1329次组卷
|
51卷引用:2012年上海市高考化学试题
2012年上海市高考化学试题(已下线)2013-2014学年浙江省宁波市八校高一上学期期末联考化学试卷(已下线)2014高考化学专题突破训练 专题10非金属及其化合物练习卷(已下线)2014高考名师推荐化学氯、溴、碘及其化合物主要性质(已下线)2013-2014学年浙江省杭州地区六校高二下学期期中联考化学试卷(已下线)2013-2014河北省石家庄一中上学期开学考试高二化学试卷(已下线)2015届湖南省长沙市长郡中学高三第一次月考化学试卷2015届辽宁省抚顺市二中高三上学期期中考试化学试卷2014-2015河北唐山市一中高一下学期开学调研考试化学试卷2015-2016学年黑龙江省大庆铁人中学高一上期末化学试卷2015-2016学年湖南省长沙市望城一中高一上期末化学试卷河南省南阳市2016-2017学年高一上学期期终质量评估化学试题2016-2017学年江西省南昌市第二中学高一上学期期末考试化学试卷河北省涞水波峰中学2018届高三第一次调研考试化学试题甘肃省兰州市第一中学2018届高三8月月考化学试题天津市和平区2017-2018学年高一上学期期末考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氯及其化合物【押题专练】辽宁省阜新市海州高级中学2019届高三上学期第一次月考化学试题河北省承德市第一中学2018-2019学年高一上学期第三次月考化学试题黑龙江省大庆市铁人中学2018-2019学年高一下学期开学考试化学试题陕西省榆林市第二中学2018-2019学年高二下学期期中考试化学试题2019届上海奉贤区高考第一次模拟化学试题陕西省西安电子科技大学附属中学2019-2020学年高一上学期期末考试化学试题2020届上海市奉贤区高考化学一模试卷(已下线)【南昌新东方】师大附中2019-2020 高一(上) 期末安徽省肥东县第二中学2019-2020学年高一下学期期中考试(共建班)化学试题河南省信阳市罗山县2021届高三第一次调研(8月联考)化学试题江西省奉新县第一中学2021届高三上学期第一次月考化学试题内蒙古自治区呼和浩特市和林格尔县第一中学2018-2019学年高二上学期第一次月考化学试题人教版(2019)高一必修第一册 第二章 海水中的重要元素 第二节 氯及其化合物 教材帮江西省上饶市横峰中学2021届高三上学期第一次月考化学试题宁夏青铜峡市高级中学2021届高三上学期期中考试化学试题黑龙江伊春林业管理局第二中学2021届高三上学期期中考试化学试题(已下线)第12讲 富集在海水中的元素——卤素(精讲)-2022年一轮复习讲练测(已下线)考点09 氯及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点09 氯及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)内蒙古自治区包钢第一中学2021-2022学年高三上学期10月月考化学试题浙江省绍兴市第一中学2016-2017学年高一下学期期末考试化学试题宁夏青铜峡市高级中学2021-2022学年高三上学期11月测试化学试题浙江省宁波中学2021-2022学年高一上学期期中考试化学试题(已下线)考点09 氯及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第12讲 富集在海水中的元素——卤素(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第05练 氯及其化合物-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第05练 氯及其化合物-2023年高考化学一轮复习小题多维练(全国通用)天津市红桥区2019-2020学年高一上学期期末考试化学试题(已下线)2.2.2 氯气与金属、非金属及还原性化合物的反应-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)黑龙江省佳木斯市第十二中学2022-2023学年高三上学期期中考试化学试题福建省龙岩第一中学2022-2023学年高一上学期第二次月考化学试题江西省景德镇一中2022-2023学年高一上学期期中(18班)化学试题.广东省广州市第八十六中学2022-2023学年高一上学期期中考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第二单元03巩固练



