解题方法
1 . 某样品溶液中可能含有硫酸铜、硫酸铁、和稀硫酸中的一种或多种,现分别取少许该样品溶液进行如下实验,通过观察现象得出相应结论,这些结论中不正确的是
| A.向样品溶液中逐渐加入少量锌粉,开始时未见产生气泡,样品溶液中一定不存在稀硫酸 |
| B.向样品溶液中加入一定质量的铁粉后,充分反应后,有残余固体且质量比原加入的铁粉多,样品溶液中一定含有硫酸铜 |
| C.向样品溶液中加入铜片,铜片溶解,溶液中一定含有硫酸铁 |
| D.向样品溶液中逐滴滴入氢氧化钠,当滴入一定量后才观察到有浑浊现象,则样品溶液中一定含有稀硫酸 |
您最近一年使用:0次
2 . 胆矾(CuSO4·5H2O)是铜的重要化合物,有着广泛的应用,如用来配制农药波尔多液。以下是CuSO4·5H2O的实验室制备流程图。

根据题意完成下列填空:
(1)向含有铜粉的稀硫酸中滴加硝酸,在铜粉溶解时最终可以观察到的实验现象:_____________ 、______________ 。
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是_________ (填化学式)。
(3)将CuSO4·5H2O与NaHCO3按一定的比例共同投入到150mL沸水中,剧烈搅拌,冷却后,有绿色晶体析出。该晶体的化学组成为Cux (OH) y (CO3) z·nH2O。实验所得的绿色晶体需充分洗涤,检验是否洗涤干净的方法是_______________ 。
(4)为了确定晶体的化学式,某实验小组进行如下实验:a.称取3.640g晶体,加入足量的稀盐酸使固体完全溶解,收集到标准状况下的气体448.0 mL;b.称取等质量的晶体,灼烧至完全分解,得到2.400g残余固体。通过计算确定晶体的化学式(写出计算过程)。

根据题意完成下列填空:
(1)向含有铜粉的稀硫酸中滴加硝酸,在铜粉溶解时最终可以观察到的实验现象:
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4·5H2O中可能存在的杂质是
(3)将CuSO4·5H2O与NaHCO3按一定的比例共同投入到150mL沸水中,剧烈搅拌,冷却后,有绿色晶体析出。该晶体的化学组成为Cux (OH) y (CO3) z·nH2O。实验所得的绿色晶体需充分洗涤,检验是否洗涤干净的方法是
(4)为了确定晶体的化学式,某实验小组进行如下实验:a.称取3.640g晶体,加入足量的稀盐酸使固体完全溶解,收集到标准状况下的气体448.0 mL;b.称取等质量的晶体,灼烧至完全分解,得到2.400g残余固体。通过计算确定晶体的化学式(写出计算过程)。
您最近一年使用:0次
解题方法
3 . 辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如下:
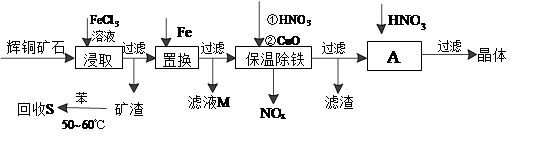
(1)写出浸取过程中Cu2S溶解的离子方程式____________ 。
(2)回收S过程中温度控制在50℃~60℃之间,不宜过高或过低的原因是_________ 、__________ 。
(3)保温除铁过程中加入CuO的目的是____________ 。
(4)A步操作为____________ 要用硝酸调节溶液的pH,其理由是____________ 。

(1)写出浸取过程中Cu2S溶解的离子方程式
(2)回收S过程中温度控制在50℃~60℃之间,不宜过高或过低的原因是
(3)保温除铁过程中加入CuO的目的是
(4)A步操作为
您最近一年使用:0次
解题方法
4 . 下列物质性质与应用对应关系正确的是
| A.铝合金熔点低,可用来制造门窗 |
| B.二氧化氯具有强氧化性,可用来漂白织物 |
| C.过氧化钠固体呈淡黄色,可用来做供氧剂 |
| D.硫酸铜溶于水呈酸性,可用来做杀菌剂 |
您最近一年使用:0次
2016-12-09更新
|
125次组卷
|
2卷引用:2015届江苏省南通市高三三模化学试卷
名校
解题方法
5 . 在如图所示的有关物质转化关系中,各物质均是我们中学化学所学的物质。C为一种黑色粉末,D为一种气体。
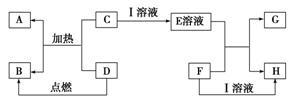
请根据框图中物质的转化关系及相关信息,用化学式填写下列空白:
(1)若F为可溶性碱,G为蓝色沉淀,则A为_________________ ;D可能为__________________ 。
(2)若G为蓝色沉淀,H为难溶性盐,则I为_________________ 。
(3)若G、H都属于盐,且G为蓝色溶液,则I可能为______________ ;F可能为_____________ 。

请根据框图中物质的转化关系及相关信息,用化学式填写下列空白:
(1)若F为可溶性碱,G为蓝色沉淀,则A为
(2)若G为蓝色沉淀,H为难溶性盐,则I为
(3)若G、H都属于盐,且G为蓝色溶液,则I可能为
您最近一年使用:0次
2016-12-09更新
|
387次组卷
|
2卷引用:江苏省扬州中学2020-2021学年高一上学期开学考暨奥赛选拔化学试题
名校
6 . 下物质间的转化通过一步化学反应不能实现的是
| A.Fe → Fe3O4 | B.CuO → Cu(OH)2 |
| C.HCl → Cl2 | D.Na → Na2O |
您最近一年使用:0次
2016-12-09更新
|
236次组卷
|
3卷引用:2014-2015江苏省南通中学高二上学期期末化学试卷
14-15高三上·江苏宿迁·阶段练习
名校
7 . 向一定量的Cu、Fe2O3的混合物中加入100 mL 2 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
| A.3.2 g | B.2.4 g | C.1.6 g | D.0.8 g |
您最近一年使用:0次
2016-12-09更新
|
349次组卷
|
8卷引用:2015届江苏省沭阳县银河学校高三上学期第一次阶段性检测化学试卷
8 . 我国古代“药金”的冶炼方法是:将炉甘石(ZnCO3)和赤铜矿(Cu2O)与木炭按一定的比例混合后加热至800℃,即可炼出闪烁似金子般光泽的“药金”。下列叙述正确的是
| A.“药金”实质上是铜锌合金 |
| B.冶炼炉中炉甘石直接被木炭还原为锌 |
| C.用王水可区别黄金和“药金” |
| D.用火焰灼烧不能区别黄金和药金 |
您最近一年使用:0次
2016-12-09更新
|
1193次组卷
|
11卷引用:2014年高一化学人教版必修二 4-1-1金属矿物的开发利用练习卷
(已下线)2014年高一化学人教版必修二 4-1-1金属矿物的开发利用练习卷山西省应县第一中学校2018-2019学年高一下学期期末考试化学试题2020届高三化学无机化学二轮专题复习——铜的氧化物的性质【选择精编26题】课时1 金属矿物的开发利用——A学习区 夯实基础(人教版必修2)课时1 金属矿物的开发利用——A学习区 夯实基础(人教版(2019)第二册)陕西省宝鸡中学2019-2020学年高一下学期期中考试化学试题必修第二册RJ第八章 第一节 课时1 金属矿物的开发利用(已下线)3.3 用途广泛的金属材料(基础练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)江苏省盐城市东台创新高级中学2021-2022学年高一4月份月检测化学试题(苏教版2019)必修第二册专题9 金属与人类文明 第一单元 金属的冶炼方法(已下线)第25讲 金属矿物的开发利用(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
12-13高三上·陕西咸阳·期末
9 . 有一铁粉和氧化铜的混合物6.96g,进行如下实验:
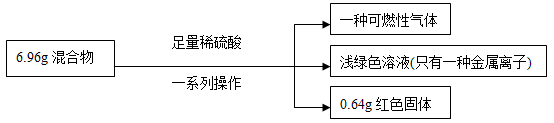
根据实验所得数据,关于混合物相关说法正确的是

根据实验所得数据,关于混合物相关说法正确的是
| A.生成气体质量为0.2g |
| B.原混合物中铁的质量分数无法计算 |
| C.实验中反应的H2SO4质量为10.78g |
| D.原混合物中铜元素的质量不一定为0.64g |
您最近一年使用:0次
2012·江苏·二模
解题方法
10 . 碱式碳酸铜的成分有多种,其化学式一般可表示为xCu(OH)2·yCuCO3。
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2·CuCO3,某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50 mol·L-1的Cu(NO3)2溶液、2.0mL 0.50 mol·L-1的NaOH溶液和0.25 mol·L-1的Na2CO3溶液按表Ⅰ所示体积混合。
实验2:将合适比例的混合物在表Ⅱ所示温度下反应。
实验记录如下:
①实验室制取少许孔雀石,应该采用的条件是___________ 。
②80℃时,所制得的孔雀石有少量褐色物质的原因是___________ 。
(2)实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:
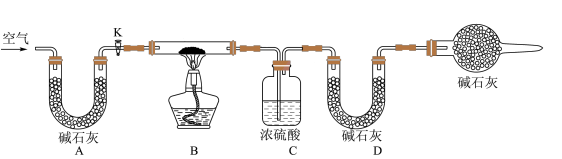
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中。
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量。
步骤3:加热装置B直至装置C中无气泡产生。
步骤4:___________ 。
步骤5:称量相关装置的质量。
①装置A的作用是___________ ;若无装置E,则实验测定的x/y的值将___________ (选填“偏大”、“偏小”或“无影响”)。
②某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量56.0g
C.装置C实验后增重9.0g
D.装置D实验后增重8.8g
为测定x/y的值,你认为可以选用上述所采集数据中的___________ (写出所有组合的字母代号)一组即可进行计算,并根据你的计算结果,写出该样品组成的化学式___________ 。
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2·CuCO3,某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50 mol·L-1的Cu(NO3)2溶液、2.0mL 0.50 mol·L-1的NaOH溶液和0.25 mol·L-1的Na2CO3溶液按表Ⅰ所示体积混合。
实验2:将合适比例的混合物在表Ⅱ所示温度下反应。
实验记录如下:
| 编号 | V (Na2CO3)/ mL | 沉淀情况 | 编号 | 反应温度/℃ | 沉淀情况 | |
| 1 | 2.8 | 多、蓝色 | 1 | 40 | 多、蓝色 | |
| 2 | 2.4 | 多、蓝色 | 2 | 60 | 少、浅绿色 | |
| 3 | 2.0 | 较多、绿色 | 3 | 75 | 较多、绿色 | |
| 4 | 1.6 | 较少、绿色 | 4 | 80 | 较多、绿色(少量褐色) | |
表Ⅰ | 表Ⅱ | |||||
②80℃时,所制得的孔雀石有少量褐色物质的原因是
(2)实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:

步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中。
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量。
步骤3:加热装置B直至装置C中无气泡产生。
步骤4:
步骤5:称量相关装置的质量。
①装置A的作用是
②某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量56.0g
C.装置C实验后增重9.0g
D.装置D实验后增重8.8g
为测定x/y的值,你认为可以选用上述所采集数据中的
您最近一年使用:0次



