2024高三·全国·专题练习
1 . H2S和CO2反应生成的羰基硫(COS)可用于粮食熏蒸,能防止某些昆虫、线虫和真菌的危害,反应热化学方程式为:CO2(g)+H2S(g) COS(g)+H2O(g);ΔH>0.下列说法正确的是
COS(g)+H2O(g);ΔH>0.下列说法正确的是
 COS(g)+H2O(g);ΔH>0.下列说法正确的是
COS(g)+H2O(g);ΔH>0.下列说法正确的是| A.上述反应中消耗34 g H2S,生成22.4 L水蒸气 |
B.上述反应的平衡常数K=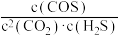 |
| C.已知该反应在加热条件下能自发进行,则其ΔS>0 |
| D.实际应用中,通过增加H2S的量来提高CO2的转化率,能有效减少碳排放 |
您最近一年使用:0次
2024高三·全国·专题练习
2 . CO2催化加氢合成二甲醚是一种CO2转化方法,其过程中主要发生下列反应:
Ⅰ. CO2(g)+H2(g) CO(g)+H2O(g);ΔH1;
CO(g)+H2O(g);ΔH1;
Ⅱ. 2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g);ΔH2。
CH3OCH3(g)+3H2O(g);ΔH2。
恒压条件下,投入1 mol CO2和适当过量的H2,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图所示。其中CH3OCH3的选择性= ×100%。
×100%。
Ⅰ. CO2(g)+H2(g)
 CO(g)+H2O(g);ΔH1;
CO(g)+H2O(g);ΔH1;Ⅱ. 2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g);ΔH2。
CH3OCH3(g)+3H2O(g);ΔH2。恒压条件下,投入1 mol CO2和适当过量的H2,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图所示。其中CH3OCH3的选择性=
 ×100%。
×100%。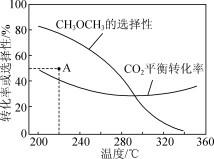
| A.ΔH1>0,ΔH2<0 |
| B.温度高于300 ℃,反应Ⅰ正向移动程度超过反应Ⅱ逆向移动程度 |
| C.220 ℃时,反应一段时间后,测得CH3OCH3的选择性为48%(即图中A点),此时反应Ⅰ和Ⅱ均未达到平衡状态 |
| D.若平衡时CH3OCH3的选择性为48%,则体系中c(CH3OCH3)∶c(CO)=48∶52 |
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
3 . 一定温度下,利用NH3催化还原NOx是目前应用广泛的烟气脱硝技术。一种以MnO2CeO2为催化剂处理NO的原理如图1所示。___________ 。
(2)该脱硝机理过程中的步骤Ⅰ可描述为___________ 。
(3)写出该脱硝过程中的化学方程式:___________ 。
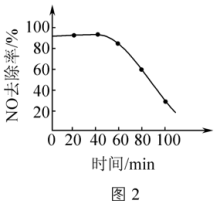
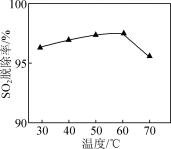
(4)为探究烟气中SO2的存在对脱硝性能的影响,在40min时向烟气中加入SO2,NO的去除率随时间变化如图2所示。试分析烟气中含有SO2导致NO去除率降低的原因:___________ 。
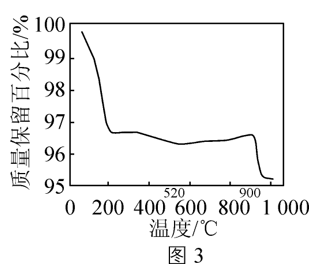
②MnO2分解为Mn2O3的最低理论温度是463℃。
结合催化剂脱硝机理,分析520~900℃范围内,催化剂重量开始增加的原因:___________ 。
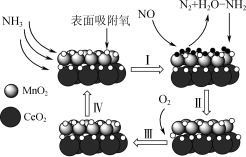 图1
图1
(2)该脱硝机理过程中的步骤Ⅰ可描述为
(3)写出该脱硝过程中的化学方程式:
(4)为探究烟气中SO2的存在对脱硝性能的影响,在40min时向烟气中加入SO2,NO的去除率随时间变化如图2所示。试分析烟气中含有SO2导致NO去除率降低的原因:
②MnO2分解为Mn2O3的最低理论温度是463℃。
结合催化剂脱硝机理,分析520~900℃范围内,催化剂重量开始增加的原因:
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
4 . 二甲醚是重要的有机合成原料,工业上常用合成气(主要成分为CO、H2)制备二甲醚,其主要反应如下。
反应ⅰ:CO(g)+2H2(g) CH3OH(g);
CH3OH(g);
反应ⅱ:2CH3OH(g) CH3OCH3(g)+H2O(g);
CH3OCH3(g)+H2O(g);
反应ⅲ:CO(g)+H2O(g) CO2(g)+H2(g)。
CO2(g)+H2(g)。
(1)一定温度下,在体积为2 L的刚性容器中充入4 mol CO(g)和8 mol H2(g)制备二甲醚,4 min时达到平衡,平衡时CO(g)的转化率为80%,c(H2)=1.4 mol·L-1,且c(CH3OH)=2c(CH3OCH3)。反应ⅲ的平衡常数Kc=_______ (保留三位有效数字)。
(2)实际工业生产中,需要在260 ℃、压强恒为4.0 MPa的反应釜中进行上述反应。初始时向反应釜中加入0.01 mol CO(g)和0.02 mol H2(g),为确保反应的连续性,需向反应釜中以n(CO)∶n(H2)=1∶2、进气流量0.03 mol·min-1持续通入原料,同时控制出气流量。①已知出气流量为0.02 mol·min-1,单位时间内CO(g)的转化率为60%,则流出气体中CO2(g)的百分含量为_______ 。②需控制出气流量小于进气流量的原因为_______ 。
(3)在ZnxO催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。______________ 。
②在合成甲醇过程中,需要不断分离出甲醇的原因为_______ 。
反应ⅰ:CO(g)+2H2(g)
 CH3OH(g);
CH3OH(g);反应ⅱ:2CH3OH(g)
 CH3OCH3(g)+H2O(g);
CH3OCH3(g)+H2O(g);反应ⅲ:CO(g)+H2O(g)
 CO2(g)+H2(g)。
CO2(g)+H2(g)。(1)一定温度下,在体积为2 L的刚性容器中充入4 mol CO(g)和8 mol H2(g)制备二甲醚,4 min时达到平衡,平衡时CO(g)的转化率为80%,c(H2)=1.4 mol·L-1,且c(CH3OH)=2c(CH3OCH3)。反应ⅲ的平衡常数Kc=
(2)实际工业生产中,需要在260 ℃、压强恒为4.0 MPa的反应釜中进行上述反应。初始时向反应釜中加入0.01 mol CO(g)和0.02 mol H2(g),为确保反应的连续性,需向反应釜中以n(CO)∶n(H2)=1∶2、进气流量0.03 mol·min-1持续通入原料,同时控制出气流量。①已知出气流量为0.02 mol·min-1,单位时间内CO(g)的转化率为60%,则流出气体中CO2(g)的百分含量为
(3)在ZnxO催化剂的作用下发生反应ⅰ,其可能反应机理如下图所示。
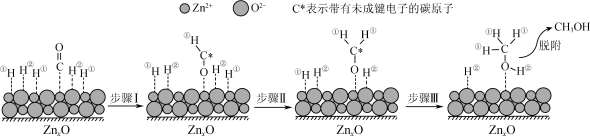
②在合成甲醇过程中,需要不断分离出甲醇的原因为
您最近一年使用:0次
2024高三·全国·专题练习
5 . 根据下列实验操作和现象,得出的结论正确的是
| 选项 | 实验操作与现象 | 实验结论 |
| A | 向一定浓度的FeCl2溶液中滴加少量酸性高锰酸钾溶液,高锰酸钾溶液紫红色褪去 | Fe2+具有还原性 |
| B | 向2 mL 0.1 mol·L-1KI(aq)中加入1 mL 0.1 mol·L-1 FeCl3(aq),充分反应,用四氯化碳充分萃取后取上层溶液滴加KSCN(aq),四氯化碳层显紫色,上层溶液试样变红 | I-和Fe3+的反应存在限度 |
| C | 在锌和稀硫酸的混合物中滴几滴CuSO4溶液,产生气体的速率加快 | CuSO4降低了锌和硫酸反应的活化能 |
| D | 二氧化锰和浓盐酸共热,产生气体的速率由慢到快 | 升温,活化分子百分率不变,活化分子总数增多 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
6 . CO2是一种常见的温室气体,也是巨大的碳资源。CO2可转化为CO、H2等燃料:CO2(g)+CH4(g)=2CO(g)+2H2(g);ΔH1=+247 kJ·mol-1。下列关于该反应的说法正确的是
| A.该反应在任何温度下都可自发进行 |
| B.反应CO2(s)+CH4(g)=2CO(g)+2H2(g);ΔH2<+247 kJ·mol-1 |
| C.反应中每生成1 mol H2,转移电子的数目为3×6.02×1023 |
| D.选择高效催化剂可以降低反应的焓变,提高化学反应速率 |
您最近一年使用:0次
2024高三·全国·专题练习
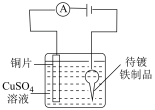
7 . 下图所示的实验能达到实验目的的是
|
|
| A.在铁件上镀铜 | B.验证AgCl溶解度大于AgI |
|
|
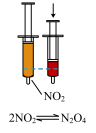
| C.推注射器,气体颜色变深,证明平衡逆向移动 | D.由FeCl3溶液制取无水FeCl3固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024高三下·全国·专题练习
8 . 用来表示可逆反应2A(g)+B(g) 2C(g);ΔH<0的正确图象为
2C(g);ΔH<0的正确图象为
 2C(g);ΔH<0的正确图象为
2C(g);ΔH<0的正确图象为A. | B. |
C. | D. |
您最近一年使用:0次
2024高三·全国·专题练习
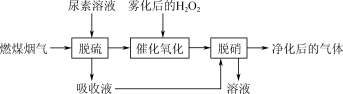
9 . 燃煤烟气中主要成分是空气,SO2和NO的含量小于1%。一种用CO(NH2)2(尿素)和H2O2在固体催化剂作用下脱硫、脱硝的流程如下:______ 。
(2)烟气中的NO与O2反应缓慢。雾化后的H2O2在催化剂中Fe元素作用下可以产生具有极强氧化活性的·OH(羟基自由基),·OH能将NO快速氧化为NO2、HNO3等物质。H2O2在一种固体催化剂表面转化的过程如图所示:______ 。
②转化(i)的过程可描述为______ 。
③化学式为LaFeO2.6的催化剂中,Fe3+和Fe2+的物质的量之比为______ 。
④其他条件一定,比较等物质的量LaFeO2.6与LaFeO2.8催化效果并说明理由:______ 。
(3)如不使用固体催化剂,用含Fe3+的溶液也能催化H2O2发生类似的转化生成·OH,且相同条件下速率更快。与使用含Fe3+的溶液相比,使用固体催化剂的优点是______ 。
(2)烟气中的NO与O2反应缓慢。雾化后的H2O2在催化剂中Fe元素作用下可以产生具有极强氧化活性的·OH(羟基自由基),·OH能将NO快速氧化为NO2、HNO3等物质。H2O2在一种固体催化剂表面转化的过程如图所示:
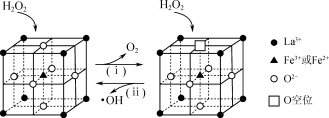
②转化(i)的过程可描述为
③化学式为LaFeO2.6的催化剂中,Fe3+和Fe2+的物质的量之比为
④其他条件一定,比较等物质的量LaFeO2.6与LaFeO2.8催化效果并说明理由:
(3)如不使用固体催化剂,用含Fe3+的溶液也能催化H2O2发生类似的转化生成·OH,且相同条件下速率更快。与使用含Fe3+的溶液相比,使用固体催化剂的优点是
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
10 . Ⅰ.H2S与CH4重整,不但可以消除污染,还可以制氢。主要反应为 ;ΔH>0。
;ΔH>0。
(1)在恒温恒容条件下,可作为上述反应达到平衡状态的判断依据的是_______。
Ⅱ.在恒压条件下,以n(CH4)∶n(H2S)=1∶2组成的混合气体发生反应: ;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。
;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。_______ 、_______ (填化学式)。
(3)M点对应温度下,H2S的转化率是_______ 。
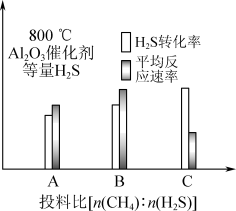
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH4会导致Al2O3催化剂失活;Co助剂有稳定催化剂的作用。如下图表示800 ℃,Al2O3催化剂条件下投入等量H2S,投料比[n(CH4)∶n(H2S)]分别为1∶1、1∶3、12∶1,达平衡时H2S转化率、平均反应速率。_______ (填“A”“B”或“C”)组图像。三组图像中,C组图像中平均反应速率最低的可能原因是_______ 。
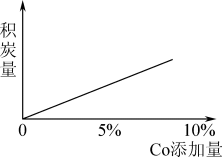
(5)未添加Co助剂时,无积炭,随着Co添加量的变化,积炭量变化如下图所示,Co助剂可能催化原料气发生反应的化学方程式为____ 。
 ;ΔH>0。
;ΔH>0。(1)在恒温恒容条件下,可作为上述反应达到平衡状态的判断依据的是_______。
| A.混合气体密度不变 |
| B.容器内压强不变 |
| C.2v正(H2S)=v逆(CS2) |
| D.CH4与H2的物质的量分数之比保持不变 |
Ⅱ.在恒压条件下,以n(CH4)∶n(H2S)=1∶2组成的混合气体发生反应:
 ;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。
;ΔH>0,达到平衡状态时,四种组分物质的量分数随温度的变化如下图所示。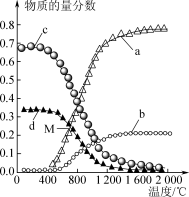
(3)M点对应温度下,H2S的转化率是
Ⅲ.在研究反应发生的适宜条件时发现:过多的CH4会导致Al2O3催化剂失活;Co助剂有稳定催化剂的作用。如下图表示800 ℃,Al2O3催化剂条件下投入等量H2S,投料比[n(CH4)∶n(H2S)]分别为1∶1、1∶3、12∶1,达平衡时H2S转化率、平均反应速率。
(5)未添加Co助剂时,无积炭,随着Co添加量的变化,积炭量变化如下图所示,Co助剂可能催化原料气发生反应的化学方程式为
您最近一年使用:0次