1 . 砷及其化合物有着广泛的用途。砷有两种常见的弱酸,砷酸(H3AsO4)和亚砷酸(H3AsO3)。已知砷酸(H3AsO4)的pKa1、pKa2、pKa3依次为2.25、6.77、11.40(pKa=-lgKa)。回答下列问题:
(1)已知:As(s)+ H2(g)+2O2(g)=H3AsO4(s) ΔHl
H2(g)+2O2(g)=H3AsO4(s) ΔHl
H2(g)+ O2(g)=H2O(1) ΔH2
O2(g)=H2O(1) ΔH2
As(s)+ O2(g)=
O2(g)= As2O5(s)ΔH3
As2O5(s)ΔH3
则反应As2O5(g)+3H2O(1)=2H3AsO4(s) ΔH=_________ 。
(2)写出砷酸(H3AsO4)的第二步电离方程式___________________________________ 。
(3)NaH2AsO4溶液呈______ (填“酸性”、“中性”或“碱性”),试通过计算说明________________________ 。
(4)亚砷酸(H3AsO3)水溶液中存在多种微粒形态,各种微粒分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液的pH关系如下图所示。

以酚酞为指示剂(变色范围pH:8.2~10.0),将NaOH溶液逐滴加入H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为__________________________ 。
(5)某化学兴趣小组同学欲探究可逆反应AsO +I2+2OH-
+I2+2OH- AsO
AsO +2I-+ H2O。设计如下图Ⅰ所示装置。实验操作及现象:按图Ⅰ装置加入试剂并连接装置,电流由C2流入C1。 当电流变为零时,向图Ⅰ装置左边烧杯中逐滴加入一定量2mol/L盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅱ所示。
+2I-+ H2O。设计如下图Ⅰ所示装置。实验操作及现象:按图Ⅰ装置加入试剂并连接装置,电流由C2流入C1。 当电流变为零时,向图Ⅰ装置左边烧杯中逐滴加入一定量2mol/L盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅱ所示。
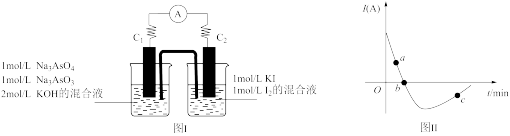
①图Ⅱ中AsO 的逆反应速率:a
的逆反应速率:a____ b( 填“ >”、” <”或“ =” )。
②写出图Ⅱ中c点对应图Ⅰ装置的正极反应式__________________________ 。
③能判断该反应达到平衡状态的是________________ 。
a.2v(I-)正=v(AsO )逆 b.溶液的pH不再变化
)逆 b.溶液的pH不再变化
c.电流表示数变为零 d.溶液颜色不再变化
(1)已知:As(s)+
 H2(g)+2O2(g)=H3AsO4(s) ΔHl
H2(g)+2O2(g)=H3AsO4(s) ΔHlH2(g)+
 O2(g)=H2O(1) ΔH2
O2(g)=H2O(1) ΔH2As(s)+
 O2(g)=
O2(g)= As2O5(s)ΔH3
As2O5(s)ΔH3则反应As2O5(g)+3H2O(1)=2H3AsO4(s) ΔH=
(2)写出砷酸(H3AsO4)的第二步电离方程式
(3)NaH2AsO4溶液呈
(4)亚砷酸(H3AsO3)水溶液中存在多种微粒形态,各种微粒分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液的pH关系如下图所示。

以酚酞为指示剂(变色范围pH:8.2~10.0),将NaOH溶液逐滴加入H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为
(5)某化学兴趣小组同学欲探究可逆反应AsO
 +I2+2OH-
+I2+2OH- AsO
AsO +2I-+ H2O。设计如下图Ⅰ所示装置。实验操作及现象:按图Ⅰ装置加入试剂并连接装置,电流由C2流入C1。 当电流变为零时,向图Ⅰ装置左边烧杯中逐滴加入一定量2mol/L盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅱ所示。
+2I-+ H2O。设计如下图Ⅰ所示装置。实验操作及现象:按图Ⅰ装置加入试剂并连接装置,电流由C2流入C1。 当电流变为零时,向图Ⅰ装置左边烧杯中逐滴加入一定量2mol/L盐酸,发现又产生电流,实验中电流与时间的关系如图Ⅱ所示。
①图Ⅱ中AsO
 的逆反应速率:a
的逆反应速率:a②写出图Ⅱ中c点对应图Ⅰ装置的正极反应式
③能判断该反应达到平衡状态的是
a.2v(I-)正=v(AsO
 )逆 b.溶液的pH不再变化
)逆 b.溶液的pH不再变化c.电流表示数变为零 d.溶液颜色不再变化
您最近一年使用:0次
名校
2 . 氨气是重要的化工原料。
(1)已知: N2(g)+O2(g)=2NO(g) △H= +180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H= -905kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H= -483.6kJ·mol-1
写出氨气在高温高压催化剂条件下生成氮气和氢气的热化学方程式:_____________________ ;如果在1 L密闭容器中,3mol NH3 在等温条件下充分反应,2min后达到平衡,平衡时吸收的热量为92.4 kJ ,则在这段时间内v(H2)=___________________ ;保持温度不变,将起始NH3的物质的量调整为8 mol,平衡时NH3的转化率为_________________ 。
(2)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:___________________ ,科学家利用此原理,设计成氨气一氧气燃料电池,则通入氨气的电极是 _____________ (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为______________________________________ 。
(3)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H<0。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是
4NO(g)+6H2O(g) △H<0。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是____________ (填字母代号)。
a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(4)如果某氨水的电离程度为1%,向浓度为0.01 mol/L MgCl2溶液中滴加氨水,则开始产生沉淀时(忽略溶液体积变化)溶液中的NH3·H2O的浓度为______________ (已知Ksp[Mg(OH)2]=4.010-12])。
(1)已知: N2(g)+O2(g)=2NO(g) △H= +180.5kJ·mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H= -905kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H= -483.6kJ·mol-1
写出氨气在高温高压催化剂条件下生成氮气和氢气的热化学方程式:
(2)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:
(3)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H<0。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是
4NO(g)+6H2O(g) △H<0。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(4)如果某氨水的电离程度为1%,向浓度为0.01 mol/L MgCl2溶液中滴加氨水,则开始产生沉淀时(忽略溶液体积变化)溶液中的NH3·H2O的浓度为
您最近一年使用:0次
解题方法
3 . 回答下列问题:
Ⅰ.我国力争于2030年前做到“碳达峰”,2060年前实现“碳中和”。二氧化碳加氢制备甲醇既可以实现二氧化碳的转化利用,又可以有效缓解温室效应问题。
已知:反应①: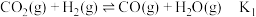
反应②: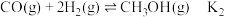
反应③: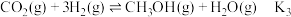
(1)原料CO2可通过捕获技术从空气或工业尾气中获取,下列物质能作为CO2捕获剂的是___________。(填标号)。
(2)平衡常数之间的关系为表示K3=___________ (用K1和K2表示)
Ⅱ.脱硝技术、含氮燃料是新的发展方向和研究热点,有着广泛的应用前景。
(3)在新型催化剂条件下NH3与NO和NO2(其中V(NO):V(NO2)=1:1)的混合气体反应生成N2,当生成1 mol N2时,转移的电子为___________ mol。
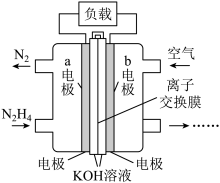
(4)肼(N2H4)可以用作燃料电池的原料。肼的电子式为___________ ;一种以液态肼为燃料的电池装置如图所示。b电极是___________ 极(填“正”或“负”),a电极的电极反应式为___________ 。
(5)用KMnO4也可高效脱除烟气中的NO,NO被氧化为 ,碱性条件下
,碱性条件下 被还原为
被还原为 。该反应的离子方程式为
。该反应的离子方程式为___________ 。
(6)实验室中利用KMnO4进行如下实验(假设每步反应完全进行),下列说法错误的是___________。

Ⅰ.我国力争于2030年前做到“碳达峰”,2060年前实现“碳中和”。二氧化碳加氢制备甲醇既可以实现二氧化碳的转化利用,又可以有效缓解温室效应问题。
已知:反应①:
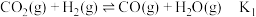
反应②:
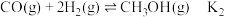
反应③:
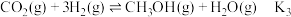
(1)原料CO2可通过捕获技术从空气或工业尾气中获取,下列物质能作为CO2捕获剂的是___________。(填标号)。
| A.NaOH溶液 | B.浓氨水 | C.生石灰 | D.NH4Cl溶液 |
Ⅱ.脱硝技术、含氮燃料是新的发展方向和研究热点,有着广泛的应用前景。
(3)在新型催化剂条件下NH3与NO和NO2(其中V(NO):V(NO2)=1:1)的混合气体反应生成N2,当生成1 mol N2时,转移的电子为
(4)肼(N2H4)可以用作燃料电池的原料。肼的电子式为

(5)用KMnO4也可高效脱除烟气中的NO,NO被氧化为
 ,碱性条件下
,碱性条件下 被还原为
被还原为 。该反应的离子方程式为
。该反应的离子方程式为(6)实验室中利用KMnO4进行如下实验(假设每步反应完全进行),下列说法错误的是___________。

| A.G与H均为氧化产物 | B.实验中KMnO4只作氧化剂 |
| C.Mn元素参与了3个氧化还原反应 | D.G与H的物质的量之和可能为0.25 mol |
您最近一年使用:0次
名校
解题方法
4 . 氢气是一种高能燃料,也广泛应用在工业合成中。
(1)标准摩尔生成焓是指在25℃和101kPa,最稳定的单质生成1mol化合物的焓变。已知25℃和101kPa
时下列反应:
①2C2H6(g)+7O2(g)=4CO2(g) +6H2O(l) △H=-3116 kJ·mol-1
②C(石墨,s)+O2(g) =CO2(g) △H=-393.5 kJ·mol-1
③2H2(g)+O2(g) =2H2O(l) △H=-571.6 kJ·mol-1
写出乙烷标准生成焓的热化学方程式:___________________________________________ 。
(2)已知合成氨的反应为:N2+3H2 2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:

①图中代表反应在恒容绝热容器中进行的曲线是______ (用a、b、c表示)
②曲线a条件下该反应的平衡常数K=_________ 。
③b容器中M点,v(正)____ v(逆)(填“大于”、“小于”或“等于”)
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为______ ;标准状况下,当阴极收集到11.2 LN2时,理论上消耗NH3的体积为_____ 。
(4)氨水是制备铜氨溶液的常用试剂,通过以下反应及数据来探究配制铜氨溶液的最佳途径。
已知:Cu(OH)2(s) ⇌Cu2++2OH- Ksp=2.2×10-20
Cu2++4NH3·H2O ⇌[Cu (NH3) 4]2+(深蓝色)+4H2O Kβ=7.24×1012
①请用数据说明利用该反应:Cu(OH)2(s) +4NH3·H2O ⇌[Cu (NH3) 4]2++4H2O+2OH-配制铜氨溶液是否可行:_________________________________________ 。
②已知反应Cu(OH)2(S) +2NH3·H2O+2NH 4+⇌[Cu (NH3) 4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol·L-1的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为_______________ ;解释出现该现象的原因是_____________________ 。
(1)标准摩尔生成焓是指在25℃和101kPa,最稳定的单质生成1mol化合物的焓变。已知25℃和101kPa
时下列反应:
①2C2H6(g)+7O2(g)=4CO2(g) +6H2O(l) △H=-3116 kJ·mol-1
②C(石墨,s)+O2(g) =CO2(g) △H=-393.5 kJ·mol-1
③2H2(g)+O2(g) =2H2O(l) △H=-571.6 kJ·mol-1
写出乙烷标准生成焓的热化学方程式:
(2)已知合成氨的反应为:N2+3H2
 2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
2NH3 △H<0。某温度下,若将1mol N2和2.8mol H2分别投入到初始体积为2L的恒温恒容、恒温恒压和恒容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请回答下列问题:
①图中代表反应在恒容绝热容器中进行的曲线是
②曲线a条件下该反应的平衡常数K=
③b容器中M点,v(正)
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为
(4)氨水是制备铜氨溶液的常用试剂,通过以下反应及数据来探究配制铜氨溶液的最佳途径。
已知:Cu(OH)2(s) ⇌Cu2++2OH- Ksp=2.2×10-20
Cu2++4NH3·H2O ⇌[Cu (NH3) 4]2+(深蓝色)+4H2O Kβ=7.24×1012
①请用数据说明利用该反应:Cu(OH)2(s) +4NH3·H2O ⇌[Cu (NH3) 4]2++4H2O+2OH-配制铜氨溶液是否可行:
②已知反应Cu(OH)2(S) +2NH3·H2O+2NH 4+⇌[Cu (NH3) 4]2++4H2O K=5.16×102。向盛有少量Cu(OH)2固体的试管中加入14 mol·L-1的氨水,得到悬浊液;此时若加入适量的硫酸铵固体,出现的现象为
您最近一年使用:0次
2017-03-15更新
|
631次组卷
|
4卷引用:湖北省黄冈中学2020届高三2月月考理综化学试题
解题方法
5 . 纯过氧化氢(H2O2)是淡蓝色的黏稠液体,可任意比例与水混溶,广泛应用于医疗消毒、绿色化学合成等领域。回答下列问题:
(1)已知:H2(g)+ O2(g)=H2O(l)∆H1=-286kJ·mol-1
O2(g)=H2O(l)∆H1=-286kJ·mol-1
H2(g)+O2(g)=H2O2(l)∆H2=-188kJ·mol-1
过氧化氢分解反应2H2O2(l)=2H2O(l)+O2(g)的∆H=_____ kJ·mol-1。
(2)100℃时,在不同金属离子存在下,纯过氧化氢24h的分解率见下表:
①由上表数据可知,能使过氧化氢分解反应活化能降低最多的离子是____ 。贮运过氧化氢时,可选用的容器材质为____ (填标号)。
A.不锈钢 B.纯铝 C.黄铜 D.铸铁
②已知反应:H2O2(l)=H2O(1)+ O2(g)K=2.88×1020。纯H2O2相对稳定,原因是H2O2分解反应的
O2(g)K=2.88×1020。纯H2O2相对稳定,原因是H2O2分解反应的___ (填编号)。
A.ΔH比较小 B.K不够大 C.速率比较小 D.活化能比较大
(3)H2O2的强氧化性使其对大多数致病菌和病毒具有消杀功能。用3%医用H2O2对传染病房喷洒消毒时,地板上有气泡冒出,该气体是___ 。
(4)过氧化氢的制备方法很多,早期制备方法如下:
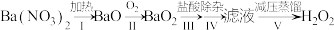
①Ⅰ为分解反应,产物除BaO、O2外,还有一种红棕色气体。该反应的化学方程式是___ 。
②Ⅱ为可逆反应,促进该反应正向进行的措施是___ (答一条即可)。
(1)已知:H2(g)+
 O2(g)=H2O(l)∆H1=-286kJ·mol-1
O2(g)=H2O(l)∆H1=-286kJ·mol-1H2(g)+O2(g)=H2O2(l)∆H2=-188kJ·mol-1
过氧化氢分解反应2H2O2(l)=2H2O(l)+O2(g)的∆H=
(2)100℃时,在不同金属离子存在下,纯过氧化氢24h的分解率见下表:
| 离子 | 加入量(mg·L-1) | 分解率% | 离子 | 加入量(mg·L-1) | 分解率% |
| 无 | 0 | 2 | Fe3+ | 1.0 | 15 |
| Al3+ | 10 | 2 | Cu2+ | 0.1 | 86 |
| Zn2+ | 10 | 10 | Cr3+ | 0.1 | 96 |
①由上表数据可知,能使过氧化氢分解反应活化能降低最多的离子是
A.不锈钢 B.纯铝 C.黄铜 D.铸铁
②已知反应:H2O2(l)=H2O(1)+
 O2(g)K=2.88×1020。纯H2O2相对稳定,原因是H2O2分解反应的
O2(g)K=2.88×1020。纯H2O2相对稳定,原因是H2O2分解反应的A.ΔH比较小 B.K不够大 C.速率比较小 D.活化能比较大
(3)H2O2的强氧化性使其对大多数致病菌和病毒具有消杀功能。用3%医用H2O2对传染病房喷洒消毒时,地板上有气泡冒出,该气体是
(4)过氧化氢的制备方法很多,早期制备方法如下:
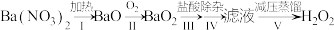
①Ⅰ为分解反应,产物除BaO、O2外,还有一种红棕色气体。该反应的化学方程式是
②Ⅱ为可逆反应,促进该反应正向进行的措施是
您最近一年使用:0次
解题方法
6 . Ⅰ.二甲醚又称甲醚,简称DME,结构简式为 ,是一种无色气体,被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,在医药、燃料、农药工业中有许多独特的用途。
,是一种无色气体,被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,在医药、燃料、农药工业中有许多独特的用途。
(1)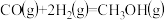
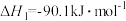

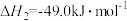

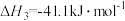

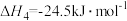
由H2和CO直接制备二甲酵(另一产物为水蒸气)的热化学方程式为___________
(2)T℃时,在2L密闭容器中充入4molCO和8molH2发生制备二甲醚的反应: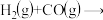
 (没有配平),测得环的物质的量随时间的变化情况如图中状态Ⅰ所示。
(没有配平),测得环的物质的量随时间的变化情况如图中状态Ⅰ所示。
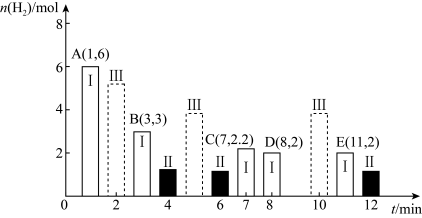
①T℃时,反应的平衡常数K1=___________ 。
②若仅改变某一条件,测得B的物质的最随时间的变化情况如图中状态Ⅱ所示,则K1___________ K2(填“>”、“<”或“=”)。
③若仅改变某一条件,测得B的物质的量随时间的变化情况如图中状态Ⅲ所示,则改变的条件可能是___________ 。
(3)燃料电池是一种绿色环保、高效的化学电源。二甲醚还可作燃料电池的燃料,以熔融 作为电解质,一极充入二甲醚,另一极充入空气和
作为电解质,一极充入二甲醚,另一极充入空气和 气体,该电池的负极反应式为
气体,该电池的负极反应式为___________ 。用该二甲醚燃料电池电解300mL饱和食盐水。电解一段时间后,当溶液的pH值为13(室温下测定)时,消耗二甲醛的质量为___________ g.(忽略溶液体积变化,不考虑损耗)
Ⅱ.25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)25℃时,0.1mol/L的 溶液呈
溶液呈___________ (填“酸性”、“碱性”或“中性”)
(2)用足量 溶液吸收工业尾气中少量SO2气体,发生反应的离子方程式为
溶液吸收工业尾气中少量SO2气体,发生反应的离子方程式为___________ 。
(3)25℃时,取浓度均为0.1000mol/L的醋酸溶液和氨水溶液各20.00mL,分别用0.1000mol/LNaOH溶液、0.1000mol/L盐酸进行中和滴定,滴定过程中溶液pH随滴加溶液的体积变化关系如图所示。下列说法错误的是_____________
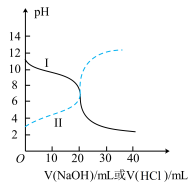
a.曲线Ⅰ,滴加溶液到10mL时: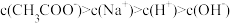
b.当NaOH溶液和盐酸滴加至20.00mL时,曲线Ⅰ和Ⅱ刚好相交
c.曲线Ⅱ:滴加溶液到10.00mL时,溶液中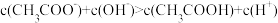
d.在逐滴加入NaOH溶液或盐酸至40.00mL的过程中,水的电离程度先增大后减小
 ,是一种无色气体,被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,在医药、燃料、农药工业中有许多独特的用途。
,是一种无色气体,被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,在医药、燃料、农药工业中有许多独特的用途。(1)
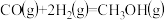
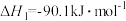

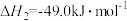

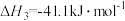

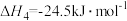
由H2和CO直接制备二甲酵(另一产物为水蒸气)的热化学方程式为
(2)T℃时,在2L密闭容器中充入4molCO和8molH2发生制备二甲醚的反应:
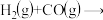
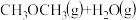 (没有配平),测得环的物质的量随时间的变化情况如图中状态Ⅰ所示。
(没有配平),测得环的物质的量随时间的变化情况如图中状态Ⅰ所示。
①T℃时,反应的平衡常数K1=
②若仅改变某一条件,测得B的物质的最随时间的变化情况如图中状态Ⅱ所示,则K1
③若仅改变某一条件,测得B的物质的量随时间的变化情况如图中状态Ⅲ所示,则改变的条件可能是
(3)燃料电池是一种绿色环保、高效的化学电源。二甲醚还可作燃料电池的燃料,以熔融
 作为电解质,一极充入二甲醚,另一极充入空气和
作为电解质,一极充入二甲醚,另一极充入空气和 气体,该电池的负极反应式为
气体,该电池的负极反应式为Ⅱ.25℃时,部分物质的电离平衡常数如表所示:
| 化学式 |  |  |  |  |  |
| 电离平衡常数 |  |  |   |   |   |
(1)25℃时,0.1mol/L的
 溶液呈
溶液呈(2)用足量
 溶液吸收工业尾气中少量SO2气体,发生反应的离子方程式为
溶液吸收工业尾气中少量SO2气体,发生反应的离子方程式为(3)25℃时,取浓度均为0.1000mol/L的醋酸溶液和氨水溶液各20.00mL,分别用0.1000mol/LNaOH溶液、0.1000mol/L盐酸进行中和滴定,滴定过程中溶液pH随滴加溶液的体积变化关系如图所示。下列说法错误的是

a.曲线Ⅰ,滴加溶液到10mL时:
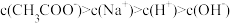
b.当NaOH溶液和盐酸滴加至20.00mL时,曲线Ⅰ和Ⅱ刚好相交
c.曲线Ⅱ:滴加溶液到10.00mL时,溶液中
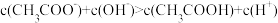
d.在逐滴加入NaOH溶液或盐酸至40.00mL的过程中,水的电离程度先增大后减小
您最近一年使用:0次
解题方法
7 . 氮氧化物(NOx)是严重的大气污染物,能引起雾霾、光化学烟雾、酸雨等环境问题。回答下列问题:
(1)氧化还原法消除NOx的转化如下:
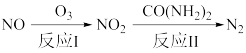
已知:NO(g)+O3(g)=NO2(g)+O2(g)△H=-201kJ·mol-1
2NO(g)+O2(g)=2NO2(g)△H=-116kJ·mol-1
反应I只有一种生成物,则反应I的热化学方程式为_______________ 。
(2)柴油机氮氧化物(NOx)处理技术是一种系统简单,占用空间较小的柴油车尾气处理技术,氮氧化物主要在催化转化装置中被处理。柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,催化转化装置中的物质变化如图所示。
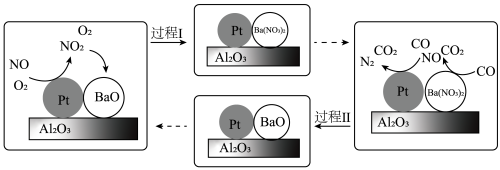
①BaO吸收NO2的化学方程式是______________ 。
②研究CO2对BaO吸收氮氧化物的影响,一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如图所示。

下列相关分析中正确的是_______________ 。
A.一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因可能是BaO与CO2反应生成BaCO3,覆盖在BaO表面
B.当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,其原因可能是BaCO3在一定程度上也能吸收NOx
C.若柴油中硫含量较高,在稀燃过程中,柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaO吸收氮氧化物的能力会下降至较低水平
D.以上分析均不对
(3)用食盐水作电解液电解烟气脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为 ,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
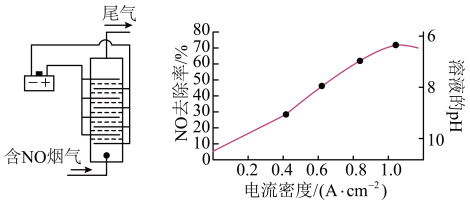
①NO被阳极产生的氧化性物质氧化为 反应的离子方程式为
反应的离子方程式为_______________ 。
②溶液的pH对NO去除率影响的原因是_______________ 。
(1)氧化还原法消除NOx的转化如下:
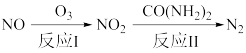
已知:NO(g)+O3(g)=NO2(g)+O2(g)△H=-201kJ·mol-1
2NO(g)+O2(g)=2NO2(g)△H=-116kJ·mol-1
反应I只有一种生成物,则反应I的热化学方程式为
(2)柴油机氮氧化物(NOx)处理技术是一种系统简单,占用空间较小的柴油车尾气处理技术,氮氧化物主要在催化转化装置中被处理。柴油发动机工作时在稀燃(O2充足、柴油较少)和富燃(O2不足、柴油较多)条件下交替进行,催化转化装置中的物质变化如图所示。

①BaO吸收NO2的化学方程式是
②研究CO2对BaO吸收氮氧化物的影响,一定温度下,测得气体中CO2的体积分数与氮氧化物吸收率的关系如图所示。

下列相关分析中正确的是
A.一定范围内,氮氧化物吸收率随CO2体积分数的增大而下降,原因可能是BaO与CO2反应生成BaCO3,覆盖在BaO表面
B.当CO2体积分数达到10%~20%时,氮氧化物吸收率依然较高,其原因可能是BaCO3在一定程度上也能吸收NOx
C.若柴油中硫含量较高,在稀燃过程中,柴油中的硫氧化为SO2,2BaO+2SO2+O2=2BaSO4,BaO吸收氮氧化物的能力会下降至较低水平
D.以上分析均不对
(3)用食盐水作电解液电解烟气脱氮的原理如图所示,NO被阳极产生的氧化性物质氧化为
 ,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
,尾气经氢氧化钠溶液吸收后排入空气。电流密度和溶液pH对烟气脱氮的影响如图所示。
①NO被阳极产生的氧化性物质氧化为
 反应的离子方程式为
反应的离子方程式为②溶液的pH对NO去除率影响的原因是
您最近一年使用:0次
2020-09-25更新
|
442次组卷
|
2卷引用:湖北省黄冈市2021届高三9月质量检测化学试题
8 . 一定条件下二氧化碳和乙苯反应可得到苯乙烯,其热化学方程式为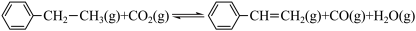
 。
。
已知:在标准大气压下,由最稳定的单质生成1mol某物质反应的焓变,为该物质的标准摩尔生成焓,用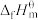 表示,稳定单质的标准摩尔生成焓为0.一些物质的标准摩尔生成焓如表所示:
表示,稳定单质的标准摩尔生成焓为0.一些物质的标准摩尔生成焓如表所示:
回答下列问题:
(1)已知:i.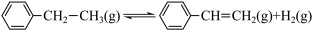
 ;
;
ii.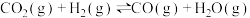
 。
。
①
___________  ,1个
,1个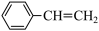 分子中含有
分子中含有___________ 个 键。
键。
②恒温恒容的条件下进行反应: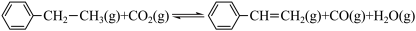 ,下列事实不能作为该反应达到平衡的依据的是
,下列事实不能作为该反应达到平衡的依据的是___________ (填字母)。
a.单位时间内减少乙苯的物质的量与二氧化碳增加量相同
b.容器内气体密度不再变化
c.容器内气体的平均相对分子质量不再变化
d.苯乙烯的体积分数不再变化
(2)一定温度下,将2mol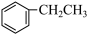 和2mol
和2mol 充入体积为2L的恒容密闭容器中,压强为
充入体积为2L的恒容密闭容器中,压强为 ,10min后达平衡,此时压强为
,10min后达平衡,此时压强为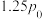 。
。
(1)前10min,该反应的平均反应速率
___________  ,乙苯的平衡转化率为
,乙苯的平衡转化率为___________ ,该温度下该反应的化学平衡常数
___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)在固定投料比(乙苯与二氧化碳物质的量之比)的条件下,实验测得乙苯的平衡转化率与温度(T)、压强(p)的关系如图所示,下列说法正确的是___________ (填字母)。
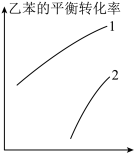
a.横坐标表示温度, b.横坐标表示温度,
b.横坐标表示温度,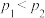
c.横坐标表示压强, d.横坐标表示压强,
d.横坐标表示压强,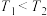
(3)一定条件下,将反应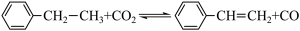 设计为电解池,电解质溶液为酸性有机介质。阳极电极反应式为
设计为电解池,电解质溶液为酸性有机介质。阳极电极反应式为___________ 。
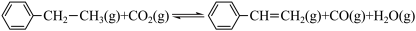
 。
。已知:在标准大气压下,由最稳定的单质生成1mol某物质反应的焓变,为该物质的标准摩尔生成焓,用
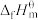 表示,稳定单质的标准摩尔生成焓为0.一些物质的标准摩尔生成焓如表所示:
表示,稳定单质的标准摩尔生成焓为0.一些物质的标准摩尔生成焓如表所示:| 物质 |  |  | 乙苯 | 苯乙烯 |
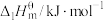 | 0 | 0 | 29.8 | 147.4 |
(1)已知:i.
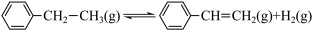
 ;
;ii.
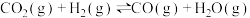
 。
。①

 ,1个
,1个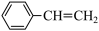 分子中含有
分子中含有 键。
键。②恒温恒容的条件下进行反应:
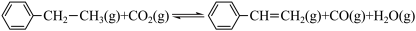 ,下列事实不能作为该反应达到平衡的依据的是
,下列事实不能作为该反应达到平衡的依据的是a.单位时间内减少乙苯的物质的量与二氧化碳增加量相同
b.容器内气体密度不再变化
c.容器内气体的平均相对分子质量不再变化
d.苯乙烯的体积分数不再变化
(2)一定温度下,将2mol
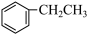 和2mol
和2mol 充入体积为2L的恒容密闭容器中,压强为
充入体积为2L的恒容密闭容器中,压强为 ,10min后达平衡,此时压强为
,10min后达平衡,此时压强为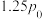 。
。(1)前10min,该反应的平均反应速率

 ,乙苯的平衡转化率为
,乙苯的平衡转化率为
(2)在固定投料比(乙苯与二氧化碳物质的量之比)的条件下,实验测得乙苯的平衡转化率与温度(T)、压强(p)的关系如图所示,下列说法正确的是

a.横坐标表示温度,
 b.横坐标表示温度,
b.横坐标表示温度,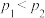
c.横坐标表示压强,
 d.横坐标表示压强,
d.横坐标表示压强,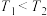
(3)一定条件下,将反应
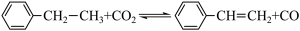 设计为电解池,电解质溶液为酸性有机介质。阳极电极反应式为
设计为电解池,电解质溶液为酸性有机介质。阳极电极反应式为
您最近一年使用:0次
解题方法
9 . H2S是存在于燃气中的一种有害气体,脱除H2S的方法有很多。
(1)国内有学者设计了“Cu2+一沉淀氧化”法脱除H2S。该法包括生成CuS沉淀,氧化CuS(Cu2++CuS+4Cl—=S+2CuCl2—)及空气氧化CuCl2—再生Cu2+。
①反应H2S(aq)+Cu2+(aq)⇌CuS(s)+2H+(aq)的K=__________
②再生Cu2+反应的离子方程式为____________ 。
(2)采用生物脱硫技术时,H2S与碱反应转化为HS-,在脱氮硫杆菌参与下,HS-被NO3-氧化为SO42—、NO3—被还原为N2。当33.6 m3(标准状况)某燃气(H2S的含量为0.2%)脱硫时,消耗NO3—的物质的量为___ mol。
(3)已知下列热化学方程式:
Ⅰ.H2(g)+ O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1
O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1
Ⅱ. H2(g)+S(s)=H2S(g) ∆H2=-20.6kJ∙mol-1
Ⅲ.S(s)+O2(g)=SO2(g) ∆H3=-296.8kJ∙mol-1
则以Claus法脱除H2S的反应:2H2S(g)+SO2 (g)=3S(s)+2H2O(1) △H=________ kJ/mol。
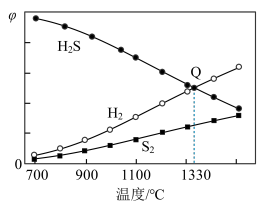
(4)101 kPa下,H2S分解:2H2S(g) ⇌ 2H2(g)+S2(g)。保持压强不变,反应达到平衡时,气体的体积分数(φ)随温度的变化曲线如图:
①在密闭容器中,关于反应2H2S(g) ⇌ 2H2(g)+S2 (g)的说法正确的是____ (填字母)。
A.Kp随温度的升高而增大
B.低压有利于提高HpS的平衡分解率
C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则v(正)<v(逆)
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中Q点:H2S的平衡转化率为____ ;S2(g)的分压为____ kPa;1330℃时,反应2H2S(g) ⇌ 2H2(g)+S2(g)的Kp=_____ (Kp为以分压表示的平衡常数)。
(1)国内有学者设计了“Cu2+一沉淀氧化”法脱除H2S。该法包括生成CuS沉淀,氧化CuS(Cu2++CuS+4Cl—=S+2CuCl2—)及空气氧化CuCl2—再生Cu2+。
①反应H2S(aq)+Cu2+(aq)⇌CuS(s)+2H+(aq)的K=
②再生Cu2+反应的离子方程式为
(2)采用生物脱硫技术时,H2S与碱反应转化为HS-,在脱氮硫杆菌参与下,HS-被NO3-氧化为SO42—、NO3—被还原为N2。当33.6 m3(标准状况)某燃气(H2S的含量为0.2%)脱硫时,消耗NO3—的物质的量为
(3)已知下列热化学方程式:
Ⅰ.H2(g)+
 O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1
O2(g)=H2O(l) ∆H1=-285.8kJ∙mol-1Ⅱ. H2(g)+S(s)=H2S(g) ∆H2=-20.6kJ∙mol-1
Ⅲ.S(s)+O2(g)=SO2(g) ∆H3=-296.8kJ∙mol-1
则以Claus法脱除H2S的反应:2H2S(g)+SO2 (g)=3S(s)+2H2O(1) △H=
(4)101 kPa下,H2S分解:2H2S(g) ⇌ 2H2(g)+S2(g)。保持压强不变,反应达到平衡时,气体的体积分数(φ)随温度的变化曲线如图:

①在密闭容器中,关于反应2H2S(g) ⇌ 2H2(g)+S2 (g)的说法正确的是
A.Kp随温度的升高而增大
B.低压有利于提高HpS的平衡分解率
C.维持温度、气体总压强不变时,向平衡体系中通入氩气,则v(正)<v(逆)
D.在恒容密闭容器中进行反应,当气体密度不再变化时,反应达到平衡状态
②图中Q点:H2S的平衡转化率为
您最近一年使用:0次
2020-01-31更新
|
336次组卷
|
3卷引用:2019年湖北省十堰市高三元月调研考试理综化学试题
10 . 研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:
Fe2O3(s)+3CO(s,石墨)═2Fe(s)+3CO2(g)△H1=+489.0kJ•mol﹣1
C(s,石墨)+CO2(g)═2CO(g)△H2=+172.5kJ•mol﹣1
则CO还原Fe2O3(s)的热化学方程式为_____ 。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H
CH3OH(g)+H2O(g)△H
①取一定体积CO2和H2的混合气体(物质的量之比为1:3),加入恒容密闭容器中,发生上述反应反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的△H____ 0(填“>”、“<”或“=”,下同)。
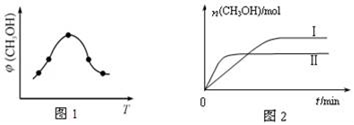
②在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数关系为KⅠ_____ KⅡ。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成.开始以氨碳比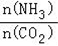 =3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为_____ 。
②将足量CO2通入饱和氨水中可得氮肥NH4HCO3,已知常温下一水合氨Kb=1.8×10﹣5,碳酸一级电离常数Ka=4.3×10﹣7,则NH4HCO3溶液呈_____ (填“酸性”、“中性”或“碱性”)。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:
Fe2O3(s)+3CO(s,石墨)═2Fe(s)+3CO2(g)△H1=+489.0kJ•mol﹣1
C(s,石墨)+CO2(g)═2CO(g)△H2=+172.5kJ•mol﹣1
则CO还原Fe2O3(s)的热化学方程式为
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H
CH3OH(g)+H2O(g)△H①取一定体积CO2和H2的混合气体(物质的量之比为1:3),加入恒容密闭容器中,发生上述反应反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的△H

②在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数关系为KⅠ
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成.开始以氨碳比
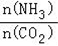 =3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为②将足量CO2通入饱和氨水中可得氮肥NH4HCO3,已知常温下一水合氨Kb=1.8×10﹣5,碳酸一级电离常数Ka=4.3×10﹣7,则NH4HCO3溶液呈
您最近一年使用:0次
2017-03-06更新
|
293次组卷
|
2卷引用:2016-2017学年湖北省宜昌市部分重点中学高二上学期期末考试化学试卷



